Intraoperativ strålbehandling vid tidig bröstcancer har jämförts med extern postoperativ strålbehandling i en stor multicenterstudie kallad TARGIT-A.
Medan intraoperativ strålbehandling har varit standardiserad har jämförelsebehandling följt lokala rutiner vid olika centrum, och därmed har både stråldoser och duration varierat påtagligt.
Studien lider av så allvarliga brister att de utgör hinder för införande av metoden i svensk rutinsjukvård.
NICE i Storbritannien har nyligen ändrat sin rekommendation rörande metoden till en mer restriktiv hållning, innebärande att man behåller befintliga Intrabeam-utrustningar, men avstår från investeringar i nya.
Det finns i dag stark evidens för att vid bröstcancer enbart avlägsna själva tumören (bröstbevarande behandling) och efteråt ge strålbehandling [1-4]. Strålbehandling kan ges i olika former:
1) brakyterapi med flera katetrar som lämnas i bröstet under en tid efter kirurgisk behandling
2) brakyterapi med ballong som lämnas i det hålrum som finns i bröstet efter att tumören avlägsnats
3) extern strålbehandling av de delar av bröstet som är närmast avlägsnad tumör (den bäst etablerade formen av strålbehandling)
4) intraoperativ strålbehandling av de delar av bröstkörteln som var närmast den avlägsnade tumören (Figur 1).
Sedvanlig extern strålbehandling efter vävnadsbesparande kirurgisk behandling av bröstcancer har i studier minskat förekomst av lokala återfall från 10,2 till 6,2 procent under en observationsperiod på 10 år [5] och från 26 till 7 procent på 15 år [1]. Med förbättrad teknik leder denna typ av strålbehandling sällan till suboptimala kosmetiska resultat eller skadliga effekter på lungor och hjärta [6]. Risken för lokalt återfall hos patienter som behandlats med kombination av bröstbevarande kirurgi och strålbehandling har visat sig jämförbar med risken när hela bröstet avlägsnats [1].
Intraoperativ strålbehandling vid bröstcancer i tidigt stadium har föreslagits som alternativ till traditionell postoperativ extern strålbehandling. Fördelar med intraoperativ strålbehandling är att strålbehandling kan utföras i direkt anslutning till det kirurgiska ingreppet. Delar av de strålbehandlingsresurser som i dag används för behandling av bröstcancer skulle därmed kunna frigöras. En del patienter kan också komma att slippa upprepade transporter mellan bostad och sjukhus under behandlingen. Det är dock avgörande att intraoperativ strålbehandling leder till motsvarande behandlingsresultat avseende lokalrecidiv och risk för dödlighet. Enbart en tillräckligt stor multicenterstudie (TARGIT-A, targeted intraoperative radiotherapy) [7] har gjorts för att utröna detta. Den inkluderade totalt 3 451 patienter, av vilka 2 298 fick strålbehandling peroperativt (Figur 2). Det är tillgängliga delresultat av denna studie som rapporteras och kommenteras här.
Intraoperativ strålbehandling med Intrabeam
Vid intraoperativ strålbehandling med ett system vid namn Intrabeam (Figur 1) riktas röntgenstrålning under 30 minuter direkt mot tumörnära områden av kvarvarande bröstvävnad efter resektion av tumören [8]. Utrustningen består av en flyttbar strålkälla vars strålar leds ut i omgivande vävnad genom klot i olika storlekar. Dessa väljs för att passa in i hålrummet efter borttagen tumör. Andra studier, med inte fullt jämförbara tekniska lösningar, har också gjorts [9].
TARGIT-A-studien
TARGIT-A har under perioden 2000 till 2012 inkluderat patienter från 33 centrum i 11 länder, totalt 3 451 patienter. Patienterna selekterades (>45 år, duktala karcinom, <3,5 cm) och randomiserades till postoperativ extern strålbehandling eller intraoperativ strålbehandling [7].
De patienter som fick en senare intraoperativ strålbehandling efter den primära operationen när en PAD fanns hade signifikant sämre resultat än de som fick strålbehandling i samband med operation. Vi berör här enbart de patienter (n = 2 298) som ingick i den del av TARGIT-A där strålbehandling gavs i direkt samband med primäroperation (Figur 2). Under behandling med systemet Intrabeam ges 20 Gy direkt till vävnad vid klotets yta. Stråldos vid extern strålbehandling varierade mellan 40 och 56 Gy och gavs vid i genomsnitt 23 fraktioner.
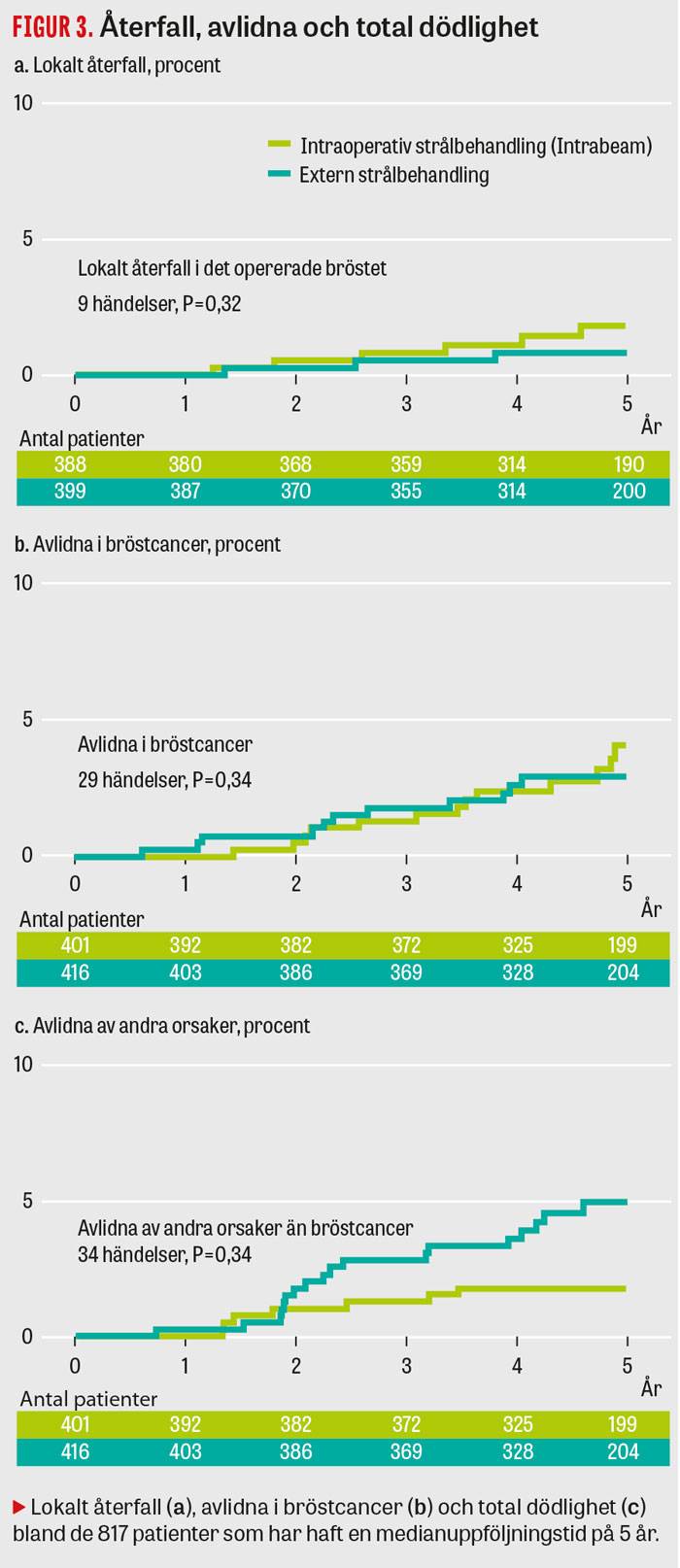
För dessa 2 298 patienter observerades ingen signifikant skillnad i estimerad risk vid 5 års uppföljning, vare sig vad gäller lokalrecidiv (intraoperativ 1,8 procent vs extern strålbehandling 0,8 procent, P = 0,32) eller dödlighet i bröstcancer (intraoperativ 3,9 procent vs extern strålbehandling 3,0 procent, P = 0,34). Dödlighet av andra orsaker än bröstcancer var lägre i den intraoperativa gruppen (intraoperativ 1,9 procent vs extern strålbehandling 5,1 procent, P = 0,04) [7].
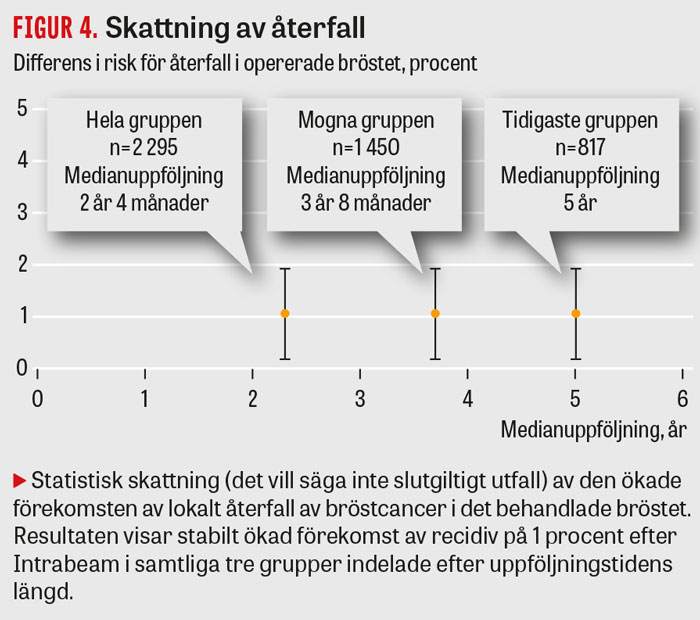
Gruppen med medianuppföljningstid på 5 år (n = 817) (Figur 3 och 4), gruppen med medianuppföljningstid 3 år och 8 månader (n = 1 450) och hela gruppen (n = 2 298) med medianuppföljningstid 2 år och 4 månader hade alla cirka 1 procent ökning i estimerat lokalt återfall i bröstcancer vid TARGIT-A jämfört med extern strålbehandling (Figur 4). Bland de 190 patienter som behandlats med intraoperativ strålbehandling och som följts i 5 år observerades 6 lokala återfall, jämfört med 3 bland de patienter som fått extern strålbehandling (Figur 3). Ingen skillnad sågs mellan grupperna i dödlighet i bröstcancer (Figur 3).
Primärt utfallsmått i TARGIT-A var lokalrecidiv bekräftat med histopatologi. Lokalrecidiv var något vanligare i den intraoperativt behandlade gruppen, men översteg inte gränsen för »non-inferiority« när strålning gavs i samband med operation [10]. Non-inferiority kunde däremot inte påvisas när intraoperativ strålbehandling gavs efter den bröstbevarande operationen. Förekomst av lokalrecidiv var något högre efter intraoperativ strålbehandling än efter extern strålbehandling, men under förutsättning att intraoperativ strålbehandling gavs primärt vid operationstillfället var skillnaden i lokalrecidiv mellan grupperna mindre än de 2,5 procent som utgjorde gräns för non-inferiority. Det framgår tyvärr inte i de publicerade studieresultaten om det fanns skillnader i mortalitet bland patienter med och utan lokalrecidiv.
En non-inferiority-gräns på 2,5 procent valdes i TARGIT-A, vilket har kritiserats eftersom gränsen baserades på en förväntad risk för lokalrecidiv på 6 procent, vilket är betydligt högre än vad senare rapporter visat. De kvinnor som inkluderades hade en betydligt lägre risk (1–2 procent recidiv) än den kohort man beräknade studien på (6 procent recidiv), vilket innebär att TARGIT-A är för liten och därmed otillförlitlig.
Total överlevnad var ett av flera sekundära utfallsmått. I hela gruppen på 2 298 patienter sågs ingen skillnad mellan intraoperativ och extern strålbehandling avseende död i bröstcancer: 1,5 mot 1,3 procent. Däremot var död i andra sjukdomar lägre efter strålning med Intrabeam: 1,1 mot 2,4 procent. Det bör påpekas att man i studien beräknat en statistiskt prognostiserad överlevnad som baseras på en median uppföljningstid på 5 år.
Den sista patienten inkluderades i TARGIT-A i juni 2012. Det innebär att samtliga patienter redan i juni 2017 har haft en uppföljningstid på fem år. Med så många inkluderade patienter i många länder och centrum kommer det sannolikt att dröja innan dessa resultat blir tillgängliga.
Fördelar med intraoperativ strålbehandling
Intraoperativ strålbehandling ger möjlighet att ge hela behandlingen (kirurgi och strålbehandling) i en seans. Strålning kan administreras främst till de vävnader som omgav tumören eftersom den kulformade strålkällan placeras i det hålrum där tumören satt och där risken för återfall är störst. Vidare finns möjlighet att skydda omgivande vävnad där risk för spridning av cancerceller är lägre. Eftersom strålbehandling ges i direkt samband med operation ökar chansen att bli av med cancerceller som vid läkning av operationssåret kan stimuleras i sin tillväxt av de vävnadsfaktorer som ökar efter en vävnadsskada/operation [11].
Nackdelar med intraoperativ strålbehandling
Trots att systemet för intraoperativ strålbehandling (Intrabeam) är en CE-märkt medicinteknisk produkt är behandlingen fortfarande på forskningsstadiet. Medianvärdet för de längsta publicerade uppföljningstiderna är i dag 5 år, och det är känt att omkring 25 procent av lokalrecidiv kommer senare än efter 5 år [12, 13]. En annan nackdel är att behandling ges innan slutgiltigt patologisvar föreligger. Detta innebär att minst 15 procent kommer att behöva kompletterande extern strålbehandling när olika riskfaktorer klarläggs vid patologisk-anatomisk undersökning [7].
Hälsoekonomiska aspekter
Två separat gjorda analyser av kostnadseffektiviteten har genomförts. I den ena analyserades kostnadseffektiviteten för intraoperativ jämfört med extern strålbehandling utifrån de 817 patienter där data finns för fem år [8]. Kostnaderna inkluderar interventioner, följdkostnader och samtliga vårdkostnader under tidsperioden. Primärt effektmått var kvalitetsjusterade levnadsår (QALY). Kostnad per patient beräknades i medeltal till 11 404 pund för intraoperativ och 11 840 pund för extern strålbehandling, en icke-signifikant besparing på 436 brittiska pund. Inte heller avseende QALY fanns signifikanta skillnader, men i snitt visade intraoperativ behandling något högre QALY (3,704 för intraoperativ och 3,663 för extern). Eftersom intraoperativ behandling i medeltal visade lägre kostnader och bättre hälsa (mätt i QALY) bedömdes metoden som kostnadseffektiv. Osäkerheten presenteras med hjälp av beräkningar som visar sannolikheten för att intraoperativ behandling är kostnadseffektiv vid olika värden på QALY. Om exempelvis värdet på QALY sattes till 30 000 pund fanns alltid över 80 procents sannolikhet att intraoperativ behandling uppfattades som kostnadseffektiv.
Den andra analysen av kostnadseffektivitet gjordes utifrån tidigare data från TARGIT-A [10]. Denna beräkning simulerade sedan kostnader och effekter från en tidshorisont som täcker patienternas livstid. I basfallet visade sig metoden då leda till både lägre kostnad och lägre QALY än alternativet med extern strålbehandling. Besparingen bedömdes dock inte som tillräcklig för att motivera den sämre effekten, och intraoperativ behandling ansågs därmed inte kostnadseffektiv.
Båda analyserna visar att användning av intraoperativ behandling leder till något sänkta kostnader, men analyserna skiljer sig åt vad gäller effekten, vilket också gör att analyserna kommer till olika slutsatser avseende kostnadseffektiviteten. För båda analyserna tillkommer också patienternas preferenser för behandlingarna och deras olika fördelar.
Beräkningar från Sydöstra sjukvårdsregionen visar att intraoperativ strålbehandling kan leda till kostnadsbesparingar i storleksordningen 25 000 till 50 000 kronor per patient.
Patienttillfredsställelse
I en HTA-rapport (health technology assessment) från 2015 [10] och en från 2016 [7] finns inga resultat om patientrapporterade mått efter intraoperativ jämfört med sedvanlig extern strålbehandling.
I en substudie till TARGIT-A och vid en 5-årsuppföljning utvärderades bröstrelaterad livskvalitet och kosmetiskt utfall hos 60 kvinnor som fått intraoperativ strålbehandling jämfört med 66 kvinnor som fått extern strålbehandling [14, 15]. Uppföljningarna gjordes efter 3, 6 och 9 månader samt efter 1, 2, 3, 4 och 5 år. Patienterna i den intraoperativa gruppen rapporterade bättre bröstrelaterad livskvalitet efter 6 månader och efter 1 år samt bättre kosmetiskt utfall efter 5 år jämfört med gruppen som fått extern strålbehandling.
Mastektomi är det alternativ som oftast erbjuds i Sverige när en kvinna vill avstå från sedvanlig extern strålbehandling. Intraoperativ behandling skulle då kunna utgöra ett behandlingsalternativ. I Sydöstra sjukvårdsregionen fanns under åren 2008–2011 totalt 531 patienter med bröstcancer (16 procent) som uppfyllde kriterier för intraoperativ strålbehandling. Motsvarande siffror för 2016 var 149 patienter (17 procent). Det kan beräknas att cirka 1 400 svenska patienter skulle uppfylla kriterierna för intraoperativ behandling.
Debatter kring TARGIT-A
TARGIT-A har kommit att debatteras intensivt [16-23], inte minst efter ett relativt positivt första utlåtande från NICE (National Institute of Health and Care Excellence) år 2014 [24]. En rapport med kompletta data från TARGIT-A har gett möjlighet till ökad klarhet på de mest kontroversiella punkterna [8]. Problemen med non-inferiority har understrukits främst på grund av otillräckligt antal patienter som uppnått 5 års uppföljningstid [15]. Kritiken att 5 års uppföljningstid sannolikt är för lite för att upptäcka alla återfall i de typer av bröstcancer som TARGIT-A fokuserat på kvarstår. Dessutom har kompletterande extern strålbehandling getts till cirka 20 procent av de intraoperativt behandlade patienterna som haft ett ofördelaktigt utfall vid histopatologisk undersökning. Detta innebär att de patienter som hade högst risk för lokalrecidiv i den intraoperativa gruppen eliminerats, vilket gynnat de samlade behandlingsresultaten i den gruppen.
Förutom vetenskaplig rapportering har de ansvariga för TARGIT-A uttalat sig i dagspress och i sociala medier (t ex https://www.youtube.com/watch?v=3g199iJxfqA) på mindre nyanserade sätt och med stark betoning på fördelarna med metoden.
Att dödlighet av annan orsak än bröstcancer är större i den externt strålbehandlade än i den intraoperativt behandlade gruppen förbryllar, eftersom effekter av strålning på hjärta och lungor inte brukar visa sig förrän efter 10 år [16]. Det finns därför misstankar om att randomiseringen av patienter i TARGIT-A inte har varit optimal [16].
När TARGIT-A planerades utgick man från en förväntad risk för lokalt återfall på 6 procent. I dagsläget finner man en lokal återfallsrisk på drygt 2 procent. Den gräns på 2,5 procent för non-inferiority som TARGIT-A tillämpar är därför inte relevant i dagsläget. Detta innebär också att antalet patienter som inkluderats i TARGIT-A inte kommer att vara tillräckligt för att besvara frågeställningen.
Utöver vetenskapliga invändningar är det svårt att utesluta påverkan av organisatoriska och resursmässiga argument i debatten [23]. Om metoden skulle införas brett i Sverige skulle ytterligare centralisering av bröstkirurgiska verksamheter krävas.
Intrabeam godkändes preliminärt för bröstcancer i tidigt stadium redan 2014 av NICE i Storbritannien [24], men i sin senaste rapport från 2017 [25] avråder NICE tills vidare från nyinvesteringar i Intrabeam-utrustningar i avvaktan på slutgiltigt ställningstagande.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Arbetet är utfört inom Metodrådet i Sydöstra sjukvårdsregionen.