Vid kronisk myeloisk leukemi har målstyrd, kontinuerlig behandling med tyrosinkinashämmare lett till dramatiskt förbättrad överlevnad.
Efter ett flertal år uppnås djupt molekylärt svar hos ca 50 procent av patienterna; ca 50 procent av dem kan då avbryta behandlingen utan tecken på återfall.
Kontinuerlig behandling med tyrosinkinashämmare kan ge långsiktiga biverkningar.
Efter patentutgång för imatinib (Glivec) erbjuds nu generika till under 5 procent av originalpreparatets pris, vilket ytterligare förbättrat kostnadseffektiviteten.
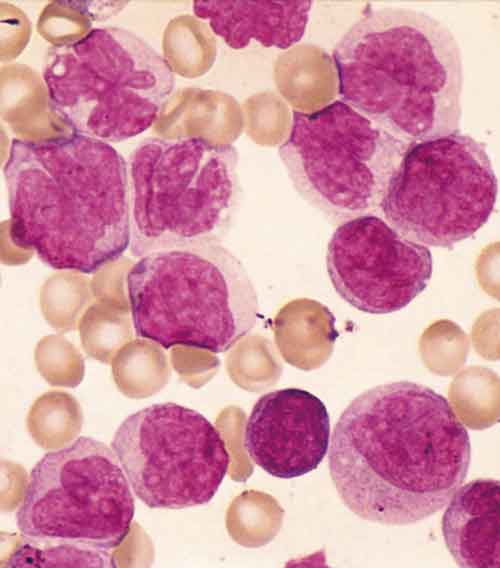
Överlevnaden vid kronisk myeloisk leukemi har förbättrats dramatiskt under 2000-talet tack vare behandling med målsökande tyrosinkinashämmare. När patentet för originalpreparatet nu har gått ut blir behandlingen betydligt billigare. (Bilden visar myeloiska celler hos patient med kronisk myeloisk leukemi efter övergång till sjukdomens blastfas.)
Foto: Secchi-Lecaque/Roussel-Uclaf/CNRI/SPL/IBL
Kronisk myeloisk leukemi (KML)är en malign blodsjukdom som drabbar knappt 100 personer per år i Sverige; medianåldern är 60 år [1]. Kronisk myeloisk leukemi var den första cancersjukdom vid vilken en bakomliggande förvärvad genetisk förändring kunde påvisas i och med upptäckten av Philadelphiakromosomen år 1960.
Denna uppstår som en följd av en reciprok translokation mellan kromosomerna 9 och 22 i benmärgens blodbildande stamceller. Förändringen leder till bildandet av fusionsproteinet Bcr-Abl, ett konstitutivt påslaget tyrosinkinas, som via ökad proliferation och minskad apoptos medför kraftig ökning av myeloiska leukemiceller.
Cellerna är genetiskt instabila och kan förvärva ytterligare genetiska aberrationer. Hos obehandlade patienter leder detta inom några år till övergång från sjukdomens kroniska fas till dess omogna och svårbehandlade blastfas, ett tillstånd liknande akut leukemi.
Fram till millennieskiftet var medianöverlevnaden för patienter med kronisk myeloisk leukemi endast 4 till 5 år. Den enda botande behandlingen var allogen stamcellstransplantation, men på grund av brist på passande donatorer och komplikationsrisker var den terapin förbehållen en minoritet av patienterna.
Tyrosinkinashämmare lanseras
Upptäckten av fusionsproteinet Bcr-Abl ledde under 1990-talet till en jakt på målsökande, tyrosinkinasinhiberande (TKI) behandling för att specifikt hämma proteinets aktivitet. Framtagandet av Bcr-Abl-hämmaren STI571, senare kallad imatinib och såld under namnet Glivec, representerar en veritabel milstolpe inom modern cancerterapi. Imatinib blev den första »målstyrda« anticancerbehandling som godkänts för kliniskt bruk.
Preparatet lanserades 2001, först för patienter som sviktade på tidigare standardbehandling med interferon-alfa, men på grund av de goda behandlingsresultaten blev det snabbt första linjens behandling. Andelen patienter som progredierade till blastfas minskade dramatiskt, och överlevnaden förbättrades påtagligt [2].
Den »andra generationens« tyrosinkinashämmare, dvs dasatinib och nilotinib, liksom senare bosutinib, introducerades under de följande åren med något snabbare reduktion av antalet leukemiceller än med standarddos imatinib [3, 4]. Detta kan medföra minskad risk för att sjukdomen tidigt övergår i den mer allvarliga blastfasen. Hittills har dock ingen skillnad i överlevnad kunnat påvisas mellan de olika preparaten.
Det femte godkända preparatet, ponatinib, är främst utvecklat för behandlingsresistent sjukdom (inklusive patienter som utvecklat BCR-ABL-mutationen T315I mot vilken övriga tyrosinkinashämmare är verkningslösa).
För närvarande är imatinib och nilotinib godkända i Sverige av Tandvårds- och läkemedelsförmånsverket (TLV) som första linjens behandling av kronisk myeloisk leukemi i kronisk fas. Övriga tyrosinkinashämmare kan förskrivas vid behandlingssvikt med en eller flera tyrosinkinashämmare.
Långsiktiga biverkningar
Under senare år har långsiktiga biverkningar efter mångårig behandling med tyrosinkinashämmare uppmärksammats allt mer [5]. En rad väldokumenterade, oftast relativt lindriga, biverkningar från huvudsakligen hud, mag–tarmkanal och CNS (främst trötthet) kan ibland reducera patienternas livskvalitet. Mer allvarliga oönskade effekter har varit svårare att knyta till användning av preparaten.
Tack vare långtidsuppföljningar av kliniska multicenterstudier och av unika svenska patientregister (inklusive KML-registret, diagnos- och förskrivningsregister m fl) har dock en ökad risk för hjärt–kärlhändelser, främst tromboembolier, noterats hos patienter som behandlas med tyrosinkinashämmare [6]. Risken är kopplad till patientens övriga kardiovaskulära riskfaktorer samt typ av tyrosinkinashämmare, dos och behandlingslängd. Risken är störst för ponatinib, därefter nilotinib, medan imatinib i stället har föreslagits ha hjärt–kärlskyddande effekter.
Fortsatta uppföljningsprojekt pågår, bl a i samverkan mellan svenska onkokardiologer och hematologer.
Påtagligt förbättrad överlevnad
Efter insatt behandling följs patienterna regelbundet cirka var 3:e–6:e månad med kvantitativ PCR av BCR-ABL1-transkriptet i perifert blod [7]. Denna analys har under det gångna decenniet standardiserats internationellt och utförs på samtliga svenska universitetskliniker. Analysen är mycket känslig; det är möjligt att detektera motsvarande en leukemicell bland ca 30 000–100 000 normala celler. En kritisk gräns, motsvarande 1 leukemicell bland 1 000 celler, har identifierats (major molecular response, MMR). Under denna nivå är risken för övergång till de avancerade formerna av kronisk myeloisk leukemi mycket liten.
Den påtagligt förbättrade överlevnaden för patienter med kronisk myeloisk leukemi har dokumenterats genom bl a flera studier genomförda på basis av det svenska KML-registret och andra populationsbaserade register. Även om övergång till blastfas fortsatt förekommer och resistens och intolerans mot tyrosinkinashämmare utgör problem, närmar sig överlevnaden för en patient med sjukdomen i kronisk fas den hos befolkningen i övrigt [1, 8, 9].
Incidensen av kronisk myeloisk leukemi är fortsatt låg, men den förbättrade överlevnaden har resulterat i stadigt ökad prevalens [10]. I dag lever i Sverige ca 1 300 patienter med sjukdomen, men antalet beräknas öka till nästan det dubbla kring år 2060 [10].
Behandlingsstopp kräver noga övervägande
När imatinib introducerades betraktades behandlingen som livslång, och man förutspådde att sjukdomen snabbt skulle komma tillbaka om medicineringen avslutades. Ett antal mindre studier, i första hand den franska STIM-studien (STIM = stop imatinib), har dock visat att 40–60 procent av patienterna med djupt molekylärt svar på behandling med tyrosinkinashämmare under minst 2 år verkar kunna avsluta behandlingen utan att drabbas av återfall i sjukdomen [11, 12].
Aktuella data från en nyare och större europeisk multicenterstudie (EURO-SKI; Europe stop kinase inhibitors) med ett betydande svenskt engagemang (115 av 821 patienter är från Sverige) pekar i samma riktning [13]. Ungefär hälften av patienter som avslutade behandling med tyrosinkinashämmare efter minst 5–6 års framgångsrik terapi kunde uppvisa fortsatt låga/icke-detekterbara BCR-ABL1-transkriptnivåer i behandlingsfritt skede, för närvarande med ca 3 års medianuppföljningstid. Molekylärt återfall, med behov att ånyo starta behandling med tyrosinkinashämmare, noterades huvudsakligen inom de första 6 månaderna efter stoppad behandling.
Det är dock fortfarande oklart om behandlingen verkligen kan leda till långsiktig »bot«. För denna viktiga frågeställning krävs mer långtidsdata.
Att avsluta behandlingen är också fortfarande en åtgärd som måste göras efter noggrant övervägande och i nära samråd mellan patient och behandlingsansvarig läkare [14], vare sig stoppet sker inom eller utanför ramen för en klinisk studie.
Såväl den europeiska medicinska onkologiorganisationen ESMO som European Leukemia Net uppdaterar nu sina riktlinjer/behandlingsrekommendationer för kronisk myeloisk leukemi. Även det svenska vårdprogrammet för kronisk myeloisk leukemi (i regi av Regionala cancercentrum och Svenska KML-gruppen) förväntas utkomma i ny version i slutet av året. Samtliga dessa dokument lär innehålla en tydlig vägledning om hur avslutande av behandlingen ska handläggas i klinisk rutin.
Med generika blir behandlingen billigare
När imatinib (Glivec) lanserades 2001 var priset för 1 års behandling ca 250 000 kr. Priset har därefter ökat marginellt i Sverige, men i en del andra länder, t ex USA, har det stigit betydligt mer. Under tiden har de fyra övriga ovan nämnda preparaten lanserats, samtliga till en högre årskostnad.
Läkemedelskostnaderna för behandling av kronisk myeloisk leukemi, liksom för andra cancerdiagnoser, har varit föremål för intensiv diskussion de senaste åren [15]. Möjligheten att avsluta behandlingen med tyrosinkinashämmare för en del av patienterna har även inneburit en betydande besparing för sjukvården. För bara det svenska deltagandet i EURO-SKI handlar det om mer än 40 miljoner kronor netto.
I december 2016 gick läkemedelspatentet ut för imatinib (Glivec) i stora delar av Europa, vilket gör att vi nu har tillgång till ett flertal olika generiska imatinibpreparat. Dessa anses enligt flera studier och det europeiska läkemedelsverket vara likvärdiga med Glivec vad gäller såväl effekter som biverkningar. Efter patentutgången har priset på imatinib sjunkit radikalt i Sverige. Drygt 6 månader efter generikaintroduktionen har kostnaden för imatinib gått ner till ca 5 procent av vad originalpreparatet kostar.
Redan tidigare har vi i svenska hälsoekonomiska beräkningar visat att bytet vid millennieskiftet från interferon-alfa (och i viss mån allogentransplantation) till imatinib som förstahandsbehandling vid kronisk myeloisk leukemi var kostnadseffektivt med en inkrementell kostnadseffektkvot (ICER) per kvalitetsjusterat levnadsår (QALY) på ca 50 000 euro [16]. Med den aktuella prisreduktionen på imatinib har denna kostnadseffektivitet blivit ytterligare kraftigt förbättrad.
Som mönster – och hopp
Forskningen kring kronisk myeloisk leukemi har länge legat i framkant vad gäller såväl kunskap kring cancerbiologi med nya läkemedelsprinciper som spektakulära kliniska genombrott för enskilda patienter med dramatiskt förbättrad överlevnad – genombrott som rimligen borde intressera Nobelkommittén.
Fortsatt utveckling mot bot, i kombination med ökad kostnadseffektivitet, pågår nu. Framstegen vid kronisk myeloisk leukemi kan tjäna som mönster och inge hopp även för andra cancersjukdomar.
Potentiella bindningar eller jävsförhållanden: Johan Richter har mottagit arvode från Novartis, Bristol-Myers Squibb, Pfizer och Ariad/Incyte för uppdrag som föreläsare och/eller rådgivare. Båda författarna har varit ansvariga prövare i ett flertal kliniska studier med sponsring från dessa och andra läkemedelsbolag.
























