Gastrisk bypass har utförts sedan 1967.
Operationen verkar genom att påskynda födopassage till distala tunntarmen där maten stimulerar endokrina celler att frisätta mättnadshormoner som ger snabbare mättnad.
Resultaten är 30 procents minskning av ursprungsvikten, samt medicinfrihet hos 2 av 3 patienter med typ 2-diabetes. Hypertoni och hyperlipidemi normaliseras hos hälften av patienterna.
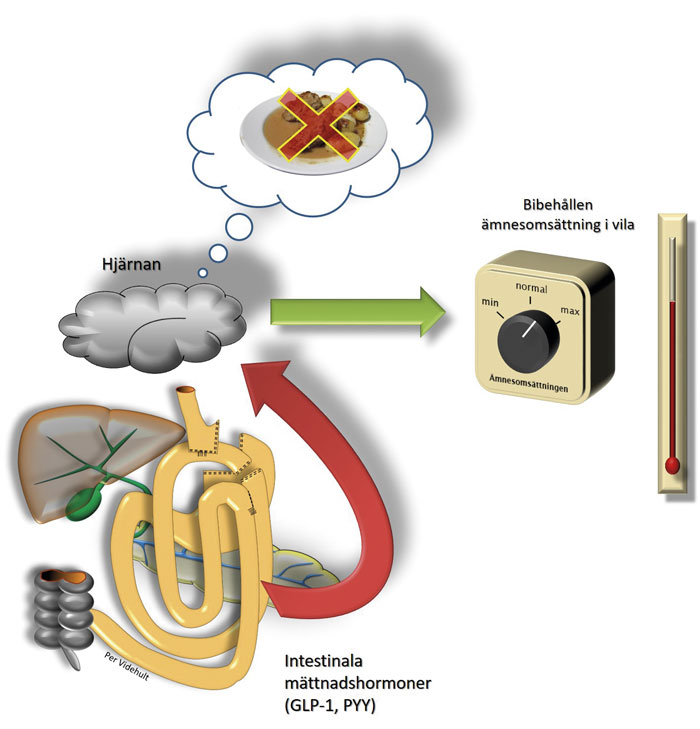
Gastrisk bypass ändrar ätbeteendet men inte genom att försvåra födointaget, utan genom att minska suget. Gastrisk bypass motverkar också den sänkning av ämnesomsättningen som ses vid traditionell bantning. Illustration: Per Videhult
I år är det 50 år sedan den amerikanske kirurgen Edward Mason publicerade sin första artikel om gastrisk bypass för behandling av fetma [1]. Operationen kom att bli den första framgångsrika behandlingen mot fetma, och med tiden har den radikalt förändrat vetenskapens syn på både fetma och diabetes.
Mason fick idén till sin operation efter att ha observerat att personer som opererats för magsår gick ner kraftigt i vikt. Operationen har genom åren modifierats. I dag görs den med titthålsteknik, tar cirka en timme och patienten får vanligen gå hem dagen därpå eller samma dag [2]. Vid ingreppet görs en bypass enligt Roux-en-Y där tunntarmen kopplas till en hönsäggsstor magsäcksficka. För att förhindra gastroesofagal gallreflux till matstrupen, med esofagit som följd, leds gallan om så att den blandas med maten först en bit längre ner i tunntarmen [3]. Viktnedgången ligger på i genomsnitt 30 procent av patientens ursprungliga vikt [2] och med en kvarstående viktnedgång på 27 procent efter 16 år [4].
Positiva metabola effekter
Ett BMI över 40 är förknippat med i genomsnitt 10 år kortare livslängd [5]. Fetmakirurgi förlänger överlevnaden [4], framför allt hos personer med diabetes, där femårsmortaliteten visats sjunka från 5,8 till 1,8 procent efter gastrisk bypass [6]. Av patienter med typ 2-diabetes som opereras kan två tredjedelar sluta med all sin medicinering [2]. Att omkopplingar i mag–tarmkanalen kan åstadkomma en nästan omedelbar normalisering av blodsockret hos patienter med typ 2-diabetes beskrevs första gången redan 1925, också då på en magsårsopererad patient [7]. Det skulle dock dröja ända tills fetmaepidemin tog fart i USA innan fenomenet uppmärksammades på allvar. Effekten är så kraftfull att vissa till och med utvecklar för lågt blodsocker [8]. Gastrisk bypass rekommenderas numera för behandling av typ 2-diabetes vid samtidig fetma [9, 10].
Gastrisk bypass har positiva effekter på de flesta överviktsrelaterade sjukdomar, men återfall förekommer, varför fortsatta kontroller är viktigt. Högt blodtryck och höga blodfetter normaliseras hos hälften av patienterna, och sömnapné och reflux försvinner hos 75 procent [2]. Femårsuppföljning har visat att diabetesförekomsten reduceras från 15,5 procent före operation till 5,9 procent efter fem år, högt blodtryck från 29,7 till 19,5 procent, höga blodfetter från 14,0 till 6,8 procent och sömnapné från 9,6 till 2,6 procent [11].
Mekanismer bakom viktnedgång
Initialt ansågs viktnedgången bero på den lilla magsäcksfickan och förbikopplad tarm. Forskning har dock visat att gastrisk bypass är ett metabolkirurgiskt ingrepp som höjer halterna av mättnadshormon i kroppen [12]. Redan på 1980-talet visades att det gick att få »normala« råttor att äta 30 procent mindre genom att transfundera dem med plasma från råttor som opererats med gastrisk bypass [13].
Viktnedgång och diabetesremission anses framför allt bero på en påskyndad födoämnespassage till slutet av tunntarmen där hormonproducerande L-celler stimuleras att snabbare frisätta mättnadshormoner i kontakt med mat [12]. L-cellerna har normalt funktionen av en måltidsbroms som förhindrar att vi äter mer än vad tarmarna kan ta emot [12]. De mest studerade av dessa mättnadshormoner är glukagonlik peptid (GLP-1) och polypeptid YY (PYY) [12]. Farmakologisk blockering av dessa får både bypass-opererade människor och djur att äta mer, medan tillförsel till icke opererade får dem att äta mindre [12]. De hormonella effekterna av gastrisk bypass kan reverseras om föda tillförs den urkopplade magsäcken via kateter [14]. GLP-1 finns numera tillgängligt som liraglutid och har i randomiserade studier på människa gett en genomsnittlig viktminskning på 7 kilo [15].
GLP-1-stegringen anses vara den viktigaste bidragande faktorn till diabetesremission [16]. Via GLP-1 kommunicerar tunntarmen med pankreas så att insulinproduktion anpassas efter socker- och kolhydratinnehållet i kosten. GLP-1 är, förutom ett mättnadshormon, också ett så kallat inkretin som ökar insulinfrisättning från pankreas [16]. GLP-1 används numera för behandling av typ 2-diabetes.
Gastrisk bypass ändrar ätbeteende hos de opererade, men inte genom att försvåra födointaget, utan genom att minska suget. Även råttor äter mindre och nyttigare efter ingreppet [17]. Gastrisk bypass motverkar också den sänkning av ämnesomsättningen som ses vid traditionell bantning [18-20]. Detta är en trolig förklaring till operationens goda långtidsresultat.
Framtida behandlingsmöjligheter
Att behandla fetma innebär att försöka lura kroppens svältförsvar, något som visat sig vara svårt, såväl medicinskt som kirurgiskt. Att äta hör till våra mest basala behov. Under historiens lopp har perioder av svält fått oss att utveckla så effektiva mekanismer för energiupptag ur tarmen att det sällan går att kirurgiskt åstadkomma normalvikt utan att samtidigt förorsaka svår mineral-, vitamin- och proteinbrist. Kunskapen om hur gastrisk bypass fungerar har lett till en rad nya behandlingsförsök mot fetma.
Endoskopisk duodeno-jejunal stentning. Frånvaron av föda i duodenum efter gastrisk bypass anses ha betydelse för viktnedgång och diabetesremission. I duodenum tros mat stimulera till frisättning av ett ännu icke identifierat antiinkretin som höjer blodsockret. Genom att endoskopiskt placera en flexibel stent i duodenum som hindrar föda från att komma i kontakt med tarmväggen har man i både djurförsök och på människa lyckats åstadkomma viktnedgång och diabetesremission [21, 22]. Svårigheten har varit att få stenten att stanna kvar, och de test som gjorts på människa har hittills förorsakat en mängd komplikationer [21].
Mättnadshormonbehandling.Syntetiska mättnadshormoner har i flera studier testats för fetmabehandling [23]. Mest studerade är GLP-1-analoger eller läkemedel vilka hämmar enzymet dipeptidylpeptidas 4, som inaktiverar kroppseget GLP-1. Viktnedgången ligger i bästa fall kring 10 procent av ursprungsvikten, vilket är mindre än efter gastrisk bypass [23]. Flera tänkbara förklaringar finns: gastrisk bypass höjer inte bara halten av ett mättnadshormon utan flera. Vidare utsöndras kroppsegna mättnadshormoner till portakretsloppet, där halterna är mångdubbelt högre än i systemkretsloppet [16, 24]. Många mättnadshormoner passerar heller inte blod–hjärnbarriären, utan signalerna överförs från portablodet till hjärnan via autonoma nerver, bland annat nervus vagus [16, 23, 25]. Genom att framställa mixturer av analoger till flera av de mättnadshormoner som bidrar till viktnedgång efter gastrisk bypass försöker man nu uppnå bättre viktnedgång [23, 25]. Om detta lyckas kan fetma bli en sjukdom som precis som diabetes är behandlingsbar med hormoner. Sjukdomarna är starkt korrelerade, och frågan är om inte framtiden kommer att utvisa att de i själva verket är två manifestationer av samma sjukdom. Traditionellt har typ 2-diabetes betraktats som en komplikation till fetma, men sambandet kan vara det omvända. Förhöjda halter av kroppseget insulin är vanligt vid fetma, och insulin är ett hormon som driver vikten uppåt.
Vagusblockering. Flera hunger- och mättnadshormoner verkar via nervus vagus. Elektrisk blockering av nerven har på människa i randomiserade studier åstadkommit 9 procents viktnedgång [26].
Sleeve-gastrektomi. Gastrisk bypass är den vanligaste fetmaoperationen i Sverige, men sleeve-gastrektomi ökar snabbt i popularitet och står nu för 33 procent av ingreppen [2]. Globalt sett är sleeve-gastrektomi den vanligaste fetmaoperationen [28]. Resultaten verkar ligga i nivå med vad som ses efter gastrisk bypass, möjligen med något sämre effekt på viktnedgång och diabetes, men med färre korttidskomplikationer [29, 30]. Långtidsresultaten återstår att se. En rad fetmaoperationer har under årens lopp introducerats med stor entusiasm för att sedan snabbt försvinna när långtidsresultaten inte hållit måttet.
Ileal transposition. Genom att kirurgiskt låta den proximala delen av tunntarmen byta plats med den distala försöker man på många håll behandla typ 2-diabetes utan att bryta tarmkontinuiteten. I en studie på 131 patienter med svårinställd diabetes sänktes på ett år fasteblodsockret från 12,4 till 7,3 mmol/l och HbA1c från 76 till 47 mmol/mol [27]. Endast 3 patienter behövde insulin (2 procent), mot 112 (85 procent) före operationen. Randomiserade studier saknas dock. Ingreppet kombineras dessutom ofta med sleeve-gastrektomi vilket gör det svårt att avgöra hur mycket det ingreppet bidrar till effekten.
Framtidens gastriska bypass
Gastrisk bypass är inte en färdigutvecklad operation. Nyligen har man genom att modifiera operationen kraftigt kunnat minska risken för tarmvred [31]. Genom att förlänga den tarmslynga där maten först hamnar (alimentära benet) har försök gjorts att förbättra viktnedgången, dock utan att lyckas [32]. Nya studier tyder dock på att man genom att i stället förlänga den gallförande slyngan (biliära benet), och därmed isolera en större del av övre tunntarmen från födoämneskontakt, kan åstadkomma en bättre viktnedgång och effekt mot diabetes [33].
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Läs även:
Översikt: Nordiska riktlinjer för kosttillskott och uppföljning efter obesitaskirurgi

























