Hydroxietylstärkelse (HES) är en kolloid infusionsvätska som använts mycket inom anestesi- och intensivvård.
Tre kliniska prövningar mellan 2001 och 2012 har övertygande visat att HES ökar risken för njurpåverkan vid sepsis. Evidensen för njurpåverkan vid annan intensivvård är dock svagare.
Europeiska kommissionen förbjöd användning av HES vid sepsis och intensivvård redan 2013 men kan inom kort utvidga förbudet till all användning av HES.
Diskussionen om kolloida vätskors roll för att öka blodvolymen bör nu utökas till att omfatta alla infusionsvätskors biverkningar.
Hydroxietylstärkelse (HES) är en kolloid infusionsvätska som under 25 år använts i stor omfattning inom anestesi- och intensivvård. Ökad risk för njurpåverkan medförde dock att HES år 2013 blev kontraindicerat vid sepsis och intensivvård.
En ny granskning av europeiska läkemedelsverkets säkerhetskommitté (PRAC) har medfört att EU-kommissionen rekommenderats att helt dra in marknadsföringstillståndet för dessa vätskor.
HES gjorde segertåg över världen
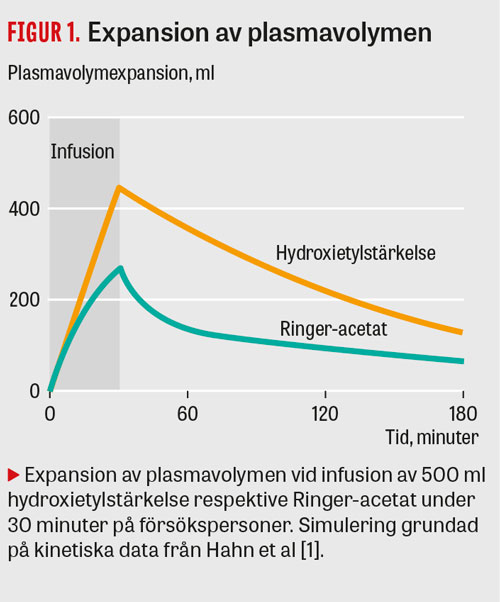
Akut minskning av blodvolymen vid blödning behandlas traditionellt med kristalloid eller kolloid infusionsvätska ända till dess att syretransporten blir så låg att blod behöver transfunderas. Ökningen av blodvolymen blir kraftfullare av kolloida än av kristalloida vätskor (Figur 1), men de är också dyrare och medför en risk för allergiska reaktioner.
Kristalloida vätskor är Ringer-acetat, Plasmalyte och isoton natriumklorid. De kolloida vätskorna är fler, men vi skiljer på fyra typer: gelatin, HES, dextran och albumin. I Sverige bestod volymbehandling med kolloid vätska länge av dextran och albumin. En industriell utveckling av HES under 1980-talet medförde dock att molekylerna kunde göras mindre. Då begränsades risken för allvarliga allergiska reaktioner, och styrbarheten ökade genom att halveringstiden i blodbanan reducerades till ca 2 timmar [1].
Med effektiv marknadsföring av två tyska företag gjorde HES ett segertåg över världen. Även i Sverige trängdes de alternativa kolloida vätskorna bort av preparat såsom Voluven, Volulyte, Venofundin och Tetraspan.
Skandal med fabricerade data
Säkerheten med HES tycktes länge vara mycket god. Det vetenskapliga underlaget för säkerheten kom främst från den tyske läkaren Joachim Boldt, som dessutom var en ofta anlitad och publikfriande föreläsare. Boldts reklamvärde stod på topp när han år 2011 avslöjades med att ha fabricerat data [2]. Plötsligt visste man inte alls vad som var sant.
I skandalens kölvatten fick allt fler upp ögonen för två studier som redan visat att HES jämfört med kristalloid vätska ökar risken för njurpåverkan vid sepsis [3, 4]. En skandinavisk studie bekräftade snart detta fynd och visade dessutom att HES även ökar dödligheten vid svår sepsis [5]. Nästan samtidigt publicerades en ännu större australisk studie som menade att HES påverkar njurarna negativt vid intensivvård för blandade diagnoser med låg förväntad dödlighet [6].
Förbjöds 2013 vid sepsis och intensivvård
Med detta underlag förbjöd EU-kommissionen år 2013 användning av HES vid sepsis, intensivvård och brännskador. HES var fortfarande tillåten för användning vid rutinkirurgi på indikationen blödning. Tre metaanalyser visade inom loppet av 1 år att ökad risk för njurpåverkan och död inte föreligger när vätskan används under rutinkirurgi [7-9]. Underlaget omfattade dock bara några tusen patienter, vilket är i minsta laget eftersom njurskada har en incidens på endast några få procent efter kirurgi.
Nya resultat väntas under 2019
EU-kommissionen har begärt att tillverkarna bättre styrker att HES är säkert när det ges utanför intensivvården. Just därför pågår två industristödda studier på ett 50-tal sjukhus i mellersta och södra Europa. Den ena jämför njurpåverkan (cystatin C-nivåerna) hos drygt 2 000 patienter som får HES eller kristalloid vätska under stor bukkirurgi (PHOENICS-studien). Den andra studien inkluderar 350 traumapatienter (TETHYS-studien). Resultat väntas under 2019.
Skälen som anförs för att dra in marknadföringstillståndet redan nu är dels att förbudet mot HES inom intensivvården inte alltid följts, dels att patienter som genomgår rutinkirurgi kan bli sjuka, varvid redan given HES torde utgöra en risk, och dels att alternativa kolloida infusionsvätskor finns. Några andra data av betydelse har dock inte framkommit sedan 2013. Den nya granskningen, som initierats från Sverige, tycks också ha styrts av eftertanke.
Kontroversiellt att dra in HES
Det är ingen hemlighet att de forskare som genomfört de stora HES-prövningarna blivit tongivande föredragshållare världen över. Som opinionsbildare har man inte alltid nöjt sig med att fördöma HES vid sepsis, utan ifrågasatt både HES generellt och om kolloida infusionsvätskor alls behövs. Även kliniskt verksamma läkare extrapolerar resultaten från sepsis till helt andra situationer.
Trist nog tycks ingen ha satsat på att klargöra mekanismen bakom njurskadan vid sepsis. Ett påstående att HES är giftigt för njuren cirkulerar, trots att sepsis är en metabolt och vätskemässigt mycket speciell situation [10]. I Skandinavien har försäljningen av HES därför minskat med 92 procent under de senaste 5 åren och kolloida vätskor med totalt 56 procent [11].
Frågan om att dra in HES är ingalunda okontroversiell [12]. PRAC:s utredning tillkallade sju internationella experter, som enades om att HES borde få vara kvar på marknaden, men det rådet följdes alltså inte [13]. Rekommendationen om indragning sändes till CMDh, en beslutsgrupp inom europeiska läkemedelsverket. I slutet av januari tillstyrkte CMDh förslaget om förbud, men med minsta möjliga majoritet (15 mot 13). Ärendet skickades därefter vidare till EU-kommissionen för ett bindande beslut.
Efter invändningar från Tjeckien, Frankrike och Spanien beslöt dock EU-kommissionen den 9 april att remittera tillbaka ärendet till PRAC. Man ville få konsekvenserna av ett eventuellt förbud bättre belysta. Det kan t ex finnas situationer i EU:s medlemsländer där medicinska behov inte täcks av alternativ till HES. Kommissionen tänker sig också att ytterligare åtgärder, såsom kanske att minska högsta tillåtna dos, skulle kunna minska risken för njurpåverkan utan att HES helt behöver förbjudas.
Lågmäld kritik mot studier
Kritik mot HES-studierna vid sepsis och intensivvård finns, även om den varit lågmäld. HES har inte givits i akutskedet av sepsis, utan först något dygn senare och då blodvolymen redan korrigerats på annat sätt [14]. HES har därför ökat blodvolymen i onödan, vilket är olämpligt. Gruppen som fick kristalloid infusionsvätska kunde dessutom få HES eller någon annan kolloid vätska i akutskedet, och omvänt.
Studien av intensivvård (den s k CHEST-studien) känns dessutom inte alls övertygande [6]. Varken dödlighet eller njurpåverkan enligt uppställda kriterier talar till nackdel för HES. Njurstödjande behandling, såsom dialys, användes visserligen oftare efter HES, men indikationen styrdes av klinikernas tycke och smak. Det finns även oklarheter i CHEST-studiens redovisning av data, vilket skapat en kontrovers. Författarna har motsatt sig att göra dem offentliga [13].
Det finns också frågetecken kring alternativen. Dextran har exempelvis inte funnits att tillgå i Sverige under de senaste 3 åren, även om detta snart kan ändras. Trots en lång historik vet vi tyvärr väldigt lite om gelatin (Gelofusine, Gelaspan) som infusionsvätska. Albumin är väl beprövat, men kostar mångdubbelt mer än de syntetiska kolloida vätskorna. Tillgången torde också ha sina gränser.
Smalt terapeutiskt fönster för kolloid vätska
Varför inte ge enbart kristalloid infusionsvätska? Många anser att kristalloid vätska bör väljas i alla situationer där det inte är möjligt att statistiskt belägga fördelar med kolloid vätska. Slutsatsen blir då att enbart kristalloid infusionsvätska är aktuell.
Enligt min mening är frågan fel ställd. Kristalloida infusionsvätskor saknar allergiska biverkningar och bör därför alltid väljas för att kompensera en måttligt stor blödning, låt säga upp till 500 ml. Kristalloida vätskor är dock behäftade med biverkningar från ödem i tarmvägg och lungor, vilka gradvis ökar i intensitet när 2–3 liter givits [15]. Efter 3 liter kristalloid vätska medför byte till en kolloid vätska sannolikt att den sammantagna risken för biverkningar minskas.
Utmaningen vore att jämföra de risker som är förknippade med att öka mängden Ringer-acetat från 3 till 6 liter jämfört med att ge 1 liter kolloid vätska. Ser man frågan så kvarstår endast ett smalt terapeutiskt fönster för kolloid infusionsvätska – men det finns fortfarande [16].
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.