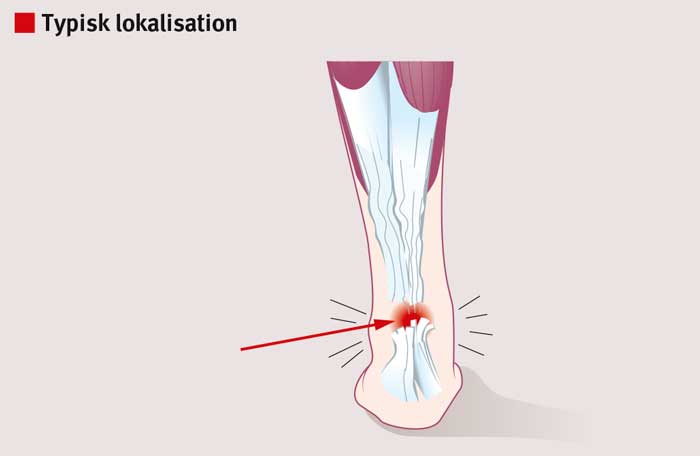
Frekvensen av akillessenerupturer har ökat under de senaste decennierna [1, 2]. Riskgruppen är framför allt män i 40-årsåldern, och skadetillfället är starkt förknippat med någon form av idrottsaktivitet där akillessenan utsätts för hög belastning. Rupturområdet är oftast beläget 3–6 cm proximalt om hälbenet; akillessenan är här som smalast, har mer begränsad vaskularisering och samtidigt större rotation [3].
Orsaken till den ökande incidensen är inte klarlagd men misstänks vara multifaktoriell [4]. En riskfaktor som kan förklara den ökade incidensen är intermittent träning. Ökad belastning ger tillväxtstimulering och därmed ökad draghållfasthet. Efter en tids inaktivitet har senans belastningskapacitet minskat, och ökad risk för ruptur föreligger om aktivitetsnivån inte anpassas [5]. Andra riskfaktorer är ökad pronation i fotleden samt läkemedelsanvändning, t ex fluorokinoloner, vilket kan ge tillväxthämning och celldöd som minskar senans draghållfasthet [6, 7].
Anatomi och patofysiologi
Akillessenans uppgift är att överföra kraften från de stora vadmusklerna gastrocnemius och soleus, även kallad triceps surae, till hälbenet (kalkaneus). Senan har höga funktionella krav och utsätts under gångaktivitet för betydande belastning, vilken ökar vid exempelvis löpning. Hälsenan är uppbyggd av åtskilliga kollagenfibrer som delvis har en fjädrande funktion. I vila antar kollagenfibrerna en vågig struktur, men vid ökande belastning blir strukturerna mer raka. Överstiger sträckningen (förlängningen) 4 procent uppstår en partiell skada och vid 8 procent kan en total ruptur ske [4].
Akillessenan har en rotation på 90 grader mellan muskelinfästningen i underbenet och infästningen till hälbenet. Rotationen och senans elasticitet resulterar i en fjäderfunktion som bl a bidrar till ett mer kostnadseffektivt löpsteg [8]. Akillessenans infästning till hälbenet i kombination med gastrocnemius proximala infästning till femurkondylerna innebär en sträckning vid extension i knäled samt dorsalflexion i fotled. Detta är rörelser som uppkommer såväl aktivt som passivt under idrottsaktivitet och innebär stor belastning av akillessenan. Snabb förändring i en enskild eller i båda lederna är därför potentiella rörelser som kan ge skada på akillessenan.
Gastrocnemius består främst av typ II-fibrer, som vid aktivering producerar snabba rörelser. Muskelkraften är högst då muskeln är maximalt sträckt och ses bl a under starten av en löpsprint [9]. Soleus är en fjäderformad muskel och består i motsats till gastrocnemius av långsamma typ I-fibrer. Muskeln har ett kortare rörelseomfång men större dragkraft. Dess främsta funktion är att hålla kroppen upprätt och förhindra att kroppen faller då tyngdpunkten passerar framför knäleden.
Klinisk presentation
Akillesseneruptur utgör sällan några diagnostiska svårigheter. Genom noggrann anamnes och riktad statusundersökning kan de flesta rupturer diagnostiseras korrekt [10].
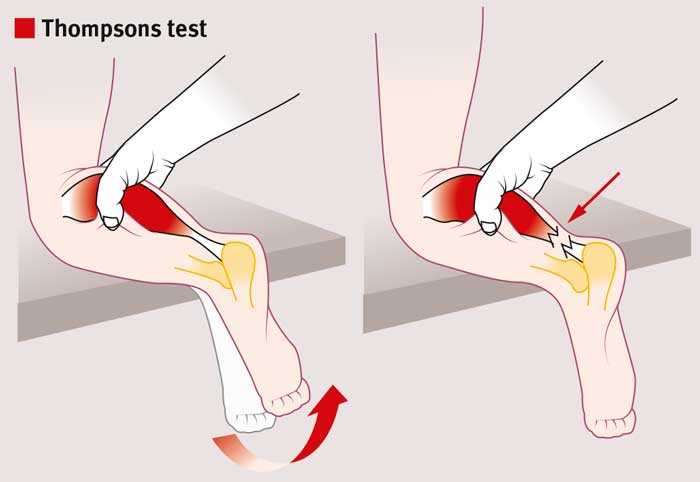
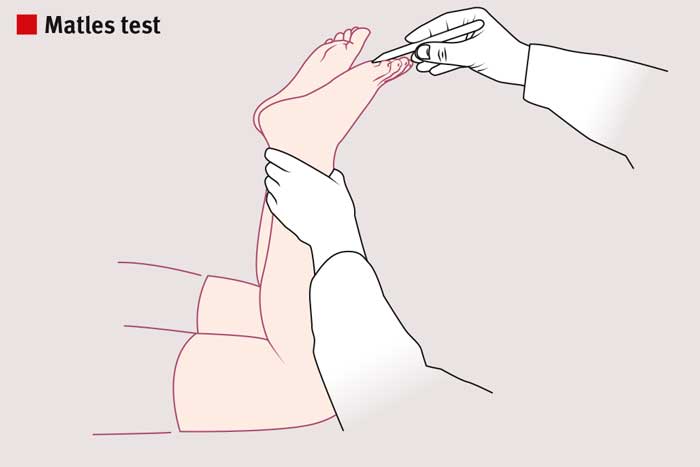
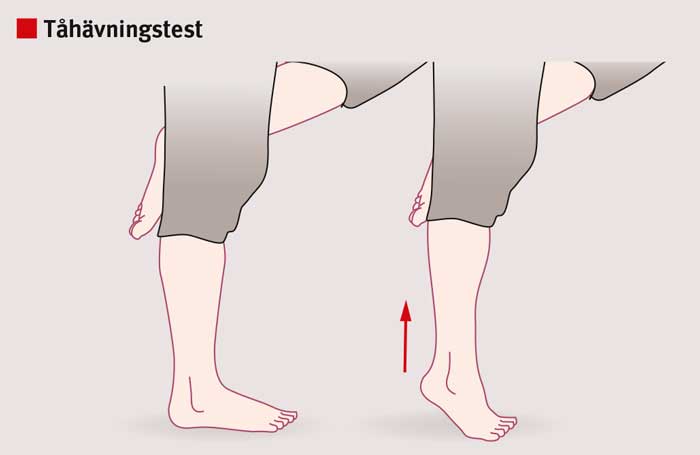
Idrott som innebär hög belastning på senan är vanligt vid skadetillfället. Ibland hör patienten att senan går av och upplever i samband med detta kraftig smärta lokaliserad till området strax ovanför hälbenet. Svullnad och blödning kan bli synlig. Patienten kan inte stå på tå på skadad sida, eftersom vadmuskulaturen är satt ur funktion. Vid undersökningen kan ett gap mellan senändarna palperas. Olika test kan användas för att påvisa skada, däribland Thompsons test (Simmonds test) alternativt Matles test.
Ett observandum föreligger då plantarmuskeln/-senan fortfarande är intakt, vilket kan resultera i falskt negativt test. Man kan i dessa fall be patienten att plantarflektera med motstånd; vid ruptur på akillessenan är plantarflexionskraften upphävd. Detta test är mycket känsligt.
Ytterligare diagnostiska hjälpmedel vid mycket svårbedömda fall utgörs i första hand av ultraljudsundersökning.
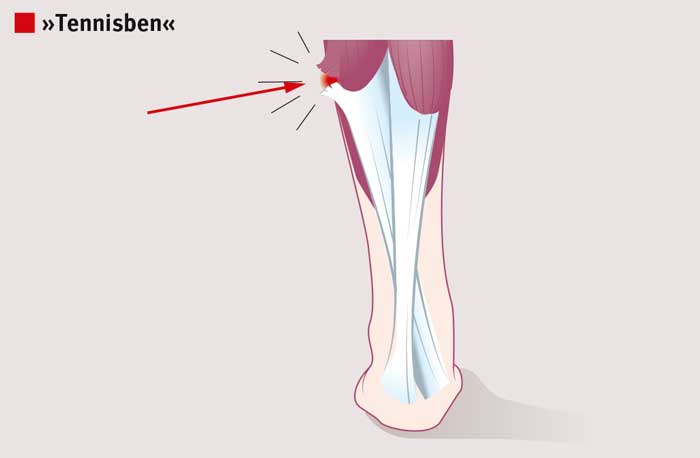
En viktig differentialdiagnos vid akillesseneruptur är bristning av den mediala gastrocnemius-muskelbuken, även kallad tennisben. Skadan har samma åldersincidens och riskspektrum som akillesseneruptur. Smärtan är dock lokaliserad till mellersta delen av vaden, och de kliniska testen, t ex Thompsons test, är negativa.
Behandling
Det finns principiellt två behandlingsmetoder att välja mellan: kirurgisk och icke-kirurgisk. Kirurgisk behandling kan vidare delas in i öppen och minimalinvasiv teknik [11]. Behandlingsrekommendationerna varierar mellan olika sjukhus, men styrs också utifrån patientens fysiska krav och egna önskemål.
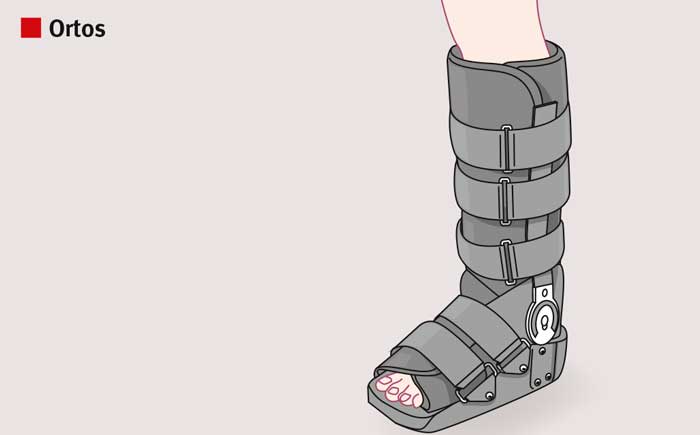
Oberoende av den akuta behandlingen avlastas skadeområdet med gips eller ortos för att minimera belastningen och därmed risken för senförlängning och reruptur. Rehabiliteringsprocessen kan därefter bestå av snabb (accelererad) eller långsammare mobilisering, med eller utan viktbelastning.
Vid icke-kirurgisk behandling erhåller patienten en belastningsbar ortos, till en början med foten i plantarflekterat läge. En vanlig behandlingstid är ca 8 veckor med korrigering av det plantarflekterade läget varannan vecka. Under de första veckorna är fotleden ofta immobiliserad, varefter successivt ökad rörelseaktivitet tillåts i kombination med ökad viktbelastning.
Evidensbaserade slutsatser
Efter granskning och analys av studier som publicerats mellan 1997 och 2012 kan nedanstående slutsatser dras.
Kirurgisk behandling leder till minskad risk för reruptur jämfört med icke-kirurgisk behandling. Skillnad påvisas främst i studier där stora patientgrupper ingår [11-20]. Den totala risken för komplikationer, t ex sårinfektion, är dock ökad vid kirurgisk behandling, framför allt vid öppen teknik [11, 12, 15, 19]. Skillnaden mellan öppen och minimalinvasiv kirurgi är liten; båda teknikerna är förenade med låg frekvens av reruptur [11, 21-26]. I två studier har dock minimalinvasiv teknik visat generellt minskad komplikationsfrekvens [11, 21], men tekniken kan samtidigt öka risken för skada på suralis-nerven [22, 24, 25]. Detta beskrivs dock framför allt i äldre studier avseende minimalinvasiv teknik.
Den funktionella nedsättning som uppstår i samband med olyckstillfället minskar successivt men förekommer fortfarande 2 år efter skadetillfället [27]. Resultaten av de funktionella test som gjorts tyder på att kirurgisk behandling ger tidigare återhämtning av funktionen än icke-kirurgisk behandling. Skillnad förekommer fram till kontroll vid 6 månader och avtar därefter [4, 28].
Någon skillnad mellan öppen och minimalinvasiv kirurgi eller mellan snabb och långsam mobilisering har dock inte kunnat påvisas [23, 28-34]. Det finns studier som visar att belastning, t ex vid gång, kan vara gynnsam för läkningsprocessen, eftersom belastning ger tillväxtstimulering av kollagenet i senan [5]. Resultatmässigt finns dock inga entydiga bevis för att mobiliseringsgraden skulle påverka det slutgiltiga funktionella resultatet. Det är också oklart huruvida tidig mobilisering har betydelse för risken för reruptur, eftersom ingen signifikant skillnad har påvisats i studier [11, 29, 30, 35-38]. Snabb mobilisering kan dock minska den generella frekvensen av komplikationer, däribland adherensbildning och risken för djup ventrombos [11, 28, 29, 35].
Resultaten av kirurgisk eller icke-kirurgisk behandling efter akillesseneruptur är likartade. Vinsten i form av låg risk för reruptur och eventuellt tidigare återhämtning av funktionen vid kirurgisk behandling överväger ofta inte den risk för infektion eller nervskada som kan uppkomma i samband med ingreppet. Däremot bör patienter som har ett yrke eller utövar idrott på en nivå som ställer höga krav på akillessenan opereras för att på så sätt minska risken för reruptur. Möjligen återhämtar de också styrka i vadmuskulaturen tidigare och i högre grad, vilket är av betydelse för att kunna återvända till idrottsaktivitet, speciellt på hög nivå.
Det finns också indikationer om minskad risk för förlängning av senan vid operativ behandling. Att undvika senförlängning har sannolikt stor betydelse för idrottsutövare. En dialog mellan behandlande läkare och patient är därför av stor betydelse för att komma fram till optimal behandling i det enskilda fallet.
Sjukskrivning och återgång till arbete/idrott
Sjukskrivningsperioden kan kortas genom minimalinvasiv kirurgisk behandling jämfört med icke-kirurgisk behandling [16]. Huruvida det även föreligger skillnad mellan öppen kirurgisk och icke-kirurgisk behandling är oklart. Tre studier har jämfört dessa metoder, men ingen uppnådde statistisk signifikans; som mest var skillnaden 54,9 jämfört med 73,4 dagar till fördel för öppen kirurgisk behandling (P = 0,06), och i de övriga två studierna var skillnaden mindre [14, 15, 17]. I fyra av fem studier påvisades dock att snabb mobilisering efter kirurgi ger kortare sjukskrivningsperiod [28, 29, 31, 35, 39].
Det framgår inte med tydlighet av tillgängliga studier varför en så låg andel av patienterna återgått till tidigare aktivitetsnivå efter skadan. Andelen som återgått varierar mellan studierna: lägst andel i en randomiserad studie var endast 54 procent [9], och i de flesta studier var andelen runt 60–65 procent. Den låga andelen av patienter som återgått till tidigare aktivitetsnivå är generell och oberoende av behandlingsmetod och tid för mobilisering.
Tiden tills idrott kan återupptas skiljer sig inte mellan kirurgisk och icke-kirurgisk behandling; däremot kan snabb mobilisering och tidig viktbelastning korta tiden efter öppen kirurgisk behandling [14-17, 21, 28, 29, 31, 32, 36, 37, 39, 40]. Det är troligt att tidig mobilisering skulle ha liknande effekt efter både minimalinvasiv kirurgi och icke-kirurgisk behandling, men ännu finns inga studier som bekräftar detta.
Fler och större randomiserade studier behövs
Kirurgisk behandling minskar frekvensen av reruptur jämfört med icke-kirurgisk behandling. Huruvida tidig mobilisering kan minska frekvensen ytterligare är ännu osäkert. Beträffande övriga komplikationer är risken större vid kirurgisk än vid icke-kirurgisk behandling. Vid minimalinvasiv kirurgisk behandling kan dock komplikationsrisken minska samtidigt som frekvensen av reruptur är låg. Tidig mobilisering kan minska den generella komplikationsfrekvensen vid såväl kirurgisk som icke-kirurgisk behandling samtidigt som sjukskrivningsperiod och tiden tills idrott kan återupptas kortas. Den funktionella styrkan förbättras under uppföljningsperioden men är inte helt återställd 2 år efter skadan oberoende av behandling.
För att fastställa vilken behandlingsmetod som ger bäst resultatet krävs fler och större randomiserade studier, med enighet om vilka resultat som ska kontrolleras, bedömas och värderas. Kostnaderna för de olika behandlingarna behöver beräknas och inkluderas innan en rättvis bedömning kan göras.
På de flesta sjukhus är rekommendationen oftast icke-kirurgisk behandling, som innebär relativt låg risk för reruptur i kombination med elimination av risken för infektion, vilken inte alltid är försumbar vid ett kirurgiskt ingrepp
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Konsensus
De flesta är ense om att
- kirurgisk behandling minskar risken för reruptur men samtidigt innebär en ökad risk för komplikationer generellt, t ex sårinfektion (oftast ytlig)
- skillnaden i resultat mellan öppen och minimalinvasiv kirurgi är liten
- behandlingsmetoden inte påverkar möjligheten att återgå till idrott
- tidig mobilisering kan minska den totala komplikationsrisken utan att öka risken för reruptur
- tidig mobilisering kan minska sjukskrivningstiden och tiden tills idrott kan återupptas
- funktionen efter en akillesseneruptur är nedsatt oavsett behandling och rehabilitering.
Åsikterna går isär om
- huruvida kirurgi eller icke-kirurgi är den optimala behandlingen
- betydelsen av eventuell förlängning av hälsenan
- när rehabiliteringsprocessen ska påbörjas och hur den ska utformas
- huruvida tidig mobilisering kan minska förekomsten av reruptur.