Dosering av läkemedel med betydande utsöndring via njurarna bör anpassas till njurfunktionen (glomerulär filtrationshastighet [GFR]).
Med hjälp av formler kan GFR skattas från plasmakoncentrationen av kreatinin eller cystatin C (estimerad GFR [eGFR]).
Moderna validerade skattningar av GFR är mer noggranna än den tidigare ofta använda Cockcroft–Gaults formel från 1976, vilken också behöver uppgift om patientens vikt.
För läkemedel med dominerande utsöndring via njurarna blir dosreduktionen som regel direkt proportionell mot sänkningen av eGFR.
Sveriges befolkning blir äldre och förskrivs allt fler läkemedel. Njurfunktionen avtar med stigande ålder, vilket medför att riskerna för feldoseringar och läkemedelsbiverkningar ökar. Figur 1 presenterar medelnjurfunktion uttryckt som glomerulär filtrationshastighet (GFR) och förekomst av nedsatt njurfunktion (GFR <60 ml/min/1,73 m2) i olika åldrar. Plasmakoncentrationen av ett läkemedel, vilken som regel motsvarar den terapeutiska koncentrationen, styrs av två faktorer: dos och eliminationshastighet. Risken för förgiftning påverkas i hög grad av det förskrivna läkemedlets terapeutiska fönster. Vissa läkemedel med renal elimination har ett brett terapeutiskt fönster, och toxicitet uppträder först vid mycket höga koncentrationer (t ex bensylpenicillin och oralt penicillin V), medan andra läkemedel (t ex aciklovir) har ett snävt fönster och kan orsaka svåra förgiftningar hos patienter med uttalad njurfunktionsnedsättning [1].
SBU har nyligen utvärderat metoder för skattning av njurfunktion (estimerad GFR [eGFR]) utifrån enkla laboratorie-analyser av kreatinin eller cystatin C i plasma [2]. Under förutsättning att kalibrerade analysmetoder och validerade skattningsformler används, kan eGFR beräknas med tillräckligt god noggrannhet för de flesta patienter. Beräkning av eGFR från kreatinin fordrar till skillnad från cystatin C uppgift om ålder och kön. Noggrannheten ökar om man beräknar medelvärdet av eGFR från kreatinin och cystatin C.
Osäker skattning vid vissa tillstånd
I vissa situationer och tillstånd blir dock eGFR osäker, i synnerhet skattningar från kreatinin hos undernärda och avmagrade patienter, eftersom P-kreatinin påverkas även av muskelmassan förutom av njurfunktionen. Vid låga GFR-värden (<30 ml/min) blir skattningar från kreatinin eller cystatin C mindre säkra, och för personer äldre än 80 år har skattningarna inte utvärderats tillräckligt. När noggrann bestämning av njurfunktionen behövs rekommenderas mätning av GFR med t ex johexol- eller Cr-EDTA-clearance.
De i SBU-rapporten validerade och rekommenderade eGFR-formlerna presenterar relativ GFR (ml/min/1,73 m2), vilket innebär att njurfunktionen normeras till en definierad kroppsstorlek (1,73 m2). Undantaget utgörs av Cockcrofts och Gaults formel från 1976 [3], som också fordrar uppgift om vikt och ger en skattning av den absoluta njurfunktionen (ml/min). SBU:s genomgång visar att skattning av GFR med denna metod är mindre tillförlitlig än skattning med nyare populationsbaserade formler [2].
Underhållsdosen kan beräknas
Det sätt på vilket ett visst läkemedel elimineras via njurarna kan variera. Bindning av läkemedel till plasmaproteiner påverkar i hög grad hur stor del av den i plasma cirkulerade mängden som utsöndras genom glomerulär filtration. Renal elimination kan också ske genom aktiv tubulär sekretion, vilket förkortar halveringstiden jämfört med om endast glomerulär filtration förekommer. Av stor betydelse för den sammantagna totala eliminationen är förstås om läkemedlet metaboliseras eller utsöndras extrarenalt, där nedbrytning via levern är viktigast.
I princip bör man ha kunskap om den absoluta njurfunktionen för att rätt beräkna underhållsdos av läkemedel med renal utsöndring [4], men om man tar hänsyn till patientens storlek kan också ett lätt tillgängligt relativt mått på GFR i de flesta fall användas för att ge en lämplig och anpassad dosering av läkemedel. Absolut GFR kan lätt räknas fram från relativ GFR om kroppsytan uppskattas från uppgifter om längd och vikt, där absolut eGFR = relativ eGFR × patientens kroppsyta (m2)/1,73 m2. I de flesta fall skiljer sig absolut och relativ GFR hos normalviktiga vuxna mindre än 15 procent.
Den totala eliminationshastigheten uttrycks som clearance och utgör summan av renal och extrarenal clearance. Clearance (Cl) brukar anges i ml/min och kan sättas i relation till distributionsvolym (l), kroppsyta (m2) eller vikt (kg). Om distributionsvolymen (VD) är känd, kan halveringstiden (t½) enkelt räknas fram från clearance (eller tvärtom) då t½ = ln(2) × VD/Cl.
Om ett läkemedel har uteslutande renal elimination och filtreras fritt genom glomerulus utan att återresorberas, kommer eliminationen via njurarna av läkemedlet i fråga att vara densamma som GFR, dvs ca 125 ml/min/1,73 m2 hos en njurfrisk ung person. Med en antagen typisk distributionsvolym på 50 l (60–65 procent av kroppsvikten) motsvarar detta en halveringstid på 6,8 timmar. Om GFR är sänkt med 50 procent, blir halveringstiden den dubbla: 13,6 timmar. Om ett läkemedels elimination är direkt proportionell mot GFR, blir halveringstiden för en given dos proportionellt förlängd: t½ patient = t½ normal × normal GFR/patientens GFR.
Anta att en patient har en GFR som är 33 procent av den normala (ca 100 ml/min/1,73m2). Då når man samma medelplasmakoncentration genom att ge läkemedlet med 3 gånger längre dosintervall, exempelvis 1 gång per dygn i stället för 3 gånger, alternativt ges läkemedlet lika ofta men med en tredjedels dos [5].
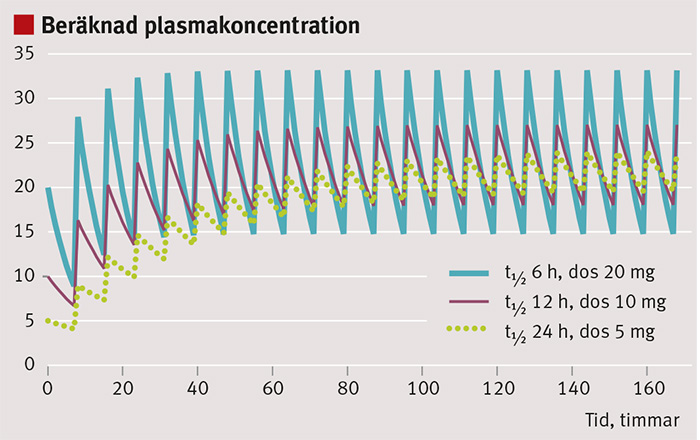
Figur 2 illustrerar plasmakoncentrationen av ett givet läkemedel som elimineras med tre olika halveringstider (6, 12 och 24 timmar) vid administration av en normal dos, halva dosen respektive en fjärdedels dos. Efter en tid nås samma medelkoncentration för alla tre regimerna. Att använda absolut GFR (ml/min) är ingen förutsättning för denna enkla beräkning. Om såväl renal som extrarenal elimination förekommer av ett läkemedel, och om man känner proportionerna mellan dem, kan den samlade halveringstiden också beräknas med stöd av eGFR, men beräkningsformeln är då lite mer komplicerad [6].
Startdos anpassas till uppskattad distributionsvolym
Men hur är det med startdosen? Om man strävar efter att snabbt nå en lämplig terapeutisk koncentration, bör laddningsdosen anpassas till patientens uppskattade distributionsvolym för det aktuella läkemedlet och inte till GFR. Detta kan vara viktigt vid t ex behandling av svåra akuta infektioner då en låg beräknad underhållsdos till följd av en långsam elimination (halveringstid) utan laddningsdos medför att det tar lång tid innan rätt koncentration nås (Figur 2). Genom att anpassa dosen till distributionsvolymen får man matematiskt en anpassning av dosen, som i praktiken korrigerar för att relativ njurfunktion (ml/min/1,73 m2 kroppsyta) används i stället för absolut njurfunktion (eftersom kroppsytan och distributionsvolymen för de flesta läkemedel är nära korrelerade). I praktiken blir således doseringen i stort sett lika men betydligt enklare att beräkna.
Cockcroft–Gaults formel bör utrangeras
Det har funnits en tradition och vana att skatta GFR med Cockcroft–Gaults formel, vilken ursprungligen togs fram för att uppskatta endogent kreatininclearance. Den metodiken överskattar GFR och bör enligt SBU-rapporten utrangeras.
Ett skäl som anförts till att behålla den ursprungliga Cockcroft–Gault-formeln vid läkemedelsdosering är att denna tidigare användes för skattning av GFR och att det är med referens till denna äldre metod som rekommendationerna i produktresuméer och Fass-texter tagits fram. Ett problem är då att de analysmetoder som i dag används för analys av kreatinin avviker från dem som var aktuella 1976 och sannolikt från flertalet av de undersökningar som ligger till grund för text i produktresuméer och Fass.
Ett annat skäl som har framförts till att använda Cockcroft–Gaults formel är att uppgift om absolut GFR (ml/min) erhålls, medan andra skattningar ger relativ GFR (ml/min/1,73 m2). Om absolut eGFR anses behövas för dosering, exempelvis med hänvisning till produktresumé, kan denna enkelt räknas fram enligt ovan. Det mest rimliga torde därför vara att övergå till en så korrekt skattning av GFR som möjligt och att dosera läkemedel efter GFR snarare än att använda en gammal formel som skattar njurfunktionen sämre.
Bäst är att mäta koncentrationen och bedöma effekten
Även om man med kunskap om den normala renala eliminationen av ett läkemedel och patientens eGFR i många fall enkelt kan ta fram ett förslag till lämplig startdos, underhållsdos och doseringsintervall, förekommer stora biologiska variationer mellan individer, vilket medför att ett framräknat doseringsschema som regel blir mer eller mindre felaktigt [7]. Dosering med hjälp av plasmakoncentrationsbestämningar, s k therapeutic drug monitoring (TDM), rekommenderas för aminoglykosider och andra läkemedel där det finns en validerad mätmetod och ett tydligt samband mellan koncentration och effekt eller biverkningar. I många fall är det kliniska effekter och förekomst av eventuella biverkningar som i första hand ska utvärderas, t ex vid behandling av blodtryck, smärtlindring eller antikoagulation.
Läs även:
Följ doseringsanvisningarna när dos ska justeras efter njurfunktion
Replik:
Bättre använda modern formel än att vara formell
Slutreplik:
Låt oss gemensamt arbeta för en förenklad rekommendation



![Figur 1. Medelvärden av glomerulär filtrationshastighet (GFR) och prevalens av nedsatt njurfunktion samt uppgift om medelantalet uttagna receptförskrivna läkemedel i olika åldersklasser i Sverige 2011 (uppgifter från Katarina Baatz, Socialstyrelsens läkemedelsregister). Originaldata avseende GFR och prevalens hämtade och modifierade från Delanaye et al [8] och McCullough et al [9].](https://lakartidningen.se/wp-content/uploads/EditorialFiles/RP/%5bCERP%5d/2012KV1227_1_webb.jpg)