Njurfunktionen bör beaktas vid läkemedelsdosering.
Vi har granskat produktresuméerna för 253 läkemedelssubstanser på Stockholms läns landstings Kloka listan 2010.
Drygt hälften av läkemedlen på listan utsöndras till ≥20 procent via njurarna, och för 61 procent av de granskade substanserna anges att njurfunktionen bör beaktas.
Regelmässigt saknas dock tillräcklig information för att förskrivaren ska förstå på vilket sätt njurfunktionen ska bedömas och hur doseringen ska anpassas till olika grader av njurfunktionsnedsättning.
Doseringsrekommendationerna vid nedsatt njurfunktion behöver därför förtydligas genom att både skattningsmetod och tydliga gränser för dosjustering anges.
Dagens otillräckliga råd och anvisningar riskerar att leda till att patienter med nedsatt njurfunktion får felaktiga doser.
Njurfunktionen bör alltid beaktas vid dosering av läkemedel som utsöndras via njurarna. Detta gäller särskilt hos äldre individer med fysiologiskt nedsatt njurfunktion [1, 2]. Inför läkemedelsförskrivning bör därför njurfunktionen bedömas genom skattning (eGFR) eller mätning av den glomerulära filtrationen, GFR, särskilt om det terapeutiska området är snävt och biverkningsprofilen ogynnsam. Att inte beakta njurfunktionen kan leda till felaktig eller riskfylld läkemedelsbehandling, vilket visats i studier från både Sverige och andra länder [3, 4].
Doseringsrekommendationerna vid nedsatt njurfunktion bör baseras på den GFR-metod som läkemedlet utvecklats med. I praktisk sjukvård bedöms njurfunktionen med olika metoder. Plasmakreatinin ensamt ger ingen god uppfattning om njurfunktionen. En bättre skattning av GFR fås med kreatinin- eller cystatin C-baserade formler [5, 6]. Skattning av eGFR med Cockcroft–Gaults formel ger absolut GFR (ml/min), medan formler som MDRD, CKD-EPI och cystatin C ger kroppsytenormerat eGFR (i ml/min/1,73 m2) [7]. Olika metoder skattar njurfunktionen påtagligt olika hos samma patient, i synnerhet hos patienter med hög ålder [8].
I denna rapport har vi undersökt hur Fasstext och produktresumé anger doseringsrekommendationer för några vanliga läkemedel vid nedsatt njurfunktion.
Metod
Granskade läkemedel
Stockholms läns läkemedelskommittés lista på rekommenderade läkemedel, Kloka listan 2010, granskades. Kloka listan fastställs årligen och innehåller rekommenderade läkemedel med bred användning inom både öppen och sluten vård [9, 10]. Initialt studerades listans samtliga 387 produkter. 17 exkluderades på grund av att de saknade relevans för frågeställningen (t ex saknade systemiskt upptag). Den slutliga granskningen omfattade 370 läkemedel eller 253 substanser [10].
Granskning av Fasstexter och produktresuméer
Fasstexter och produktresuméer granskades under perioden januari–juni 2010 respektive september 2010–mars 2011 enligt en förutbestämd mall. Initialt studerade en biverkningssjuksköterska (MH) Fasstexten och en specialist i klinisk farmakologi (CAH, SR, DR) motsvarande text i produktresumén. En slutgranskning gjordes av biverkningssjuksköterska (LH) och specialist i klinisk farmakologi (DR, CAH). Data från produktresumén ingår i de slutliga analyserna.
Uppgifter om läkemedlets eliminationsväg, normaldosering, doseringsrekommendation vid nedsatt njurfunktion, skrivningar om biverkningar och angivna GFR-mått och mätmetoder noterades. Det noterades om möjlighet till koncentrationsbestämning (TDM) för det aktuella läkemedlet fanns vid Karolinska universitetslaboratoriet. Behov att uppdatera produktresumén avseende dosering vid nedsatt njurfunktion kodades enligt Tabell I.
Klassificeringssystem för renal utsöndring
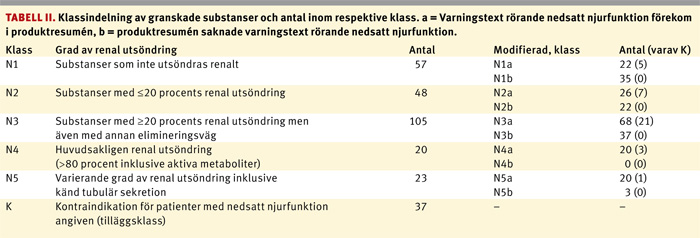
Substanserna klassificerades enligt en femgradig skala (N1–N5) beroende på grad av utsöndring via njuren. Varje klass kunde få tilläggsklass »a« vid förekomst av varningstext rörande nedsatt njurfunktion eller »b« vid avsaknad av sådan. Om substansen även var kontraindicerad vid nedsatt njurfunktion användes »K« som tilläggsklass (Tabell II).
Resultat
Tabell II redovisar hur de 253 granskade substanserna fördelade sig mellan de olika njurutsöndringsklasserna. Fler än hälften av substanserna (58 procent) hade mer än 20 procents renal utsöndring vid systemisk exponering (klass N3–N5), varav 107 substanser i dessa klasser (72 procent) hade en varningstext gällande nedsatt njurfunktion (tilläggskod »a«). Av samtliga granskade substanser fick 61 procent tilläggsklassificeringen »a«. 37 substanser (15 procent) hade kontraindikation vid nedsatt njurfunktion, t ex metformin med känd risk för allvarlig biverkan. Flest kontraindikationer förekom i gruppen N3a (Tabell II). Av de substanser som huvudsakligen utsöndras via njurarna (N4) angavs bara etoposid, karboplatin och mannitol vara kontraindicerade, men samtliga i denna njurutsöndringsklass hade någon typ av varningstext vid nedsatt njurfunktion.
58 (23 procent) av de 253 läkemedelssubstanstexterna innehöll uppgift om GFR-gräns för när dosjustering bör övervägas. I de fall där GFR-gräns fanns angiven i doseringsavsnittet angavs det på följande vis: »kreatininclearance ml/min« (38 substanser), »kreatininclearance ml/min/1,73 m2« (3 substanser), »GFR ml/min« (5 substanser) och »P-kreatinin« (12 substanser). Rekommendationerna för 13 substanser innehöll flera mått samtidigt.
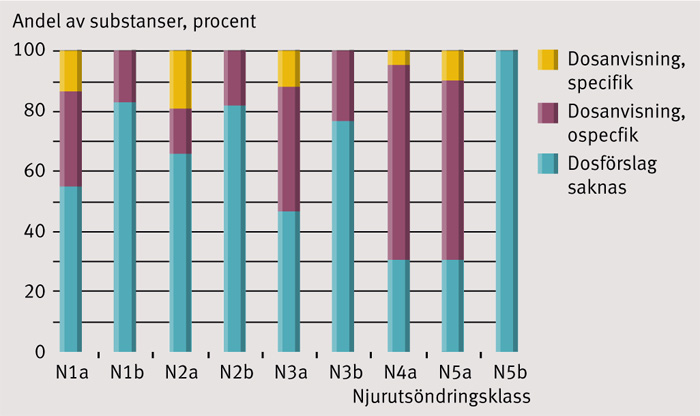
GFR-mätmetoden var tydligt definierad för en enda substans, karboplatin, där GFR uppmätt med 51Cr-EDTA-clearance angavs som grund för dosberäkning. Texterna innehöll information om dosering vid hemo- och/eller peritonealdialys för 27 av de 253 granskade substanserna, flest i klass N5a. Figur 1 presenterar den typ av dosanvisning som förelåg i produktresuméerna i förhållande till graden av renal utsöndring. Det är tydligt att förslag till dosanpassning ofta saknas eller är ospecifika.
Läkemedelsbehandling kan vid behov monitoreras genom koncentrationsbestämning (s k therapeutic drug monitoring, TDM). 43 av de 253 granskade läkemedelssubstanserna kunde koncentrationsbestämmas vid Karolinska universitetslaboratoriet när genomgången gjordes. Andelen substanser som rutinmässigt kan följas med koncentrationsbestämning ökade med stigande renal utsöndringsgrad: 19 procent (N3a), 30 procent (N4a) och 50 procent (N5a). I princip samtliga substanser med hög renal utsöndring (N3a, N4a och N5a) bedömdes ha behov av viss uppdatering av produktresumén avseende dosering vid nedsatt njurfunktion; de viktigaste var att GFR-gränser för dosjustering och metod för mätning eller skattning av GFR inte var tydligt angivna i texter som angav att njurfunktionen behövde beaktas (Tabell I). En annan anledning var oklarheter kring kontraindikationen vid nedsatt njurfunktion (10 substanser).
Generiska substanser granskades inte fullständigt, ändå identifierades ett behov av viss harmonisering för minst 19 substanser.
Diskussion
De 253 substanser vi har granskat här är läkemedel som representerar 14 olika terapiområden med bred klinisk användning i sjukvården. Kloka listans läkemedel stod år 2010 för ca 40 procent av den totala läkemedelskostnaden och för ca 80 procent av den receptförskrivna läkemedelsvolymen (mätt i definierade dagliga dygnsdoser, DDD) i Stockholms läns landsting.
För mer än hälften av läkemedlen angavs att man bör ta hänsyn till njurfunktionen vid dosering. Det kan tyckas motsägelsefullt att många läkemedel som inte var helt beroende av utsöndring via njurarna ändå angavs vara kontraindicerade vid nedsatt njurfunktion. En spekulativ förklaring kan vara att läkemedel med hög njurutsöndring är bättre undersökta vid godkännandet. Läkemedelsmyndigheten behöver då inte lika ofta ange kontraindikation som försiktighetsåtgärd.
Vi har i detalj undersökt texterna i Fass och produktresuméer för ett urval av de vanligaste läkemedlen. Många av dem godkändes för många år sedan då kraven var annorlunda. Vi vet inte om kvalitetsbristerna också omfattar nyligen godkända läkemedel eller äldre potenta läkemedel som förskrivs mindre ofta. Vårt urval är dock ur klinisk synvinkel relevant eftersom användningen är stor.
Behov av förtydligande i produktresuméerna
Den europeiska läkemedelsmyndigheten EMA utarbetar i samarbete med de nationella läkemedelsmyndigheterna riktlinjer för Läkemedelsindustrin att förhålla sig till vid läkemedelsutveckling [11]. Det svenska Läkemedelsverket har alltså möjlighet att påverka riktlinjerna för hur dosering vid nedsatt njurfunktion ska undersökas och dokumenteras. Det är vår uppfattning att den GFR-mätmetod som ligger till grund för doseringsanvisningarna bör anges tillsammans med tydliga GFR-gränser för eventuell dosjustering. Rimligen är det bäst att använda den mest noggranna metod eller skattning av GFR som finns tillgänglig.
SBU har nyligen publicerat en rapport om vilka enkla laboratoriemetoder och formler som mest noggrant skattar njurfunktionen [6, 12]. Denna rapport belyser dock inte metodernas ändamålsenlighet för läkemedelsdosering.
Bristande information om GFR-mätning
Vi fann inte någon dosrekommendation som vilade på cystatin C-baserad eGFR i denna genomgång. Cystatin C-baserad eGFR är relativt nytt, och många läkemedel utvecklades innan metoden fanns tillgänglig. Det är viktigt att komma ihåg att val av eGFR-formel kan styra dosnivå och därmed påverka behandlingsresultat och biverkningar av renalt utsöndrade läkemedel [13-15]. Plasmakreatiningränser, utan skattning av GFR, för dosjustering angavs för tolv substanser. Detta är olämpligt eftersom det är en dålig markör för GFR utan korrigering för ålder, kön och muskelmassa. Olika njurfunktionsmått förekom också tillsammans i samma produktresumé, vilket kan öka risken för missförstånd och feldosering.
Konklusion
Slutsatsen är att många produktresuméer bör bli tydligare avseende doseringsanvisningar för patienter med nedsatt njurfunktion. Detta är angeläget från patientsäkerhetssynpunkt.
Potentiella bindningar eller jävsförhållanden: Charlotte Asker-Hagelberg och Lennart Holm arbetar numera på Läkemedelsverket och Maria Hentschke på Socialstyrelsen. Åsikterna i artikeln är författarnas egna och speglar inte nödvändigtvis respektive myndighets ståndpunkt.