Läkemedelsspecifika kvalitetsindikatorer för äldre har utvecklats av Socialstyrelsen och används till exempel i forskningssammanhang och för uppföljning av sjukvårdens kvalitet. Denna typ av indikatorer är tilltalande eftersom de är lätta att använda på såväl läkemedelslistor som registerdata.
Vår studie redovisar hur väl vanliga läkemedelsspecifika indikatorer korrelerar med en referensstandard för kvaliteten på läkemedelsbehandlingen. För enskilda indikatorer var specificiteten ≥90 procent och sensitiviteten ≤32 procent.
En patient utan utfall på indikatorerna har oftast lämplig behandling, men indikatorerna hittar sammantaget endast hälften av de patienter vars behandling behöver ses över.
Det är välkänt att suboptimal läkemedelsbehandling är vanlig hos äldre. Detta leder till såväl lidande och utebliven nytta för patienten som stora kostnader för samhället, bland annat genom att bidra till sjukhusinläggningar. Därför är det angeläget att förbättra äldres läkemedelsbehandling.
För att beskriva och förbättra läkemedelsanvändningen kan så kallade kvalitetsindikatorer användas. En kvalitetsindikator är ett mätbart mått på förskrivningen där det finns stöd för att måttet kan användas för att beskriva kvalitet [1]. De används ofta i forskningssammanhang. Inom hälso- och sjukvården används de dels som hjälpmedel vid läkemedelsgenomgångar, dels för att följa upp sjukvårdens kvalitet, till exempel i Öppna jämförelser.
Socialstyrelsens kvalitetsindikatorer för läkemedelsbehandling hos äldre introducerades 2004 och reviderades 2010 [2]. Indikatorerna är antingen läkemedelsspecifika eller diagnosspecifika. De förstnämnda är lättast att använda eftersom de endast kräver uppgifter om läkemedelsbehandlingen. De kan alltså lätt användas på läkemedelslistor och registerdata, och detta gör att de kan hitta över- men inte underbehandling. Indikatorer som handlar om dosering kan dock vara svårare att använda på registerdata, eftersom förskriven daglig dos inte registreras systematiskt i Läkemedelsregistret. I vetenskapliga sammanhang och vid uppföljningar/jämförelser i sjukvården är det därför vanligt att fokusera på vissa av de läkemedelsspecifika indikatorerna.
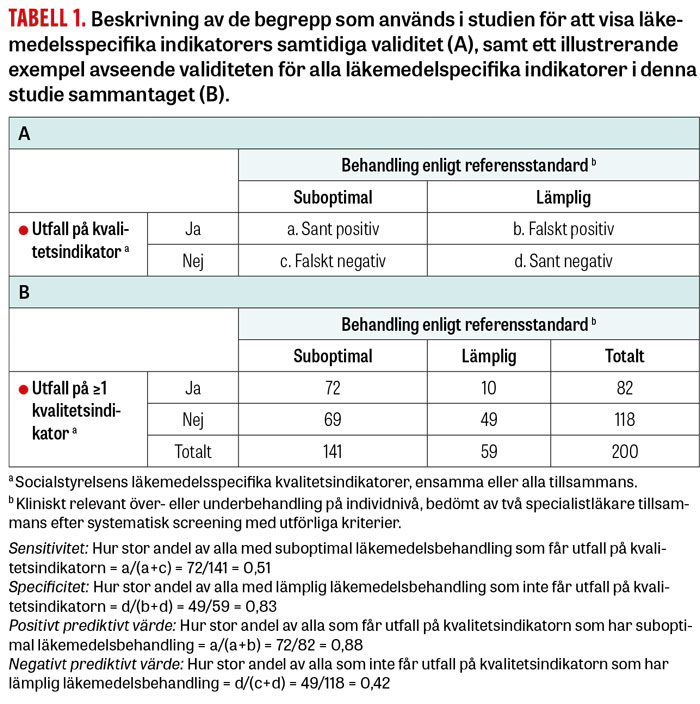
Trots att det finns gott om publicerade studier där man använt sig av Socialstyrelsens indikatorer [2] saknas evidens för de enskilda indikatorernas samtidiga validitet, det vill säga sensitivitet och specificitet samt positivt och negativt prediktivt värde (Tabell 1). Den vetenskapliga litteraturen inskränker sig hittills till två studier som visar hur väl antal läkemedel i läkemedelslistan respektive aggregerade resultat för tre europeiska läkemedelsspecifika indikatorset korrelerar med kvaliteten på läkemedelsbehandlingen [3, 4].
Det finns ingen etablerad referensstandard för att avgöra kvalitet på läkemedelsbehandling. En medicinsk bedömning är dock grunden, eftersom all förskrivning behöver ske utifrån den enskilda patientens hälsotillstånd. Det är angeläget att inkludera både över- och underbehandling i en referensstandard, eftersom båda varianterna bidrar till att patienter inte får den nytta av läkemedel som är önskvärd.
Syftet med denna studie var att undersöka den samtidiga validiteten hos enskilda läkemedelsspecifika kvalitetsindikatorer från Socialstyrelsen.
Metod
Vi har studerat 200 patienter med höftfraktur som rekryterades år 2009 till en randomiserad kontrollerad studie med syftet att utvärdera effekter av läkemedelsgenomgångar [5]. Inklusionskriterier i den ursprungliga studien var patienter, 65 år eller äldre, som opererats för höftfraktur på Sahlgrenska universitetssjukhuset, bodde i Göteborgs närområde och gav informerat samtycke. Totalt 200 av 253 konsekutiva patienter med höftfraktur inkluderades; 14 uppfyllde inte inklusionskriterierna, 10 avled före inklusion, 23 önskade ej delta och 6 inkluderades inte av andra skäl.
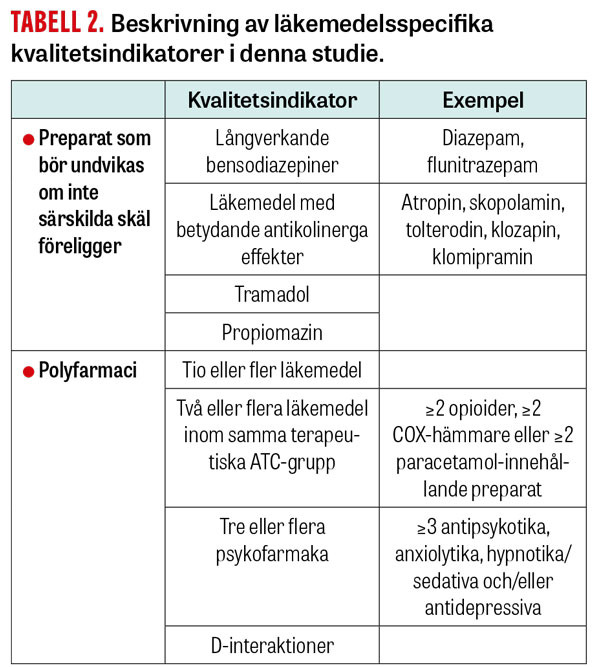
Läkemedelsbehandlingen kartlades i ursprungsstudien, och inkluderade såväl regelbunden som vidbehovsmedicinering. Vi utgick från den läkemedelslista som fanns i journalen och kompletterade vid behov med information från Läkemedelsförteckningen och primärvårdsjournalen. Läkemedel för externt bruk inkluderades endast om de kunde förväntas ha systemeffekter. Behandlingen bedömdes enligt läkemedelsspecifika kvalitetsindikatorer och enligt en referensstandard som använts i tidigare studier [3, 4]. Vi inkluderade dels fyra indikatorer för potentiellt olämpliga läkemedel hos äldre, dels fyra olika indikatorer för polyfarmaci (Tabell 2).
Referensstandardbedömningarna gjordes av en allmänläkare (BB) och en geriatriker (AK) (2012–2013) oberoende av varandra. De diskuterade sedan samtliga bedömningar och nådde konsensus. Bedömningarna gjordes systematiskt i två steg för att identifiera suboptimal läkemedelsbehandling, definierad som över- och/eller underbehandling. Först identifierades potentiell över- och underbehandling med hjälp av de irländska kriterierna STOPP (Screening tool of older persons’ potentially inappropriate prescriptions) och START (Screening tool to alert to right treatment). Dessa omfattar 65 potentiellt olämpliga läkemedel/kombinationer och 22 potentiellt saknade läkemedel [6]. Sedan bedömdes om identifierade utfall på STOPP/START-kriterierna var kliniskt relevanta på individnivå. Om nyttan av ett potentiellt olämpligt läkemedel bedömdes överstiga risken, såsom ett antipsykotiskt läkemedel hos en patient med schizofreni, bedömdes motsvarande STOPP-utfall som inte kliniskt relevant (ej överbehandling). På samma sätt bedömdes en potentiellt saknad behandling som inte kliniskt relevant (ej underbehandling) om det fanns skäl till att patienten inte behandlades med läkemedlet, till exempel att han/hon upplevt problem med biverkningar. Hos patienter utan över- eller underbehandling kategoriserades läkemedelsbehandlingen som lämplig.
Bedömningarna baserades på 1) elektroniska journaler från sjukhuset, 2) primärvårdsjournaler från de två år som föregick höftfrakturen samt 3) tidigare insamlade studiedata inklusive fallriskbedömning, kognition, boende och njurfunktion. Om tillgänglig information inte räckte för att bedöma klinisk relevans av ett STOPP/START-utfall kategoriserades utfallet som inte kliniskt relevant.
Studien godkändes av etikprövningsnämnden i Göteborg (dnr 095-09 med tilläggsansökan 2012).
Analys
Analyser utfördes med SPSS. Mann–Whitneys test och χ2-test användes för jämförelser mellan grupper. Kappa-statistik användes för att bedöma överensstämmelse mellan de två bedömarna avseende STOPP/START-utfall. När det gäller sambandet mellan utfall på kvalitetsindikatorer och referensstandard beräknade vi sensitivitet och specificitet samt positivt och negativt prediktivt värde inklusive 95 procents konfidensintervall (KI). I en känslighetsanalys inkluderades över- men inte underbehandling i referensstandarden. Genom logistisk regression erhölls oddskvoter (95 procents KI) för suboptimal läkemedelsbehandling vid utfall på ≥1 indikator. Vi justerade resultaten för ålder, kön, kognition (nedsatt/demens eller ej), boendeform (särskilt eller eget boende), dosdispensering (som associerats med olämplig läkemedelsbehandling) [7-9] och antal läkemedel (ett surrogatmått på sjuklighet) [10].
Resultat
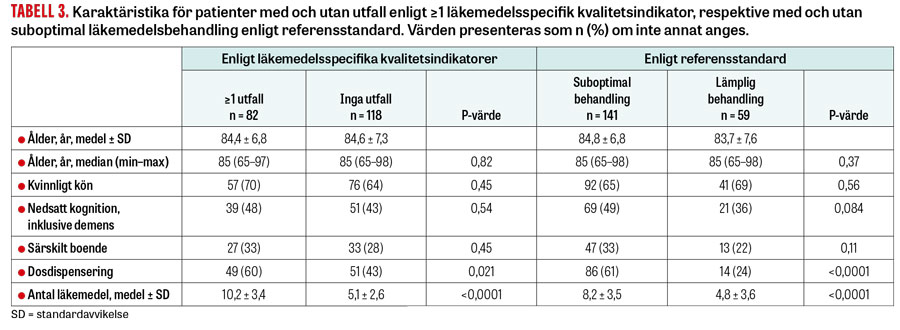
Patienterna var i genomsnitt 84,5 år gamla (65–98 år) och 68 procent var kvinnor. De hade mellan 0 och 21 läkemedel med ett genomsnitt på 7,2. Dosdispensering var vanligare hos patienter med olämplig läkemedelsbehandling enligt såväl läkemedelsspecifika kvalitetsindikatorer som referensstandard (Tabell 3). Dessa patienter behandlades också med fler läkemedel.
Totalt hade 82 patienter (41 procent) utfall på någon av de läkemedelsspecifika kvalitetsindikatorerna, medan 141 (71 procent) hade suboptimal läkemedelsbehandling enligt referensstandard. Kappa-värdet för överensstämmelsen mellan bedömarna var 0,52.
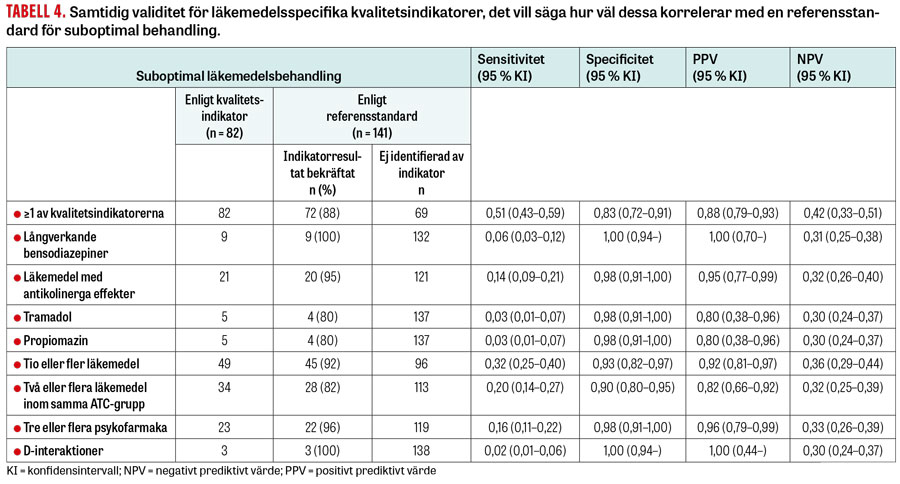
Såväl indikatorer avseende olämpliga läkemedel som indikatorer avseende polyfarmaci hade låg sensitivitet (0,02–0,14 respektive 0,02–0,32; Tabell 4). Specificiteten var generellt hög (0,90 till 1,00). Det negativa prediktiva värdet låg mellan 0,30 och 0,36 och det positiva prediktiva värdet mellan 0,80 och 1,00. När alla indikatorerna användes samtidigt var sensitiviteten 0,51 och specificiteten 0,83. I känslighetsanalysen, där över- men inte underbehandling ingick i referensstandard, förändrades värdena endast marginellt och konfidensintervallen var överlappande (data visas ej).
Vid ojusterad logistisk regression visade det sig att patienter med utfall på minst en indikator 5,1 gånger så ofta hade suboptimal läkemedelsbehandling (95 procents KI: 2,4–10,9). När relevanta faktorer togs med i modellen var motsvarande oddskvot 2,0 (0,8–5,3). När endast över- men inte underbehandling inkluderades i referensstandard för suboptimal behandling var ojusterad och justerad oddskvot 4,2 (2,2–8,0) respektive 1,7 (0,7–3,9).
Totalt sett identifierades 69 patienter (49 procent) med suboptimal läkemedelsbehandling inte av någon av indikatorerna. Den vanligaste sortens överbehandling hos dessa patienter var bensodiazepiner hos patienter med fallrisk (n = 17), acetylsalicylsyra (ASA) i för hög dos (n = 13) eller utan indikation (n = 7) samt loop-diuretika på grund av ankelödem utan andra tecken på hjärtsvikt (n = 12). Den vanligaste underbehandlingen hos patienter som inte identifierades av läkemedelsspecifika indikatorer var hjärt–kärlsjukdom utan behandling med statin (n = 7), ASA/klopidogrel (n = 5) eller betablockare (n = 5), förmaksflimmer utan antikoagulantia (n = 5) respektive osteoporos utan kalcium-/D-vitaminbehandling (n = 6).
Diskussion
Denna studie visar att läkemedelsspecifika kvalitetsindikatorer har god specificitet och högt positivt prediktivt värde. Drygt 8 av 10 patienter med lämplig läkemedelsbehandling hade inte utfall på någon av indikatorerna. Dessutom bekräftades suboptimal läkemedelsbehandling hos nästan 9 av 10 patienter med utfall på någon av indikatorerna.
Sensitivitet och negativt prediktivt värde var lågt. Totalt sett kunde man endast hitta ungefär hälften av patienterna med suboptimal läkemedelsbehandling om man utgick från samtliga indikatorer i denna studie. Sensitiviteten hos enskilda indikatorer varierade och fångade som högst 1 av 3 patienter med suboptimal läkemedelsbehandling (tio eller fler läkemedel) och som lägst 1 av 50 patienter med sådan behandling (D-interaktioner). Det faktum att ungefär 2 av 3 patienter utan utfall på indikatorerna i själva verket hade suboptimal behandling gör att dessa indikatorer inte lämpar sig för att karaktärisera kvaliteten på patienters läkemedelsbehandling. Det är intressant att notera att resultaten endast påverkades marginellt när över- men inte underbehandling inkluderades i referensstandarden för suboptimal läkemedelsbehandling.
Förutom att studien tillför ny kunskap inom ett fält där kunskap tidigare saknats, är det en styrka att bedömningarna av läkemedelsbehandlingens lämplighet utgick från patientens hälsotillstånd. Vårt val av referensstandard för karaktärisering av läkemedelsbehandlingen har dock både styrkor och begränsningar. En styrka är att två läkare med olika specialistkompetenser i läkemedelsintensiva specialiteter oberoende av varandra bedömde behandlingen på individnivå baserat på relativt omfattande information. Då studien var retrospektiv kunde dock bedömningarna inte baseras på en klinisk undersökning. Ytterligare en begränsning är att STOPP/START-kriterierna som användes som screeningverktyg inte fångar alla sorters suboptimal behandling. Resultatens generaliserbarhet torde vara relativt god eftersom få patienter exkluderades i ursprungsstudien. Höftfraktur är också en vanlig diagnos i Sverige, och suboptimal läkemedelsbehandling förekommer ofta i denna patientgrupp [11]. Patientmaterialet samlades in innan regeringen gjorde en specifik satsning för att minska förskrivningen av olämpliga läkemedel till äldre. Prevalensen av utfall på vissa indikatorer kan därför vara lägre än den som redovisas här.
Vår studie bekräftar att suboptimal läkemedelsbehandling är vanlig hos äldre. Även om resultaten inte var statistiskt signifikanta, var det dubbelt så vanligt med sådan behandling om patienten hade utfall på ≥1 indikator efter att hänsyn tagits till relevanta faktorer. Den stora skillnaden mellan ojusterad och justerad oddskvot tyder på att andra faktorer än läkemedelslistan i sig kan vara viktiga när man vill identifiera patienter med suboptimal läkemedelsbehandling. Ett exempel på en faktor som associerats med suboptimal behandling är dosdispensering [7]. Att det inte räcker med att titta på läkemedelslistan för att avgöra kvaliteten på läkemedelsbehandlingen stöds också av att antalet läkemedel har begränsningar som indikator [3].
Sammanfattningsvis visar vår studie att många patienter med suboptimal läkemedelsbehandling missas om man enbart utgår från läkemedelsspecifika kvalitetsindikatorer. Samtidigt har de patienter som fångas av indikatorerna oftast suboptimal behandling. Resultaten kan bidra till förståelse för att man inte kunnat se effekter av särskilt organiserade läkemedelsgenomgångar på objektiva patientnära utfallsmått [12-14]. Dessa utgår ofta från läkemedelslistan och fångar därmed endast en del av de patienter som har suboptimal behandling. Å andra sidan är resultaten uppmuntrande eftersom läkemedelsspecifika indikatorer är enkla att inkorporera i förskrivarstöd. Våra resultat tyder på att sådan feedback till läkaren vid förskrivning skulle kunna signalera risk för olämplig läkemedelsbehandling.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.