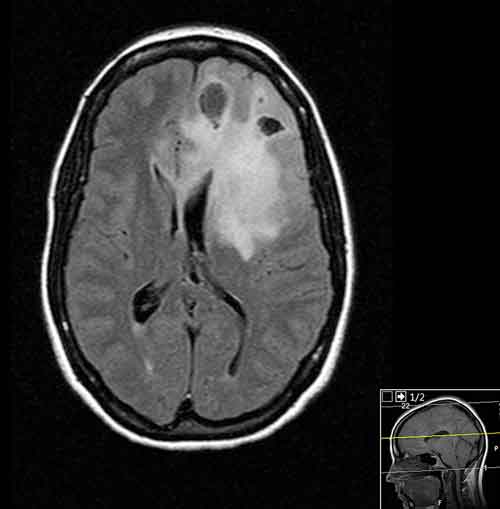
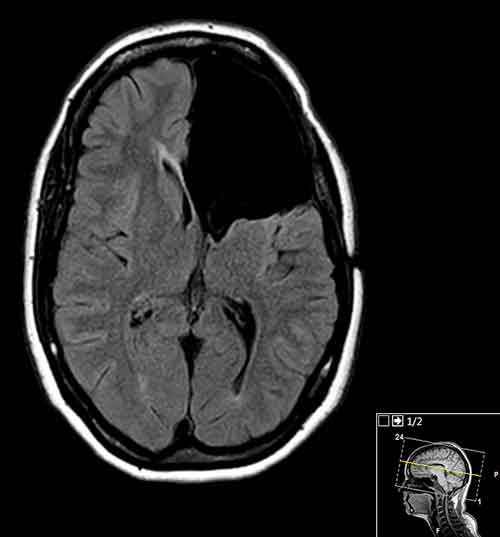
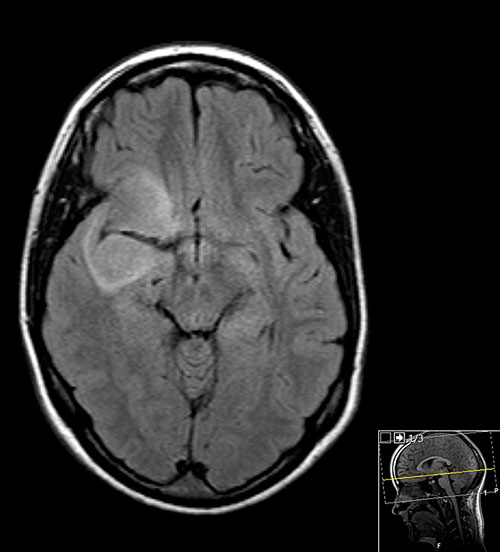
Låggradiga gliom utgör ca 15 procent av alla primära hjärntumörer hos vuxna. De växer ca 4 mm/år och är ofta lokaliserade nära hjärnområden med viktig neurologisk funktion.
Tidig och radikal kirurgisk resektion av låggradiga gliom förlänger patientens överlevnad, minskar risken för omvandling till mer elakartade tumörformer och för tumörrecidiv samt kan bidra till en mer kontrollerad epilepsi och förbättrad kognition.
Vakenkirurgi av hjärntumörer möjliggör maximal resektion med samtidig kontroll av framför allt språk och kognitiva funktioner, som inte kan övervakas om patienten är sövd.
Låggradiga gliom utgör ca 15 procent av alla primära hjärntumörer hos vuxna och inkluderar grad 1- och grad 2-gliom enligt WHO:s tumörklassifikation [1]. Majoriteten av grad 2-gliom består av astrocytom, oligodendrogliom och oligoastrocytom och drabbar särskilt yngre individer (20–60 år). De växer ca 4 mm/år och är ofta lokaliserade i områden med viktig neurologisk funktion såsom motorik och språk. Det vanligaste debutsymtomet är epilepsi och mer sällan neurologiska bortfallssymtom eller huvudvärk [2]. Låggradiga gliom är infiltrerande, obligat långsamt växande tumörer som förr eller senare brukar omvandlas till en mera malign, aggressiv tumörtyp [3].
Inställningen till behandling av låggradiga gliom belägna i anslutning till funktionella hjärnområden var tidigare konservativ, eftersom riskerna för postoperativa neurologiska bortfallsymtom ansågs stora. Det finns i dag inga stora randomiserande kontrollerade studier som visar att resektion av låggradiga gliom förbättrar patientens överlevnad jämfört med biopsi [4].
Flera aktuella retrospektiva studier indikerar emellertid att tidig och radikal kirurgisk resektion av låggradiga gliom förlänger patientens överlevnad [5-11], minskar risken för omvandling till mer elakartade tumörformer och risken för tumörrecidiv [12] samt kan bidra till en mer kontrollerad epilepsi [13, 14] och förbättrad kognition [15]. Ofta blir resektionen inte total då tumörceller finns utanför den makroskopiskt synliga tumören. Målet är därför att ta bort så mycket som möjligt av tumören med bibehållna neurologiska funktioner. Vid fortsatt tumörtillväxt efter primäroperation kan upprepade resektioner göras med flera års intervall [16].
Under de senaste årtiondena har det skett en snabb utveckling av preoperativa utredningsmetoder. Med hjälp av magnetresonanstomografi (MRT), funktionell MR (fMRI) och traktografi, MR-spektroskopi (MRS) och navigerad transkraniell magnetstimulering (nTMS) erhålls detaljerad information om hjärnlesioner och deras närhet till funktionella områden. Framsteg inom neuronavigation och neurofysiologisk monitorering har lett till förbättrad kirurgisk precision.
Hjärnkirurgi på vaken patient är en metod som möjliggör maximal resektion med samtidig kontroll av framför allt språk och kognitiva funktioner, som inte kan övervakas när patienten är sövd. Flera större internationella serier om vaken kirurgi vid hjärntumörer har publicerats [17-20].
Vid neurokirurgiska kliniken i Linköping används sedan 2007 en operationsmetod där patienten är vaken under resektionen av hjärntumör. I realtid kan funktionella test utföras. Metoden bygger på ett nära teamarbete mellan neurokirurg, anestesiolog, neurofysiolog, anestesisjuksköterskor och operationssköterskor.
Vi presenterar de första 7 årens erfarenheter av funktionsbevarande kirurgi i Linköping.
Metod
Totalt 40 vuxna patienter med nyupptäckta radiologiskt misstänkta låggradiga gliom i närheten av känsliga hjärnområden opererades vaket under perioden oktober 2007 till augusti 2014. Låggradiga gliom som inte var belägna bredvid känsliga hjärnstrukturer bedömdes inte aktuella för vakenkirurgi och exkluderades.
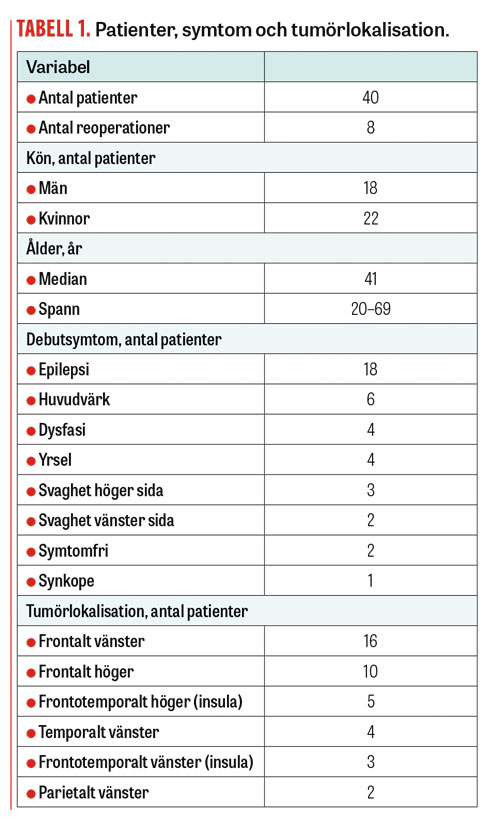
Alla patienter bedömdes preoperativt som medicinskt friska och i skick att genomgå en vakenkirurgisk operation. Relativa kontraindikationer för vakenkirurgi uppfattades vara bl a svår astma, KOL, panikångest, depression, övervikt och icke-svensktalande. Totalt 8 reoperationer genomfördes på 6 patienter på grund av tumörrecidiv eller planerad tvåstegsoperation. Totalt utfördes 48 vakna hjärntumöroperationer (Tabell 1). Alla patienter undersöktes preoperativt med fMRI för språklateralisering, traktografi för identifiering av subkortikala motoriska och språkliga banor och i vissa fall MRS om tumördiagnosen var osäker. Vissa patienter genomgick nTMS för fastställande av kortikala motoriska och språkliga områden.
»Sövd-vaken-sövd«-metoden. De första 13 patienterna opererades med enbart lokalanestesi och intravenös sedering, men eftersom den långa vakenperioden i flera fall ledde till trötthet och smärtgenombrott genomförs numera ingreppen enligt sövd-vaken-sövd-metoden. Patienten är då sövd i början av operationen. Andning och luftväg kontrolleras med larynxmask. Patienten väcks när skallbenet avlägsnats. Sederingen under den vakna perioden baseras på dexomedetomidin, en specifik alfa-2-agonist som ger god anxiolys samtidigt som patienten är kontaktbar utan andningsdeprimerande effekt [21, 22]. När tumörresektionen genomförts sövs patienten åter inför den avslutande delen av operationen.
Fördelen med denna metod är att patienten är vaken och alert under själva tumörresektionen.
Eftersom opioidanalgetika endast kan användas i begränsad omfattning, anläggs standardiserad lednings- och lokalanestesi.
Kontroll av funktioner. Kartläggning av kortikala funktioner görs när patienten är vaken. Med direkt kortikal elektrisk stimulering och sensorisk reaktionspotential (sensory evoked potentials; SEP) detekteras primära motorkortex, sensoriska kortex och centralfåran. Kortikala språkområden lokaliseras med direkt kortikal elektrisk stimulering med stimuleringspenna under tiden som patienten får benämna bilder. Avbruten talfunktion indikerar viktiga språkområden.
Under resektionen monitoreras motoriken via direkt elektrisk kortikal stimulering genom kvarliggande elektrod över motorkortex och registrering av EMG från muskler. Detta kombineras regelbundet med klinisk kontroll av muskelfunktionen. Monitorering av språkfunktion sker genom samtal med patienten, bildbenämning, läsning och räkning.
EEG-monitorering sker med kvarliggande elektrod mot kortex för att upptäcka anfallsaktivitet, framför allt vid kortikal elektrisk stimulering. Subkortikal elektrisk stimulering och registrering av EMG utförs för bedömning av avståndet till subkortikala bansystem.
Hjärnincisionen anpassas till den funktionella kartläggningen. Patienten är vaken under hela resektionen. Den motoriska och verbala testningen sker enligt ett standardiserat protokoll. Vid tecken till motorisk svaghet och/eller dysfasi avbryts resektionen i ca 15 minuter. Om bortfallen då går i regress fortsätter kirurgin. Vid kvarstående bortfall sövs patienten, och operationen avslutas.
Postoperativ MRT-kontroll görs inom 72 timmar om cytologisk granskning indikerat högmalign tumör. För övriga patienter utförs MRT efter 2–3 månader.
Huvudansvarig kirurg (Sverre Boström) deltog vid alla operationer.
Resultat
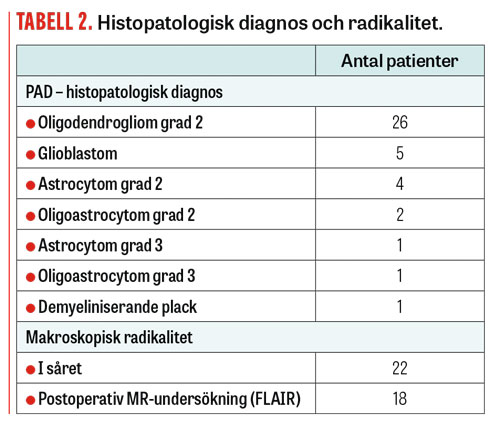
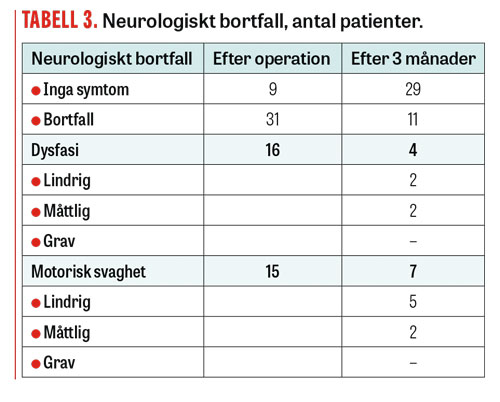
Tumörkarakteristika, PAD, neurologiska symtom och radikalitet redovisas i detalj i Tabell 2 och 3.
Operationsresultat. Vid 3-månaderskontroll hade 4 patienter kvarstående dysfasi, något som samtliga haft även preoperativt. Hos 2 av dessa patienter gick dysfasin sedermera helt i regress. 7 patienter hade kvarstående motorisk svaghet, vilket 5 haft före operationen. Paresen var lindrig hos 5 och måttlig hos 2. Ingen patient hade grav pares eller nytillkommen dysfasi 3 månader efter primäroperationen.
I augusti 2014 hade 6 opererade patienter avlidit. Av dessa hade 4 glioblastom, en oligodendrogliom grad 2, som vid reoperation 6 månader senare hade omvandlats till grad 3, och en oligoastrocytom grad 2. Denna patient var 68 år vid vakenoperationen och avled 7 månader senare på grund av lungemboli.
Peroperativ makroskopisk radikalitet bedömdes ha uppnåtts hos 22 patienter och partiell resektion hos 18. Dessa 18 utvecklade någon form av bortfallssymtom under operationen, varför resektionen avbröts.
MR-kontroll 3 månader postoperativt visade komplett resektion hos 18 och tumörrest hos 22 patienter (Figur 2–4 samt Tabell 1 och 2). Hos 4 av patienterna med tumörrest på MRT (bedömda som radikalt opererade av operatör) var tumörresten liten. PAD visade i alla dessa fall grad 2-tumör, varför någon omedelbar reoperation inte bedömdes vara indicerad. Hos övriga icke-radikalt opererade patienter hade huvuddelen av tumören i de flesta fall avlägsnats och endast mindre rester kvarstod.
Alla patienter kontrollerades postoperativt med MR var 6:e månad för att påvisa eventuellt tumörrecidiv eller malign omvandling.
Vakenkirurgi. Av totalt 48 genomförda operationer genomfördes 21 helt vaket och 27 med narkos enligt sövd-vaken-sövd-metoden.
Sammanlagt 5 patienter drabbades av lambåinfektion med borttagande av benlock, antibiotikabehandling och kranioplastik. Vid 5 operationer fick patienten oplanerat sövas: 2 på grund av motorisk oro, 1 på grund av kramper, 1 på grund av hjärnsvullnad och 1 patient på grund av svår smärta i samband med dissektion av fissura Sylvii och arteria cerebri media.
Totalt 39 patienter kunde tänka sig att opereras vaket igen vid tumörrecidiv; 1 patient som hade blivit konverterad till sövning på grund av oro önskade inte genomgå någon ny vakenkirurgisk operation.
Diskussion
Våra resultat visar att vakenkirurgi är en säker och betydelsefull operationsmetod som tolereras väl av patienterna, vilket ansluter till internationella erfarenheter [23].
Tumörerna var huvudsakligen belägna i vänster hemisfär i nära anslutning till kortikala språk- och motorområden. Internationellt utförs ofta vakenkirurgi vid operation av språknära tumörer, medan motornära tumörer resekeras under sövning med monitorering och neuronavigering [18].
Vi anser emellertid att även dessa patienter bör opereras vaket, eftersom tekniska hjälpmedel enligt vår erfarenhet inte alltid är exakta, bl a beroende på hjärnförskjutning (brain shift) och mätproblem. Regelbunden testning av patientens motoriska funktion i vaket tillstånd bidrar till ökad säkerhet och färre postoperativa pareser än om patienten opereras sövd [24].
Ställer högre krav på snabb handläggning
MR-verifierad radikalitet uppnåddes hos 18 patienter trots den känsliga lokalisationen. Hos 18 av de 22 patienterna med subtotal resektion hade operationen medvetet avbrutits på grund av varierande grad av neurologiska bortfallssymtom. Bevarad funktion prioriterades framför komplett tumörresektion. I samtliga fall kunde majoriteten av tumören avlägsnas.
Resultaten är jämförbara med andra publicerade serier [5]. Av de 7 patienter som histologiskt hade högmalign tumör utvecklade 2 övergående motoriska bortfallssymtom. Vi uppfattar att vakenkirurgi av patienter med högmaligna gliom är genomförbar men ställer högre krav på snabb handläggning [20].
Vedertagen uppfattning om hjärnan har reviderats
Låggradiga gliom ger sällan upphov till neurologiska bortfallssymtom trots omfattande storlek, närhet till känsliga kortikala strukturer och tillväxt längs subkortikala bansystem [25]. Den i regel långsamma tumörtillväxten aktiverar hjärnans plasticitet och leder ofta till omstrukturering av många av hjärnans funktionella områden [26, 27].
Denna nyvunna kunskap har lett till att den tidigare vedertagna anatomiska uppfattningen om hjärnan som ett statiskt organ har reviderats. Många av hjärnans funktionella delar, i synnerhet talfunktionen, utgörs av en mosaik av spridda kortikala områden sammanbundna via ett intrikat subkortikalt nätverk [28].
God kännedom om detta nätverk är nödvändig vid kirurgi av låggradiga gliom. Operation av sövda patienter med navigering baserad på data från MRT, fMRI och traktografi är tidvis oprecis och förenad med lägre resektionsgrad och fler neurologiska bortfallsymtom [29]. Vid vakenkirurgi med intraoperativ monitorering blir patienten sin egen referens. Studier har visat att detta ökar resektionsgraden, reducerar neurologiska symtom och förlänger överlevnaden [30].
Hjärnans inneboende plasticitet kan även ha betydelse för planering av eventuella reoperationer. Angränsande funktionella områden vid primäroperationen kan via rehabilitering sannolikt omorganiseras, vilket ger utrymme för ytterligare kirurgisk resektion [31].
Intraoperativ MRT skulle i framtiden kunna vara ett viktigt hjälpmedel, framför allt i de fall där man uppfattar makroskopisk radikalitet utan neurologiska symtom [32]. Vårt team har nu kompletterats med en psykolog för språklig och mer komplex kognitiv testning före, under och efter operationen.
Konservativ inställning inte längre rimlig
Övertygande litteraturdata indikerar att den tidigare konservativa inställningen till dessa tumörformer inte längre är rimlig. Patienter som insjuknar med låggradiga gliom är oftast unga, neurologiskt intakta och har lång förväntad överlevnad. Våra resultat visar att kontrollerade resektioner med bevarad neurologisk funktion nu är fullt möjliga och bör rekommenderas.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Läs även författarintervjun med Peter Milos.