Nya cancerläkemedel ger nya behandlingsmöjligheter för tumörsjukdomar. I många fall sker dock godkännande innan en optimal dokumentation erhållits.
God behandlingseffekt ses oftast hos en subpopulation, men prediktiva markörer saknas. Nyttan för den enskilda patienten kan därför inte förutsägas.
Kostnader för nya behandlingar är höga, och möjligheterna att beräkna vad som är rimlig kostnad för en enskild patient och för samhället (det hälsoekonomiska värdet) är bristfälliga.
Ett av professionen initierat läkemedelsregister visar på möjligheten att erhålla en bra bild av nya läkemedels användning i rutinverksamheten som stöd i arbetet för vårdgivare, myndigheter, industri och inte minst för patienter.
Vi ser en kontinuerligt förbättrad överlevnad hos dem som drabbas av cancersjukdomar. Förbättringen återspeglar effekten av många faktorer, t ex bättre behandlingsalternativ, men även tidig diagnos har bidragit till ökad överlevnad. Med introduktionen av nya cancerläkemedel ser vi nu behandlingsmöjligheter för tumörsjukdomar där det tidigare saknats kliniskt meningsfulla alternativ. För många nya läkemedel är dock behandlingsvinsten begränsad och ibland associerad med nya biverkningar. Därtill är kostnaderna i regel höga, med utmaningar för den värdebaserade prissättning som vi har i landet och risk för prioriteringar som kan begränsa tillgången till läkemedlen.
Diskussionen är livlig om hur man ska se på graden av tilläggsnytta för såväl den enskilda patienten som samhället. Avgörande är att hitta rätt behandling till rätt patient i rätt tid för att undvika att många patienter utsätts för verkningslösa behandlingar med biverkningar och att resurser kan användas där de gör bäst nytta.
Detta koncept med individualiserad behandling inkluderas i allt fler kliniska studier med målet att hitta specifika prediktiva markörer. Konceptet, som även benämns »precisionsmedicin«, förutsätter i dag att patienternas direkta upplevelser inkluderas [1, 2].
Erfarenheter från en klinik visar potentiellt värde
I dag saknas optimala möjligheter för uppföljning av cancerläkemedel efter marknadsföringsgodkännande. Därför föreligger svårigheter att entydigt bedöma såväl nyttan för patienterna i rutinanvändning som kostnadseffektivitet ur samhällets perspektiv och om behandlingen når alla behövande patienter.
Under 2009 tog därför landets verksamhetschefer i onkologi ett beslut om att skapa ett nytt läkemedelsregister. Målsättningen var att kunna följa upp och analysera värdet av nya läkemedel ur ett brett samhällsperspektiv, men också att skapa bättre underlag för arbetet med introduktionen av nya läkemedel.
Det var dock svårt att erhålla ett tillräckligt nationellt heltäckande engagemang, till stor del beroende på resursbrist på sjukhusen och reellt stöd från ansvariga beslutsfattare, Sveriges Kommuner och landsting och berörda myndigheter.
Därför redovisas nu erfarenheter från enbart en onkologisk klinik. Erfarenheterna visar på det potentiella värdet av ett nationellt register för alla aktörer inom vården.
Arbetet med uppföljning av nya cancerläkemedel är en del av »Cancerplanen« för Stockholms läns landsting och Region Gotland [3].
Registret byggdes upp inom INCA
Till registret har kontinuerligt under åren inkluderats nya läkemedel som fått marknadsföringstillstånd av den europeiska läkemedelsmyndigheten EMA/Läkemedelsverket för användning i Sverige. Registret omfattar i dag olika parametrar som på ett mångfasetterat sätt belyser användningen i den kliniska verksamheten (Fakta 1). Parametrarna har tagits fram efter ett brett samarbete som inkluderat vården och akademiska företrädare, där även myndigheter, industrin och patienter har getts möjlighet att lämna synpunkter.
Läkemedelsregistret byggdes upp inom den nationella s k INCA (informationsnätverk för cancervården)-plattformen, först under ledning av Onkologiskt centrum Umeå och senare med stöd av Regionalt cancercentrum (RCC) Stockholm–Gotland.
De deltagande klinikerna skulle själva ansvara för sin egen rapportering till registret, och varje klinik på universitetssjukhusen skulle ta ett regionalt ansvar. Ett stort värde sågs i att kunna följa användningen av de alltmer kostsamma läkemedel som introducerades, inte minst de läkemedel som administreras på sjukhus med ytterst begränsad uppföljningsmöjlighet.
Anslutningen och rapporteringen till registret har varierat stort över landet. Resurser specifika till projektet har tillhandahållits av Regionalt cancercentrum Stockholm–Gotland och berörda kliniker. Varje klinik äger sina egna data att användas i förbättringsarbete enligt gällande förordningar.
Projektet med extern redovisning av avidentifierade data är godkänt av regionala etikprövningsnämnden i Stockholm avseende regionens data.
Resultat
Resultaten som redovisas från registret bygger på regionala data som inrapporterats mellan 1 januari 2010 och 1 februari 2017. Totalt har 1 766 nya behandlingar registrerats på 1 304 unika patienter varav
- 708 behandlingar vid prostatacancer (41 procent av alla registreringar)
- 310 behandlingar vid bröstcancer (18 procent)
- 251 behandlingar vid melanom (14 procent)
- 188 behandlingar vid kolorektal cancer (11 procent)
- 113 behandlingar vid njurcancer (7 procent)
- 53 behandlingar vid lungcancer (3 procent)
- 60 behandlingar vid huvud–halscancer (3 procent).
Antalet avslutade behandlingar är 1 508. De absolut flesta patienter hade vid insättningen av aktuellt läkemedel ett mycket gott (32 procent) eller gott (56 procent) allmäntillstånd enligt WHO:s gradering (Tabell 1).
De absolut flesta registreringarna omfattade patienter med manifest avancerad sjukdom, och för en mindre del (15 procent) var behandlingen adjuvant eller neoadjuvant (behandlingen ges i syfte att minska tumörstorleken före operation eller lokal strålbehandling). Endast 11 procent omfattade pågående kliniska studier.
De mest frekventa registreringarna ses totalt för läkemedlen abirateron (324 registreringar), bevacizumab (255) och enzalutamid (222). Inom tumörgruppen prostatacancer utgjorde abirateron 46 procent, enzalutamid 31 procent och radium-223 12 procent av nya läkemedel. I gruppen behandling för bröstcancer var motsvarande registreringar bevacizumab 38 procent, eribulin 22 procent, pertuzumab 20 procent och trastumuzumab–emtansin 9 procent. För kolorektal cancer utgjorde bevacizumab 55 procent och cetuximab 33 procent av registreringarna.
Hela 1 193 behandlingar genomfördes i kombination med annan terapi: I ca 35 procent av fallen handlade det om kombination med konventionella cytostatika, i 58 procent om kombination med endokrin behandling och i ca 4 procent i kombination med radioterapi.
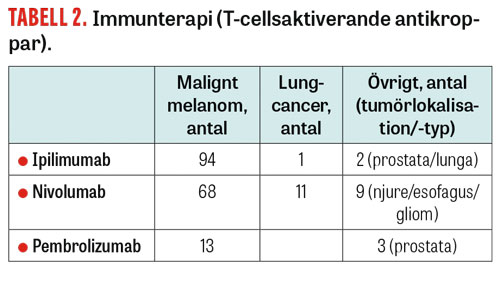
Den nya generationens immunterapi med T-cellsaktiverande antikroppar (immune checkpoint inhibitors) (ipilimumab, nivolumab och pembrolizumab) hade till största delen använts inom förväntade och godkända indikationer, dvs melanom, lungcancer och njurcancer (Tabell 2).
Behandlingsindikationen och intentionen var i de absolut flesta fallen palliativ, 1 601 av registreringarna (92 procent), och kurativ endast i 8 procent av alla registreringar. För 395 registrerade behandlingar angavs att ett test hade utförts för analys av prediktiv markör. Majoriteten startade och avslutade behandlingen med full dos. Dosen var initialt reducerad hos endast 20 patienter. Dosreduktion noterades för framför allt cabazitaxel (4/10), everolimus (2/5) och trabektidin (3/4).
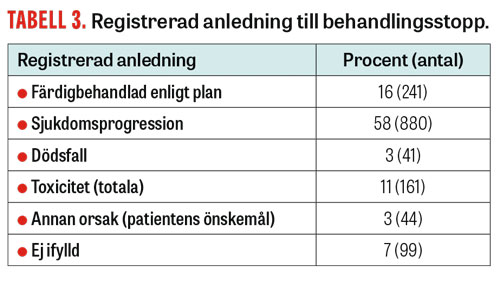
Orsaken till behandlingsavbrott var i 58 procent (880) av behandlingarna progress av sjukdomen, och 16 procent bedömdes som färdigbehandlade (Tabell 3). Behandlingen avbröts på grund av toxicitet i 161 fall (11 procent). I 42 fall (3 procent) önskade patienterna själva avbryta behandlingen, och i 3 procent av fallen rapporterades behandlingsstoppet bero på plötslig död.
Som bästa registrerade effekt noterades komplett remission i <3 procent av fallen, partiell respons i 27 procent och stabil sjukdom i 24 procent av alla registreringar. Progressiv sjukdom utan tecken på något terapisvar noterades i 446 (30 procent) av registreringarna. Orsaken till att effekten inte var evaluerbar kan huvudsakligen hänföras till att behandling pågår eller till att behandlingen med läkemedel givits som ett led i den adjuvanta situationen.
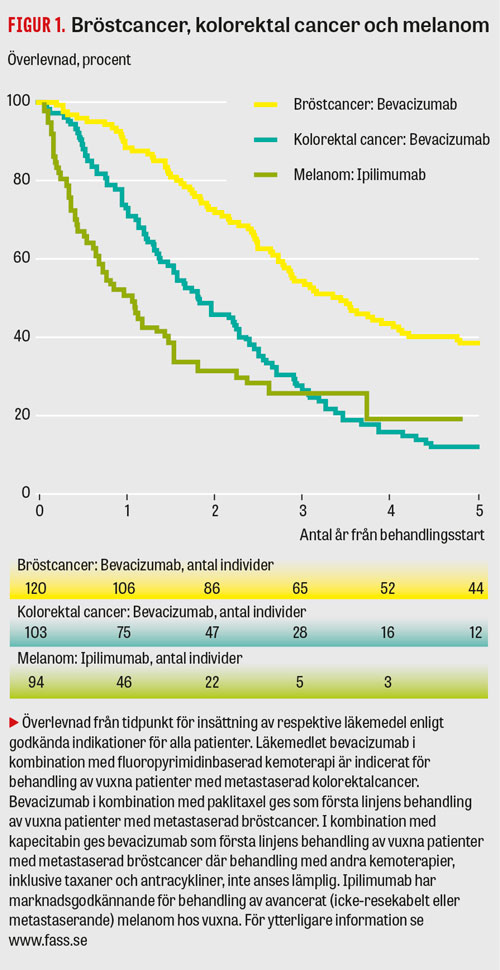
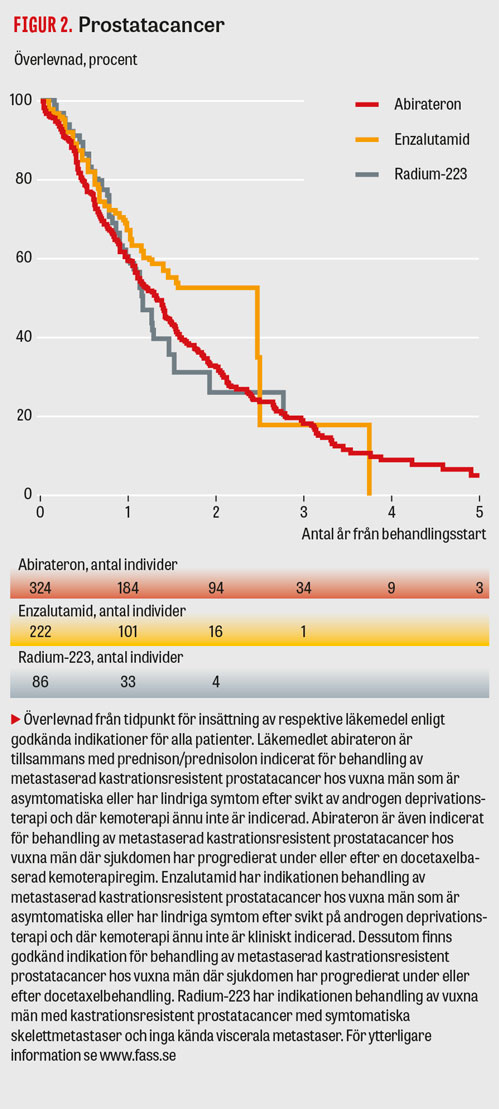
I Figur 1 och 2 redovisas överlevnaden från tiden för insättning av behandling för några av de registrerade läkemedlen. Överlevnadskurvorna visar att dödligheten är stor under det första året, men för ett antal läkemedel ser man en utplaning som talar för att vissa patienter kan bli långtidsöverlevare.
Diskussion
Det beskrivna registret Nya läkemedel inom cancervården är det första som på ett mer systematiskt sätt kan redovisa användningen av nya cancerläkemedel på en klinik. Användningen kan fångas upp på individnivå och är speciellt intressant för rekvisitionsläkemedel där vi i dag enbart har försäljningsstatistik.
I dag finns motsvarande resultat i stort sett endast från sedvanliga kliniska prövningar genomförda på en speciell studiepopulation. Resultaten visar på möjligheter att följa upp de tidigare kliniska prövningarnas resultat på ett helt befolkningsunderlag och därmed erhålla en bild av läkemedlets användning i rutinverksamheten.
Denna kunskap är av vikt för den egna klinikens verksamhet men även för andra läkemedelsansvariga så att alla behövande patienter får tillgång till nya effektiva och säkra läkemedel enligt nationella eller regionala rekommendationer.
Registret kan med fördel användas även för andra terapiområden än cancer.
Pilotprojekt med intressanta aspekter
Projektet får ses som ett angeläget pilotprojekt. Ett antal tillkortakommanden bör beaktas i det framtida nödvändiga arbetet med en optimal nationell uppföljning. Registreringen är begränsad i tiden till en regionklinik med relativt få patienter och återspeglar de läkemedel som var aktuella för registrering enligt inklusionskriterierna från januari 2010 till och med januari 2017.
Inmatningen av uppgifter baseras på ett stort personligt engagemang av enskilda kliniker med stöd av Regionalt cancercentrum Stockholm–Gotland och medlemmar i Stockholms läns läkemedelskommittés expertråd för onkologiska och hematologiska sjukdomar. I Stockholm sker registreringen i dag manuellt. För en framtida optimal registrering är det nödvändigt att skapa en lösning där uppgifterna till registret hämtas automatiskt ur aktuella journalsystem.
Trots ovan nämnda begränsningar föreligger ett flertal intressanta aspekter. Redovisningen omfattar 1 766 nya behandlingar registrerade på 1 304 unika patienter, varav en stor del har avslutat behandlingen. De patienter som inkluderades var till större delen i gott allmäntillstånd. Detta speglar de kliniska prövningarna, som vanligtvis inkluderar patienter i WHO-grad 0–1. I den kliniska verksamheten behandlas dock även patienter inom WHO-grad 2 (sängliggande <50 procent), vilka också fångas upp av registret.
Ökad långtidsöverlevnad för subgrupper
Behandlingsintentionen var enligt indikationerna vid registrering i de absolut flesta fall palliativ, vilket var förväntat. Behandlingsresultaten ter sig relativt sett tämligen modesta i rutinanvändningen för den stora gruppen patienter vad gäller terapisvar mätt som tumörrespons. För läkemedel som ipilimumab och PD-1-hämmare samt läkemedel mot prostatacancer tycks överlevnadsdata spegla det som var grund för marknadsgodkännandet [4-7]. Även om de flesta patienterna har kort överlevnadstid efter insättning av dessa nya läkemedel, ses ökad långtidsöverlevnad för subgrupper av patienter där vi tidigare inte haft något bra behandlingsalternativ.
En alltmer komplicerande faktor vid överlevnadsanalyser är att behandlingen ges i kombination med andra läkemedel; ytterligare behandlingar har i vissa fall satts in i efterföljande nya behandlingslinjer när progressiv sjukdom påvisats. Detta bör adresseras bättre i kommande register.
Av registret framgår att orsaken till behandlingsavbrott huvudsakligen kan hänföras till progressiv tumörsjukdom, liknande det som rapporterats i registreringsstudierna [4-7]. En tämligen stor andel kan relateras till toxicitet. Dessutom ville ett antal patienter på eget initiativ avsluta behandlingen.
Besvärande är att det för närvarande finns relativt få goda prediktiva markörer som kan bistå med att ge rätt patienter behandling. Detta kan till stor del förklara varför så många får behandling enligt registret utan att uppvisa något uppenbart positivt behandlingssvar. Hoppingivande är att vi i dag ser ett större fokus på att utveckla mer individualiserad behandling [1], dvs att endast de patienter som förväntas ha nytta av behandlingen får den och att de med resistenta tumörer inte utsätts för verkningslösa behandlingar med biverkningar. Samtidigt frisätts resurser för andra behov, t ex för andra mer effektiva läkemedel.
Expertråd regional styrgrupp för registret
Kunskapen som erhålls från registret kan ge stöd till kommande introduktioner av nya cancerläkemedel. I Stockholm sker introduktionen på samma sätt som för övriga läkemedel i nära samverkan mellan en rad aktörer. Nya läkemedel introduceras enligt en fastställd införandeprocess som är nationell för vissa läkemedel och regional för andra. Vid båda alternativen fattar Stockholms läns läkemedelskommitté beslut om rekommendation av läkemedlen efter bedömning av vårdprogramgrupper och expertrådet för onkologiska och hematologiska sjukdomar. Därefter har aktuella vårdgivare ansvar för implementering i rutinverksamheten.
I expertrådet ingår bl a läkemedelsansvariga inom de onkologiska och hematologiska klinikerna i regionen, ansvariga från avdelningen för klinisk farmakologi på Karolinska universitetssjukhuset i Stockholm och hälso- och sjukvårdsförvaltningarna samt ett aktivt deltagande från Regionalt cancercentrum Stockholm–Gotland.
Expertrådet utgör sedan en tid regional styrgrupp för registret.
För stöd i arbetet har även en ny cancerdatabas byggts upp inom regionen av Regionalt cancercentrum Stockholm–Gotland. Databasen omfattar uppgifter från såväl interna som externa databaser för att underlätta uppföljning av andra värdefulla parametrar och för bättre stöd till FoU [8].
Samsyn och vilja att delta avgörande
Den trots allt begränsade kunskap som i dag finns vid introduktion av nya cancerläkemedel förutsätter bättre uppföljning i rutinvården med hjälp av heltäckande öppna register. Även om en sedvanlig kontrollgrupp saknas ger registret med »data från verkligheten« en beskrivning av läkemedlets användning i den kliniska vardagen. Inte minst gäller det i en svensk kontext, eftersom det i många kliniska registreringsstudier är ett tämligen begränsat antal patienter som inkluderats från svenska kliniker.
Nyttan kan också vägas mot faktorer såsom en förändrad vårdkonsumtion.
För att registret ska få genomslag och ge praktisk nytta måste det finnas en samsyn och vilja att delta. En avgörande faktor är att tillräckligt med personella resurser kan avsättas för arbetet, eftersom det i dag inte finns optimala tekniska lösningar för automatisk överföring av data från journaler till register. Här finns fortfarande stora möjligheter till förbättringar i samverkansformer mellan alla berörda parter; inte minst gäller det förutom landstingen även Sveriges Kommuner och landsting och myndigheter. Ett flertal utredningar har genomförts, och stora nationella resurser har under åren redan avsatts till denna typ av arbeten [9], men utan att större förbättringar de facto kunnat noteras i den kliniska uppföljningen.
Patientperspektivet av optimal uppföljning för att uppnå rätt och rättvis användning av nya läkemedel i rutinsjukvården är uppenbart.
Konklusion
I dag godkänns allt fler läkemedel innan traditionella välkontrollerade fas 3-studier har genomförts, och i många registreringsstudier saknas deltagande av svenska kliniker. En effektiv, patientsäker och jämlik behandling förutsätter därför att det finns möjlighet till uppföljning.
De generella erfarenheter från en av professionen initierad systematisk uppföljning av nya cancerläkemedel som presenterats här visar på möjligheten att erhålla en bild av läkemedlets användning inom rutinsjukvård. Från registret Nya läkemedel inom cancervården redovisas registreringar från verksamheter inom Stockholm-Gotland.
Liknande register kan med fördel användas inom andra terapiområden än cancer och kan kompletteras med data från nationella och regionala register samt kvalitetsregister inkluderande patientupplevelser.
Kunskapen är av vikt för många aktörer inom vården för att bidra till en effektiv, patientsäker och jämlik behandling enligt gällande riktlinjer.
Potentiella bindningar eller jävsförhållanden: Johan Falkenius är huvudprövare för en fas 1-studie med Merck-Serono. Stefan Norin har medverkat i kliniska prövningar för GlaxoSmithKline, Janssen och Gilead. Roger Henriksson har varit rådgivare för fas 1-studie med bioteknikbolaget Immunicum.
F d överläkare Ann-Marie Billgren har bidragit vid starten av registret. Diana Linden har hjälpt till med inmatning av kliniska data i registret.
Fakta 1. Registret »Nya läkemedel i cancervården«
Följande uppgifter registrerades för varje behandling
- Ansvarig läkare
- Patientidentitet
- Tumördiagnos
- Behandlingsintention
- Behandlingslinje vid palliativ behandling
- Om behandling ingår i en klinisk studie
- Om prediktiv testning utförts och vilken
- Patientens allmäntillstånd (performance status)
- Om behandlingen givits i kombination med annan behandling
- Startdatum
- Stoppdatum
- Administrationssätt
- Bästa registrerade effekt
- Anledning till behandlingsstopp, inklusive toxicitet