Lyckad smärtbehandling bygger på noggrann smärtanalys med anamnes, status och eventuell röntgenundersökning med antagande om möjliga smärtmekanismer.
För framgångsrik smärtbehandling krävs en tydlig behandlingsstrategi baserad på aktuell smärtmekanism och information till patienten. Behandlingen bör utvärderas och eventuellt justeras.
Starka opioider är den viktigaste preparatgruppen vid farmakologisk smärtlindring i palliativ vård.
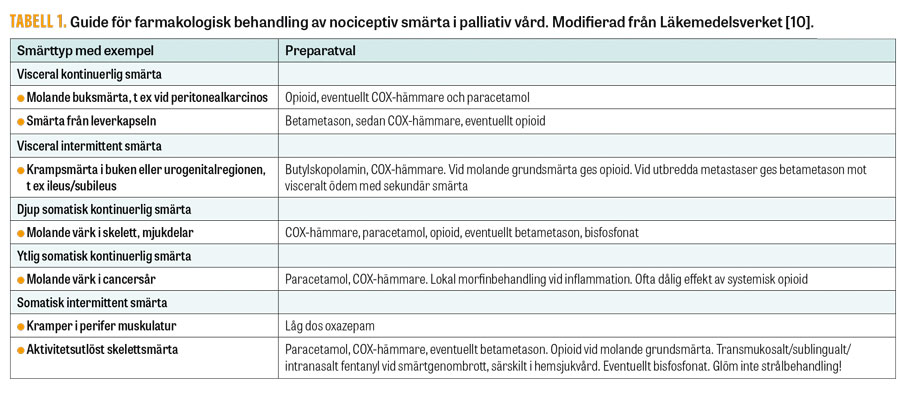
Tabell 1
Smärta är ett av de vanligaste symtomen hos patienter i palliativt sjukdomsskede. För att lyckas med smärtbehandlingen är det viktigt att behärska de grundläggande principerna kring smärtanalys, behandlingsstrategier och farmakologisk smärtlindring. Kunskapen ökar kring komplexa smärttillstånd och andra besvärande symtom i denna patientgrupp, och det är därför viktigt med kontinuerlig fortbildning för alla specialister som behandlar patienter i palliativt sjukdomsskede.
Smärtanalys och behandlingsstrategi
En noggrann smärtanalys med anamnes (Fakta 1), status och eventuell röntgenologisk undersökning utgör basen. Målet är att försöka förstå bakomliggande smärtmekanism(er), som kan innehålla både fysiologiska (nociceptiva och neuropatiska), psykologiska, sociala och existentiella komponenter. Smärtmekanismen ger sedan vägledning inför behandlingsvalet. När farmakologisk smärtlindring är aktuell ska också faktorer som patientens njurfunktion, förväntade biverkningar, administrationssätt och annan läkemedelsbehandling vägas in.
Målet är individualiserad behandling baserad på aktuell smärtmekanism, vilket i första hand leder till smärtfrihet i vila och acceptabel nattsömn. Behandlingen får inte ske på bekostnad av patientens livskvalitet, t ex svåra biverkningar. Är patienten smärtfri men oförmögen att kommunicera med närstående ska behandlingen omprövas och justeras.
Tabell 1 visar ett antal typexempel på olika nociceptiva smärttillstånd med förslag på tänkbar farmakologisk behandling.
Farmakologisk behandling av neuropatisk smärta
Vid spridd cancersjukdom ses inslag av neuropatisk smärta hos upp till 40 procent av patienterna [1], och det är viktigt att identifiera detta eftersom behandlingen skiljer sig från den som ges mot nociceptiv smärta. För diagnosen neuropatisk smärta krävs att patienten har känselstörning inom ett neuroanatomiskt korrelerbart område, t ex en perifer nervs utbredningsområde eller ett dermatom.
Fakta 2 ger exempel på preparatval vid neuropatisk smärta. Det finns få studier av specifik behandling av cancerrelaterad neuropatisk smärta. Tricykliska antidepressiva och gabapentin utgör ofta basbehandling, men även opioider har en plats vid neuropatisk smärta. Kortikosteroider kan minska ödemet runt den smärtande nervstrukturen och används inte sällan med god effekt. Kombinationsbehandling med ovanstående preparat blir ofta nödvändig, och ökad kunskap kring orsaker till neuropatisk smärta belyser komplexiteten vid dessa smärttillstånd [2]. Vid svåra smärttillstånd med neuropatiska inslag kan det bli aktuellt med NMDA-receptorblockad via metadon eller ketamin; här bör också spinal smärtlindring med ett lokalanestetikum vara ett alternativ.
Farmakologisk behandling av nociceptiv smärta
Opioider utgör basen för den farmakologiska behandlingen av smärta i palliativ vård, men behöver ofta kompletteras med läkemedel som angriper smärtan via andra mekanismer.
COX-hämmare, antikolinergika och kortikosteroider.COX-hämmare är särskilt värdefulla vid behandling av smärta med inflammatoriska inslag, t ex smärtande skelettmetastaser. Även vid viscerala smärttillstånd såsom koliksmärtor kan dessa preparat ha en god effekt genom minskad spasm i den glatta muskulaturen [3]. Ibuprofen och naproxen är vanliga preparat, och för parenteral behandling finns ketorolak.
COX-2-hämmare kan vara av värde hos patienter med stor blödningsrisk, eftersom mer COX-1-selektiva preparat inte är lämpliga på grund av den trombocythämmande effekten. Som exempel kan nämnas patienter med koagulationsrubbningar, dålig trombocytfunktion eller antikoagulantiabehandling. Parecoxib är en parenteral COX-2-hämmare som utgör ett alternativ till ketorolak. Den ökade kardiovaskulära risk som har uppmärksammats vid användande av COX-2-hämmare måste beaktas vid behandling av patienter med hjärt–kärlsjukdom, men tappar naturligt nog sin betydelse vid behandling av patienter med stor blödningsrisk i livets absoluta slutskede.
För samtliga dessa preparat gäller varsamhet vid nedsatt njurfunktion och hjärtsvikt.
Antikolinergika såsom glykopyrron och butylskopolamin minskar spasmen i glatt muskulatur och kan vara till stor hjälp vid kramptillstånd i viscerala organ, t ex vid ileus/subileus [4]. Kortikosteroider kan ha god smärtlindrande effekt som tillägg i denna patientgrupp, eftersom de ofta minskar illamåendet, förbättrar aptiten och ökar välbefinnandet [5]. I Sverige används huvudsakligen betametason.
Vid generaliserad smärta på inflammatorisk bas (typexempel är patienten med prostatacancer och migrerande, generaliserad skelettsmärta), leverkapselsmärta, medullakompression och huvudvärk vid hjärntumörer/-metastaser bör betametason finnas med bland behandlingsalternativen.
Övriga läkemedel. Bensodiazepiner kan vara verkningsfulla vid kramptillstånd i tvärstrimmig muskulatur. Man bör då välja preparat med kort halveringstid och få/inga aktiva metaboliter, förslagsvis oxazepam. Det parenterala förstahandsvalet är midazolam.
Bisfosfonater kan vara ett alternativ vid svårbehandlad skelettsmärta när vanliga analgetika och/eller strålbehandling inte ger avsedd effekt [6].
Opioider. Svaga opioider som kodein och tramadol bör undvikas vid smärtbehandling i denna patientgrupp. De har inte bättre effekt än COX-hämmare vid cancerrelaterad smärta [7] och har en takeffekt, dvs över en viss dos får patienten bara mer biverkningar och ingen förbättrad smärtlindring. Har patienten en opioidkänslig smärta blir därför valet en stark opioid. Enligt den senaste systematiska översikten från European Association for Palliative Care utgör morfin, oxikodon och hydromorfon likvärdiga förstahandspreparat [8]. I första hand rekommenderas peroral behandling.
Vid otillfredsställande smärtlindring trots ökad peroral dos görs övergång till parenteral administration med aktuell opioid, förutsatt att smärtan fortsatt bedöms vara opioidkänslig. Inom den palliativa vården finns en stor och mångårig erfarenhet av kontinuerlig subkutan behandling med portabel smärtpump, som möjliggör finjustering av dygnsdosen.
Peroral behandling med en stark opioid kan inledas direkt med en beredning med långsam frisättning (depåberedning) som ges i tvådos med 12 timmars mellanrum. Vid smärtgenombrott ges en extrados av motsvarande kortverkande opioid, som vid varje dostillfälle ska vara en sjättedel av patientens ordinarie dygnsdos av opioid. Med ledning av antalet extradoser under det senaste dygnet kan dosen av depåberedningen sedan successivt ökas. Parallellt med att dygnsdosen ökas behöver då också vidbehovsdosen justeras så att den motsvarar en sjättedel av ordinarie dygnsdos.
Vid nedsatt njurfunktion, särskilt vid GFR <30 ml/min, bör man på grund av ackumulation av aktiva metaboliter och risk för överdosering undvika morfin och hellre använda oxikodon eller transdermalt fentanyl [9]. Transdermal fentanylbehandling kan även vara ett alternativ vid stabil opioidkänslig smärta om patienten har svårt att svälja tabletter. Transdermal fentanylbehandling är dock olämplig vid instabil smärtsituation och behov av höga opioiddoser.
Nyare kortverkande beredningsformer av fentanyl med transmukosal, sublingual eller intranasal administration har ett snabbt och förutsägbart upptag med smärtlindrande effekt under ca 1 timme och utgör ett alternativ vid behandling av genombrottssmärtor [8], framför allt om patienten vistas i hemmet.
Biverkningar vid opioidbehandling. Vanliga biverkningar av de starka opioiderna är illamående, förstoppning och initial trötthet. Illamående och förstoppning ska förebyggas genom förskrivning av antiemetika (meklozin, metoklopramid eller haloperidol) och laxantia i form av osmotiskt verkande medel med eventuellt tillägg av motorikstimulerande preparat. Laxantiabehandlingen behöver som regel fortsätta under hela opioidbehandlingen, men antiemetika kan ofta flyttas över till vidbehovslistan efter någon vecka eftersom tolerans utvecklas mot illamående. Tröttheten klingar ofta av efter 4 till 5 dagars behandling.
Om patienten efter det är fortsatt onormalt trött och/eller har kognitiv påverkan samtidigt som smärtan har försvunnit, ska opioiddosen sänkas.
Risk för andningsdepression föreligger framför allt hos den opioidnaive patienten, men efter någon vecka med kontinuerlig opioidbehandling har kroppen utvecklat tolerans för detta. Smärta i sig stimulerar andningscentrum och motverkar den andningsdepression som kan ses vid opioidtillförsel till en frisk person.
Kan hjälpa många patienter
Med farmakologisk smärtlindring som bygger på ett smärtmekanistiskt tänkande kan vi hjälpa många patienter i palliativt sjukdomsskede. Opioider är den viktigaste preparatgruppen, men de behöver ofta kompletteras med läkemedel med andra angreppssätt. Det är angeläget att denna specialistkunskap når alla som behandlar dessa patienter; kanske är det dags att öppna dörren för palliativmedicinsk kompetens även inom svensk akutsjukvård.
Potentiella bindningar eller jävsförhållanden: Sedan början av 2000-talet har Staffan Lundström som expert föreläst för och erhållit arvode från ett flertal olika läkemedelsbolag: Mundipharma AB, GlaxoSmithKline, Roche, Fresenius Kabi, Baxter AB, Smith Nephew och Convatec.
Fakta 1. Smärtanamnes
Upptagning av anamnes hos patienter i palliativ vård bör omfatta frågor om följande:
- Besvärsdebut
- Smärtlokalisation
– välavgränsad
– diffus
– utstrålande (nervrotsengagemang?)
- Tidsförlopp
– konstant
– intermittent
– variation över dygnet
– aktivitetsutlöst
- Karaktär
– molande, dov, konstant (ofta nociceptiv)
– huggande/skärande (ofta nociceptiv [från leder och viscera])
– tryckande, bultande/pulserande (ofta nociceptiv [från kärl])
– brännande/ilande/stickande (ofta neuropatisk)
- Intensitet
– VAS/NRS (numerisk skala) eller verbal skattning. För kognitivt påverkade vuxna kan man använda sig av Abbey Pain Scale (finns tillgänglig på www.palliativ.se)
- Faktorer som förvärrar eller förbättrar smärtan
Fakta 2. Preparatval vid neuropatisk smärta
Förslag på preparatval vid neuropatisk smärta
- Gabapentin
- Amitriptylin
- Duloxetin
- Opioider
- Steroider
Preparatval vid lokal perifer neuropatisk smärta med allodyni
- Lidokainplåster
Preparatval vid samtidig depression
- Amitriptylin eller duloxetin
Preparatval vid samtidig ångest
- Pregabalin
























