Nanomaterial kan komma att användas inom medicinen inom en snar framtid, exempelvis inom bilddiagnostik, men även för målstyrd leverans av läkemedel. Nanopartiklar kan även användas för att oskadliggöra eller avlägsna toxiner från blodet.
Nanotoxikologi syftar till att förstå de toxiska effekterna av nanomaterial vid avsiktlig eller oavsiktlig exponering; förhoppningen är att möjliggöra framställning av icke-toxiskt material utan att de eftertraktade egenskaperna går förlorade.
Nanomaterial som kommer i kontakt med biologiska system eller frigörs i naturen kläs snabbt i ett hölje av organiska eller oorganiska substanser, och dessa adsorberade substanser och molekyler (biokorona) spelar en viktig roll för nanomaterialens toxicitet.
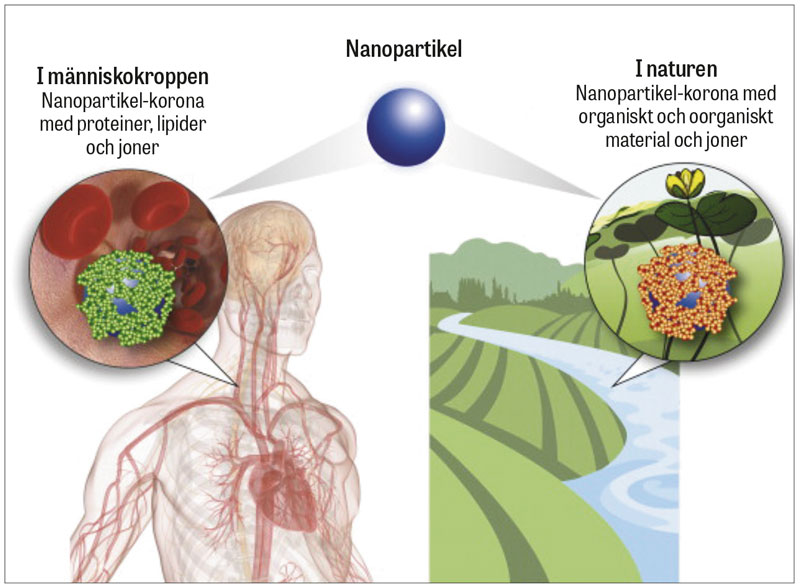
Figur 1. Nanomaterial har en biologisk identitet. Nanopartiklar som hamnar i blodbanan (vänster) eller i andra organ eller frisätts i naturen (höger) adsorberar biomolekyler och andra organiska eller oorganiska substanser, och detta ythölje (biokorona) påverkar partiklarnas toxicitet. Modifierad med tillstånd från Winkler och medarbetare [40].
Nanoteknik innebär avsiktlig framställning av material i nanostorlek i syfte att tillvarata de nya och ibland oväntade fysikalisk-kemiska egenskaperna som då uppstår, och med nanomedicin menas helt enkelt att nanotekniken appliceras för kliniskt bruk [1]. Det är värt att påminna om att många biologiska strukturer också har nanodimensioner, vilket innebär att syntetiska nanopartiklar skulle kunna påverka och interagera med biologiska nanostrukturer [2]. Det faktum att nanopartiklar är små gör att de också kan vara mycket användbara inom medicinen, exempelvis för målstyrd leverans av läkemedel vid behandling av cancer [3] eller diabetes [4]. Lovande djurförsök har även visat att magnetiska nanopartiklar kan användas för att avlägsna toxiner och patogener in vivo [5] eller utanför kroppen, som ett slags dialys [6]. Det finns i dag nanopartiklar godkända för kliniskt bruk, bland annat magnetiska nanopartiklar av järnoxid som används som kontrastmedel vid undersökning med magnetkamera [1]. För en mer detaljerad genomgång av nanomedicinska applikationer hänvisas till andra artiklar i detta temanummer. Problemet är att deras litenhet också gör att nanopartiklar kan åstadkomma oönskade effekter till följd av att de lyckas korsa biologiska barriärer, till exempel blod–hjärnbarriären eller blod–luftbarriären i lungorna [7].
På EU-nivå satsas det stort på nanosäkerhetsforskning, och inte mindre än 50 olika forskningsprojekt har finansierats enbart inom det sjunde ramprogrammet (www.nanosafetycluster.eu). I Sverige startade nyligen projektet MISTRA Environmental Nanosafety, med fokus främst på effekterna av nanomaterial i miljön (www.mistraenvironmentalnanosafety.org). Konsortiet avser bland annat att studera partiklar av volframkarbid (en legering av volfram och kol som ger upphov till ett mycket hårt material) som kan uppstå vid slitage av dubbdäck mot vägbanan, en angelägenhet inte minst på våra breddgrader. Betydelsen av den »biokorona« (se nedan) som uppstår på ytan av nanopartiklar kommer också att undersökas, såväl de molekyler som adsorberas av nanopartiklar i kroppen som det hölje av substanser som uppstår vid frisättning av nanopartiklarna i miljön (Figur 1).
Hur exponeras vi för nanopartiklar?
Vid yrkesexponering är de viktigaste exponeringsvägarna för nanopartiklar via lungorna och huden. Som konsument kan man också exponeras via lungorna och huden, men även via mag–tarmkanalen eftersom nanopartiklar kan förekomma i livsmedel och livsmedelsförpackningar. För ett par år sedan genomförde en forskargrupp i Australien en studie där solskyddsmedel innehållande radioaktiva nanopartiklar av zinkoxid applicerades på försökspersonernas hud (utomhus, under 5 dagar), varpå man undersökte om partiklarna (eller kanske Zn-jonerna) adsorberats genom huden. Man fann att så var fallet, om än i mycket liten utsträckning [8]. Dessutom publicerade amerikanska forskare nyligen en studie gjord på ett 60-tal försökspersoner som visade att oralt intag av kollodialt silver (dvs silvernanopartiklar) i upp till 14 dagar inte är förenat med några kliniskt påvisbara besvär [9]. Detta är den enda kontrollerade studien av oralt intag av syntetiska nanomaterial hos människa till dags dato. Majoriteten av alla nanotoxikologiska studier görs av förklarliga skäl i cellkultur eller på djur.
Det finns än så länge inga rapporterade fall av sjukdom orsakad av exponering för syntetiska nanomaterial [10]. Däremot finns epidemiologisk forskning som påvisat ett samband mellan exponering för luftburna partiklar som alstras genom förbränningsprocesser eller mekanisk nötning och kardiovaskulär morbiditet och mortalitet [10]. I en studie som publicerades hösten 2015 kunde man påvisa kolbaserade föroreningar i form av kolnanorör i luftvägarna hos barn med astma, och utifrån detta gjordes antagandet att alla som lever i en trafikerad miljö – barn såväl som vuxna – sannolikt är exponerade för sådana (antropogena) material [11]. I den aktuella studien tog man dock inte ställning till om dessa partiklar gav upphov till astmabesvären. Det är också välkänt att det bildas stora mängder nanopartiklar vid svetsning, och aktuell forskning talar för att det finns ett samband mellan dessa nanopartiklar och luftvägsbesvären hos svetsare [12], även om denna yrkesgrupp också kan vara utsatt för andra faktorer utöver nanopartiklar. I ytterligare en rapport beskrev kinesiska forskare hur ett antal kvinnliga arbetare utvecklade allvarliga luftvägssymtom – två av kvinnorna avled – och att man funnit nanopartiklar av polyakrylat på arbetsplatsen samt att man påvisat nanopartiklar i lungorna hos några av dessa patienter [13]. Man drog slutsatsen att nanopartiklarna var orsaken till den allvarliga lungsjukdomen hos dessa arbetare. Artikeln har emellertid fått svidande kritik från flera håll, inte minst därför att den faktiska exponeringen inte kontrollerades och därför att orsakssambandet inte kunde verifieras; dessa kvinnor hade sannolikt varit utsatta för många andra skadliga substanser, och studien får nog sägas framför allt påvisa vikten av personlig skyddsutrustning och adekvat ventilation, något som helt saknades.
De senaste årens forskning har visat att en intakt hud utgör en fullgod barriär mot nanopartiklar. Men om huden är skadad kan det se annorlunda ut. Ilves et al [14] kunde visa att nanopartiklar av zinkoxid (förekommer bl a i solskyddsmedel) kunde penetrera huden hos möss med atopisk dermatit samt att nanopartiklar som applicerades på huden fungerade som adjuvans och gav upphov till en kraftig ökning av IgE-antikroppar hos möss som samtidigt stimulerades med allergen (ovalbumin) [15]. I en annan studie fann man att nanopartiklar av kiseldioxid i sig själva inte hade någon effekt på huden hos möss med atopisk dermatit men att nanopartiklarna tillsammans med ett allergen (husdammskvalster) påverkade antikroppsnivåerna [15]. Nanopartiklar som hamnar i blodbanan på ett eller annat sätt (avsiktligt eller oavsiktligt) skulle kunna korsa inre biologiska barriärer, till exempel blod–hjärnbarriären. Hos den gravida kvinnan är det möjligt att nanopartiklar skulle kunna korsa placentabarriären och/eller påverka placentan så att dess barriärfunktion störs [16]. Detta är ett område där mer forskning behövs.
Kolnanorör en möjlig karcinogen
Det är viktigt att inte dra alla nanomaterial över en kam. Men samtidigt finns det studier som visar att vissa nanomaterial skulle kunna ge upphov till skadliga effekter under förutsättning att människor exponeras för dessa material. Kolnanorör framställs i stora volymer över hela världen. Kolnanorör kan antingen förekomma som enkelväggiga eller flerväggiga strukturer (ihåliga »rör«) med en diameter på ett par upp till ett tiotal nanometer och en längd som kan variera avsevärt. Studier som gjordes på möss redan för 10 år sedan visade att enkelväggiga kolnanorör kan ge allvarliga skador på lungorna. Kolnanorör som placeras i svalget och sedan tar sig ner i luftvägarna hos möss kan ge upphov till inflammation med granulombildning samt bindvävsomvandling (fibros) [17].
Möss som exponeras för samma mängd kimrök, ett kolbaserat nanomaterial som utgör ett vanligt fyllnadsmedel i gummiblandningar, uppvisar inte dessa symtom. Man fann även att lungfunktionen var nedsatt hos möss som exponerats för kolnanorör [17].
Dessa fynd, och det faktum att kolnanorör till sin form liknar asbestfibrer, gör att det finns farhågor om att kolnanorör kan påverka människors hälsa på ett liknande sätt. I en mycket uppmärksammad studie som publicerades 2008 fann Poland et al [18] att flerväggiga kolnanorör som injicererades intraperitonealt hos möss gav upphov till granulombildning och att dessa symtom var längdberoende, det vill säga långa kolnanorör (i det här fallet kolnanorör där en betydande andel av fibrerna var längre än 20 µm) gav upphov till granulombildning, medan korta kolnanorör var förhållandevis inerta. Man studerade inte förekomsten av mesoteliom (den cancerform som är mest förknippad med exponering för asbestfibrer) men drog ändå slutsatsen att flerväggiga kolnanorör uppvisar samma beteende som asbestfibrer [18]. Det är ett väletablerat samband att långa och tunna (och biopersistenta) fibrer ger upphov till patologiska effekter.
Andra forskare har visat att flerväggiga kolnanorör når ända ut till pleuran och ger upphov till subpleural fibros hos möss som inandas dessa material i hög dos under kort tid (6 timmar) [19]. Det är alltjämt kontroversiellt huruvida kolnanorör kan ge upphov till mesoteliom [20], men på basis av ett flertal olika djurstudier så kom IARC (samarbetsorganet för WHO och FN i frågor som rör cancerepidemiologi) hösten 2014 fram till att vissa – dock inte alla – kolnanorör bör klassas som en »möjlig karcinogen« [21].
Enzymatisk nedbrytning av kolnanorör
En slutsats av ovanstående resonemang är att alla kolnanorör inte bör klumpas ihop och betraktas som ett enda material; det är med andra ord skillnad på kolnanorör och kolnanorör. Li et al [22] visade nyligen att ytladdningen hos flerväggiga kolnanorör är avgörande för deras förmåga att inducera lungfibros hos möss, således kunde man reducera toxiciteten genom att modifiera ytan hos dessa nanomaterial på kemisk väg. I en annan studie av brittiska och italienska forskare visade man att långa kolnanorör kunde modifieras på kemisk väg så att dessa material inte längre gav upphov till granulombildning hos möss [23].
Båda dessa studier är exempel på framställning av icke-toxiskt material med bevarad funktion. Det är viktigt att de eftertraktade egenskaperna bibehålls när man gör dessa förändringar av ytegenskaperna. Till saken hör också att asbestfibrer är biopersistenta, det vill säga att dessa material inte kan städas undan av kroppens immunförsvar. Frågan är hur det förhåller sig med kolnanorören. Vår forskargrupp har tillsammans med amerikanska kollegor kunnat påvisa att enkelväggiga kolnanorör bryts ner av myeloperoxidas, ett enzym som uttrycks i höga koncentrationer i neutrofila granulocyter och som frisätts då dessa celler aktiveras [24]. I en annan rapport beskrevs hur makrofager kan bryta ner kolnanorör [25].
Nanomaterial har en biologisk identitet
Nanomaterial uppvisar sällan eller aldrig en »naken« yta i ett biologiskt system utan de adsorberar i stället olika proteiner och lipider och troligen även andra biomolekyler beroende på sin storlek, ytladdning, grad av funktionalisering och så vidare. Denna »biokorona« kan variera beroende på den biologiska miljö som nanopartiklarna hamnar i (blodbanan, luftvägarna osv), och man kan således tala om en ny biologisk »identitet«. På liknande sätt kan ett ytskikt av organiska och oorganiska substanser adsorberas till nanopartiklarna i naturen (Figur 1).
De senaste årens forskning har gett vid handen att det är biokoronan som avgör hur immunförsvaret »ser« nanopartiklarna [26] och även reglerar cellulärt upptag av nanomaterial [27]. Tenzer et al [28] kunde visa att en biokorona bildas mycket snabbt (inom mindre än en halv minut) hos nanopartiklar som kommer i kontakt med blodplasma, och dessutom visade man att detta ytskikt av plasmaproteiner påverkade graden av hemolys samt graden av trombocytaktivering. Kapralov et al [29] i sin tur har visat att både proteiner och lipider ingår i den biokorona som bildas på kolnanorör i lungorna hos möss samt att denna »korona« påverkar upptag av makrofager. Andra forskare har visat att det bildas en biokorona på liposomer som administreras i blodbanan hos möss och att detta hölje av proteiner påverkar receptormedierat upptag av dessa partiklar [30].
Att partiklarna maskeras av en biokorona måste alltså tas med i beräkningen när man framställer målstyrda, det vill säga ligandförsedda, nanopartiklar för medicinskt bruk [31]. Men i vissa sammanhang vill man åstadkomma just att partiklarna flyger under radarn och undgår igenkänning av kroppens immunförsvar [32].
Mot en säker hantering av nanomaterial
Det är ingen tvekan om att det forskas mycket på nanomaterial. Men man kan fråga sig om vi är på rätt spår, om all denna forskning under mer än ett decennium har gjort att vi nu »förstår« och kan hantera nanomaterial på ett säkert sätt [33]. I Sverige har en nationell plattform för säker hantering av nanomaterial etablerats för att främja kunskapsutbytet mellan akademi, näringsliv, myndigheter och andra aktörer (www.swetox.se). Detta är ett steg i rätt riktning, men det är också viktigt att en nationell handlingsplan utvecklas i samklang med internationella insatser inom EU och OECD. Dagens nanosäkerhetsforskning är till sin natur interdisciplinär men också internationell, och det behövs en konsensus eller åtminstone en dialog kring dessa frågor, till exempel med vilka metoder man bör mäta och testa nanomaterial och huruvida nanomaterial bör klassas som nya material eller inte enligt den europeiska kemikalielagstiftningen, Reach.
Men vad är det som återstår, vad bör den fortsatta forskningen framför allt ta sikte på? Det är tydligt att vi måste lära oss mera om nanomaterialens egenskaper, inte bara hur materialen beter sig i laboratoriet utan också i relevanta biologiska miljöer. Nanomaterial kan »åldras«, inte minst i naturen, och i och med det förändras också deras egenskaper och (kanske) även deras toxicitet [34]. En utmaning därvidlag är att de nanomaterial som studeras ofta är inhomogena och i själva verket utgör en blandning av partiklar med olika storlek, form, ytegenskaper och så vidare, vilket gör det svårt att dra slutsatser om vilka av dessa egenskaper som ger upphov till de biologiska effekterna. Utöver nanomaterialens inneboende egenskaper – som alltså kan förändras på ett dynamiskt vis – måste hänsyn också tas till den förvärvade biologiska identiteten, som i stor utsträckning beror på vilka proteiner, lipider eller andra substanser som adsorberas på ytan, och även denna biokorona kan alltså förändras vid nanopartiklarnas resa genom människokroppen alternativt då nanopartiklarna hamnar i den naturliga miljön. Dessutom behövs validerade in vitro- och in vivo-metoder samt metoder för screening av ett stort antal olika nanomaterial, och det behövs även referensmaterial för att kunna jämföra resultaten mellan olika laboratorier [35, 36].
Nya systembiologiska verktyg kan underlätta förståelsen av bakomliggande mekanismer, och dessa metoder kan även ge uppslag till nya biomarkörer så att exponering och effekt kan mätas [37]. Det behövs också nya metoder för att kunna detektera nanomaterial i biologisk vävnad. Chen et al [38] kunde nyligen påvisa olika kolbaserade nanomaterial med hög känslighet genom en masspektrometribaserad metod, ett slags »molekylär histologi« som kan appliceras utan att partiklarna i sig själva är inmärkta.
Slutligen behövs mycket mer information om hur den faktiska exponeringen för nanomaterial ser ut för att kunna göra en adekvat riskbedömning [39] – risk är alltid en produkt av både fara och exponering, och toxicitet hos en viss substans är alltid en dosfråga, så även för nanomaterial. Eller som Falstaff, Fakir uttryckte det i En hvar sin egen professor: »Vattnet är ett farligt gift, vilket omger Visby stift«.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Läs också författarintervjun med Bengt Fadeel.
























