Fosterkirurgi är en växande multidisciplinär subspecialitet med fokus på att förbättra naturalförloppet vid livshotande och svåra medfödda missbildningar och sjukdomar.
Fosterkirurgi vid ryggmärgsbråck leder till bättre postnatal neurologisk funktion och halvering av shuntbehovet vid hydrocefalus.
Endoskopisk ballongocklusion av trakea på foster med kongenitalt diafragmabråck kan bli en framtida behandlingsmetod vid risk för allvarlig lunghypoplasi.
Förlossning med säkring av fri luftväg med s k EXIT (ex utero intrapartum treatment) är livräddande för foster med larynxatresi eller huvud–halstumörer. EXIT kräver ett väl samtränat multidisciplinärt team och bör endast utföras på centrum med vana av ingreppet.
Indikationerna för fosterkirurgi har i första hand varit livräddande åtgärder i situationer där fostret annars riskerar att dö perinatalt, men på senare år har indikationerna vidgats till att även inkludera interventioner med syfte att förbättra naturalförloppet vid vissa allvarliga medfödda sjukdomar och missbildningar. Generellt är ett kirurgiskt ingrepp på foster indikerat endast för tillstånd med känt naturalförlopp, vilka med stor sannolikhet obehandlade leder till döden eller till gravt kroniskt handikapp. Detta ökar kraven på den diagnostiska säkerheten. Man ska inte endast kunna ställa en säker diagnos, utan man måste också kunna avgöra hur allvarlig missbildningen är i det individuella fallet och hur naturalförloppet utan fetalt ingrepp torde utveckla sig.
Eftersom effekterna av det kirurgiska ingreppet omfattar två individer (kvinnan och fostret), ska risken för allvarliga maternella komplikationer vara liten [1]. Oavsett om ingreppet görs med endoskopisk teknik eller med öppen hysterotomi är prematur vattenavgång och förtidsbörd gemensamma och vanliga komplikationer vid alla fosterinterventioner [2].
Syftet med denna artikel är att beskriva den viktigaste forskningen och erfarenheterna av dessa ovanliga ingrepp internationellt samt ge en samlad bild av var fosterkirurgin står i dag. Vi vill även beskriva vad som förväntas bli möjligt att utföra i framtiden. Majoriteten av de fosterinterventioner som utförs i Sverige i dag beskrivs i en artikel av Eleonor Tiblad et al i detta tema.
Ryggmärgsbråck
Fosterkirurgi för myelomeningocele och myeloschis är i dag en etablerad behandlingsmetod vid flera centrum i världen. I en prospektiv randomiserad studie (MOMS; Management of myelomeningocele study), finansierad av amerikanska National Institutes of Health (NIH) och publicerad i New England Journal of Medicine 2011, jämfördes resultaten av fetal slutning med traditionell postnatal behandling. En interimsanalys efter det att 183 patienter inkluderats visade signifikant bättre utfall efter öppen prenatal kirurgi, med konsekvensen att studien avslutades i förtid [3].
Skälet till att intervenera prenatalt är att foster med ryggmärgsbråck drabbas av progressiv försämring av funktion under andra halvan av graviditeten. Sannolikt sker försämringen på grund av både mekanisk skada på ryggmärgen efter nötning mot livmoderväggen och toxisk påverkan av substanser i fostervattnet, som utgörs av fostrets urin som blir alltmer koncentrerad i tredje trimestern. Genom att redan under fosterstadiet sluta ryggmärgsbråcket kan man undvika progressiv nervskada och funktionsbortfall och reversera den herniering av lillhjärnan ned i bakre skallgropen (Arnold–Chiari II-missbildning) som uppstår vid de flesta öppna ryggmärgsbråck.
Fosterkirurgi botar inte ryggmärgsbråck, men kan medföra vissa funktionsförbättringar. Det ökar sannolikheten för bättre gångförmåga och för att förhindra Chiari-missbildning och shuntkrävande hydrocefalus (riskkvot 0,48) [4, 5].
De fetala ingreppen sker vid 19–26 graviditetsveckor. Allvarliga komplikationer som perinatal död i nära anslutning till operationen eller prematur förlossning före 30 veckor förekom i 2,5 respektive 13 procent av fallen [3-5]. Graviditetslängden vid förlossning efter fosterkirurgi är i genomsnitt drygt 34 fullgångna veckor. Effekten på kognitiva funktioner, kontroll över blåsa och tarm och sexuell funktion är ännu inte utvärderad i långtidsuppföljningar, men sådana väntas komma inom några år.
De maternella riskerna vid öppen fetal kirurgi är inte negligerbara och innefattar transfusionskrävande blödning (4–9 procent) och lungemboli eller lungödem (2–6 procent) sekundärt till tokolytisk behandling och djup generell anestesi. Ökad risk för komplikationer finns såväl vid den aktuella graviditeten (prematur vattenavgång, placentaavlossning) som vid framtida graviditeter som en konsekvens av en tunn eller fenestrerad uterusvägg efter kirurgin [3, 5, 6].
De centrum som utför ingreppen i Europa – universitetssjukhusen i Leuven (Belgien), Zürich (Schweiz)och Katowice (Polen) – och USA informerar föräldrarna utförligt preoperativt om både maternella och fetala risker.
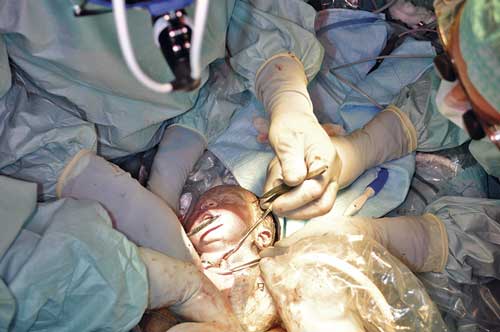
Operationen utförs med EXIT-metod (ex utero intrapartum treatment) (se nedan). Hysterotomin utförs efter kartläggning med ultraljud av placentans nedre kant i optimalt område så att fostrets rygg exponeras. Vid ventral placenta lyfts uterus ut ur buken genom laparotomin, och hysterotomin uförs upptill i fundus uteri eller i bakväggen. Fostret ligger kvar i livmodern och sövs samt erhåller även analgesi, både via moderns anestesi och med tillägg av fentanyl intramuskulärt. För att undvika navelsträngskompression instilleras uppvärmd Ringer-acetat i livmodern som substitut för fostervattnet när hinnorna öppnats. Ryggmärgsbråcket sluts därefter av neurokirurg på sedvanligt sätt (Figur 1).
Intensiv övervakning av kvinnan och fostret är nödvändig de första 48 timmarna postoperativt, då även kombinerad tokolytisk behandling ges. Kvinnan förlöses med kejsarsnitt i fullgången tid eller vid prematur förlossningsstart, liksom vid alla framtida graviditeter på grund av ökad risk för uterusruptur.
Det finns även centrum i Europa och i övriga delar av världen som utför ingreppet minimalinvasivt via endoskop, men resultaten av denna metod är ännu inte utvärderade i någon prospektiv randomiserad studie. Hittills har två patienter från Sverige behandlats med öppen prenatal kirurgi för ryggmärgsbråck i Polen respektive Schweiz. Det första barnet föddes mycket prematurt 1 månad efter operationen. Det andra barnet föddes i graviditetsvecka 36, har god motorisk funktion och blåsfunktion, men har behövt en ventrikulo-peritoneal shunt. Inga maternella komplikationer inträffade.
Kongenitalt diafragmabråck
Kongenitalt diafragmabråck är en missbildning orsakad av en defekt i diafragmamuskeln. Magsäck, tarm, mjälte och ofta även levern hernierar upp i torax, där de komprimerar lungorna, vilket orsakar lunghypoplasi och pulmonell hypertension. Graden av lunghypoplasi och pulmonell hypertension blir avgörande för patientens överlevnad [7]. Kongenitalt diafragmabråck förekommer i en frekvens av 1:2 500–3 000 födda barn, vilket innebär att det i Sverige årligen föds omkring 30–40 barn med denna missbildning.
I allvarliga fall får patienten grav andningspåverkan direkt efter födelsen, vilket kräver omedelbar intubation och assisterad ventilation med hög syrgaskoncentration. Patienter med svår lunghypoplasi och pulmonell hypertension kan även behandlas med ECMO (extrakorporeal membranoxygenering), vilket är en modifierad hjärt–lungmaskin som barnet kopplas till om adekvat gasutbyte inte kan erhållas med ventilation i respirator [8]. Trots förbättringar av intensivvården kvarstår en mortalitet på minst 20–30 procent upp till tonåren [9, 10], och det förekommer en betydande morbiditet bland överlevande patienter [11]. Om även de drygt 20 procent av fallen där graviditeten avbryts räknas med, är den totala överlevnaden vid 1 års ålder endast ca 50 procent.
Kongenitalt diafragmabråck var en av de första missbildningarna där fosterkirurgi började tillämpas med syfte att minska graden av lunghypoplasi och öka den postnatala överlevnaden. Under 1980-talet genomfördes först öppen kirurgi och senare försök att ligera trakea för att stimulera lungtillväxt. Stora förhoppningar sattes till denna nya behandlingsform, men resultaten från en NIH-finansierad randomiserad studie visade klart sämre överlevnad hos de prenatalt opererade fallen än hos de barn som erhöll konventionell postnatal behandling, och den öppna kirurgiska behandlingen upphörde [12].
I Europa utvecklades av en ny endoskopisk teknik där en silikonballong placeras i trakea strax ovan karina, och detta har lett till nya studier om effekten av prenatal behandling vid diafragmabråck. Operationen benämns fetal endoskopisk trakeal ocklusion. Ocklusionen leder till att vätska som utsöndras i luftvägarna under fosterlivet stannar kvar och lungorna expanderar. Detta verkar stimulera lungtillväxt och även lungkärlsutveckling sekundärt [13, 14]. För optimal effekt avlägsnas ballongen endoskopiskt efter 4 veckor. Startar förlossningen prematurt är det av största vikt att ballongen avlägsnas alternativt punkteras ultraljudslett för att säkra fri luftväg för barnet (Figur 2) [15].
En kvarstående utmaning är att korrekt kunna selektera patienter som kan ha nytta av prenatal intervention. Den observerade och den förväntade kvoten mellan lungvolym och huvudomkrets (lung-to-head ratio) och leverpositionen har visat sig vara den bästa prenatala prognostiska markören hittills. Observerad/förväntad lunga/huvudkvot <35 procent och/eller intratorakal lever samt högersidiga bråck är associerat med sämre prognos [16].
Det pågår en prospektiv randomiserad multicenterstudie (TOTAL trial) med syfte att jämföra överlevnad och sjuklighet vid uttalad lunghypoplasi (observerad/förväntad lunga/huvudkvot <25 procent) respektive moderat lunghypoplasi (observerad/förväntad lunga/huvudkvot 26–35 procent) hos dem som genomgår fosterkirurgi med dem som behandlas postnatalt [15]. Information om studien och deltagande centrum finns på www.totaltrial.eu. Resultaten ser preliminärt lovande ut med fördubblad överlevnad för gruppen med den svåraste graden av lunghypoplasi [15].
Sverige deltar inte i studien men kan remittera patienter för deltagande, och tre patienter med dålig prognos har remitterats från Sverige till Leuven i Belgien. Två av dem erhöll behandling prenatalt, varav en överlevde. Om studien visar positiva resultat kan det bli aktuellt att erbjuda fetoskopisk ballongocklusion som behandling även i Sverige.
EXIT-metoden
EXIT är ett ingrepp med syfte att säkra fri luftväg hos det nyfödda barnet för att undvika neonatal asfyxi och hjärnskada (Figur 3 och 4). Luftvägen säkras med antingen intubation eller trakeotomi, medan den uteroplacentära cirkulationen bibehålls genom navelsträngen [17]. Metoden utvecklades initialt för att kunna säkra fri luftväg efter fosterkirurgi för trakeal ocklusion med clips hos foster med diafragmabråck. Indikationerna har dock utvidgats till larynxatresi, stora orofaryngeala tumörer och cervikala tumörer som komprimerar trakea liksom befarad lunghypoplasi på grund av intratorakala cystor, tumörer och vätskeansamlingar (Fakta 1) [18].
Som längst har man kunnat bibehålla den uteroplacentära cirkulationen och syresättningen till barnet i upp till 90 minuter under det att fri luftväg säkras [17].
Eftersom dessa diagnoser är extremt ovanliga utförs endast någon enstaka EXIT-operation årligen i Sverige. Centrum för fostermedicin vid Karolinska universitetssjukhuset i Stockholm har genomfört sammanlagt nio EXIT-förlossningar sedan 1998 på indikationerna teratom, lymfatisk missbildning, larynxatresi samt orofaryngeal tumör. Åtta barn överlevde; ett avled senare postnatalt på grund av grundsjukdomen. Inga maternella komplikationer tillstötte.
En EXIT-operation kräver ett väl samtränat multidisciplinärt team av fostermedicinare, obstetriker, öron-, näs- och halsspecialist, anestesiolog, neonatolog och barnkirurg.
Den kongenitala missbildningen och fostrets luftvägar kartläggs noga prenatalt med hjälp av ultraljud och magnetröntgen. Den gravida kvinnan sövs mycket djupt med inhalationsanestesi för att uppnå maximalt relaxerad livmoder, eftersom kontraktioner försämrar gasutbytet till fostret och ökar risken för placentaavlossning under ingreppet. Med hjälp av intraoperativt ultraljud kartläggs placentans utbredning, och hysterotomin planeras i ett fritt fönster för att undvika maternella blödningar. Hysterotomin kan utföras med resorberbara stejplar som säkerställer hemostas och fäster fosterhinnorna till myometriet.
Därefter förlöses endast barnets huvud, övre delen av bröstkorgen och armarna genom hysterotomin, och barnet placeras i ett vidöppet läge som möjliggör intubation eller trakeotomi. Resten av kroppen behålls intrauterint för att undvika dels kompression av navelsträngen, dels placentaavlossning. Uppvärmd Ringer-acetat infunderas kontinuerligt i uteruskaviteten för att undvika kompression av navelsträngen. Barnet övervakas under ingreppet med pulsoximetri och intraoperativ ekokardiografi. Intravenös infart kan sättas i en fri arm, där ytterligare anestesi och smärtlindring kan ges till barnet.
Man utvärderar luftvägen och eventuell tumörutbredning och intuberar om möjligt med laryngoskop eller använder bronkoskop för att säkra luftvägen. Är detta inte möjligt utförs dissektion samt trakeotomi med eventuellt retrograd intubation. Vid stora halstumörer kan tumörresektion vara nödvändig initialt för att få access till halsen [17]. När luftvägen är säkrad och man kan ventilera barnet förlöser man resten av kroppen.
Risken för maternell blödning >1 000 ml är ökad, men vid ett väl planerat och genomfört ingrepp är risken för maternell morbiditet liten och jämförbar med den efter akuta kejsarsnitt [19].
Medfödda hjärtfel
Ultraljudsledda fetala hjärtinterventioner med ballongvidgning vid vissa mycket allvarliga medfödda hjärtfel utförs vid flera centrum i världen (www.ifcir.org). Indikationen är framför allt uttalad aortastenos med risk för utveckling av hypoplastiskt vänsterkammarsyndrom. Andra indikationer är pulmonalisatresi med intakt kammarseptum och risk för utveckling av hypoplastiskt högerkammarsyndrom samt hypoplastiskt vänsterkammarsyndrom med restriktivt förmaksseptum.
Naturalförloppet fetalt vid dessa missbildningar är annars progress från fungerande biventrikulär cirkulation till enkammarhjärtan samt myokardskada.
Syftet med interventionen är att förbättra möjligheterna till bevarande av biventrikulär cirkulation postnatalt och att förbättra möjligheten till perinatal överlevnad [20, 21]. Mer än 250 interventioner på dessa indikationer har publicerats hittills [21]. Resultaten talar för att man kan förbättra prognos och överlevnad i mycket väl selekterade fall. Dock saknas utvärdering av överlevnad och långtidsutfall i större kontrollerade randomiserade studier. Fetala hjärtinterventioner har hittills inte utförts i Sverige.
Cystisk adenomatoid avvikelse och sekvestrerad lunglob
Förbättringar i obstetrisk ultraljudsdiagnostik har resulterat i ökad prenatal detektion av fetala lungmissbildningar. Incidensen anges i dag till 1/10 000–35 000 graviditeter [22].
Kongenital cystisk adenomatoid missbildning (congenital cystic adenomatoid malformation; CCAM) eller numera kongenital missbildning av lungvävnaden (congenital pulmonary airway malformation; CPAM) är en typ av lungmissbildning som kommunicerar med bronkialträdet och har sin kärlförsörjning från lungkärlen. Hyperekogeniteten gör att den tydligt kan visualiseras med fetalt ultraljud.
Bronkopulmonell sekvester är avdelad, icke-funktionell lungvävnad med egen kärlförsörjning från aorta.
Naturalförloppet hos bägge typerna av missbildning är oftast gynnsamt, och de allra flesta patienter kan följas upp postnatalt och behandlas endast vid symtom. I enstaka fall kan missbildningen växa avsevärt och leda till kompression av lungor och kärl i mediastinum, vilket orsakar hjärtsvikt och hydrops fetalis som obehandlad resulterar i intrauterin fosterdöd [23]. Vid begynnande hydropsutveckling är prenatal intervention indicerad [23]. Foster med utbredda mikrocystiska lungmissbildningar kan behandlas med steroider i första hand, vilket i 80 procent av fallen ger regress av hydrops [24]. Om tecken på hydrops kvarstår, är behandlingsalternativen beroende av graviditetslängden [25]. Förlossning före 32 graviditetsveckor innebär extremt dålig prognos.
Om patienten inte svarar på upprepade doser steroider, har öppen fosterkirurgi med intrauterin lungresektion försökts i små serier på 24 patienter vid ett fåtal centrum i världen med ca 50 procents överlevnad [3, 24].
Makrocystiska missbildningar kan dekomprimeras perkutant med ultraljudsledd torakocentes eller genom inläggning av en torakoamniotisk shunt [26].
För foster med sekvestrerad lunglob och hydrops har prenatal laserablation av försörjande artärer prövats. Laserbehandlingen har visats minska behovet av postnatal lungresektion [27]. Vid hydrops efter graviditetsvecka 32 har man vid Children’s Hospital of Philadelphia, USA (det fosterkirurgiska centrum som har störst erfarenhet internationellt) prövat med EXIT-förlossning och samtidig torakotomi och resektion av missbildningen innan barnet ska börja andas [28].
Ett annat alternativ, vid fall av stora tumörer där barnet inte förväntas kunna syresätta sig ens i respirator, är EXIT-till-ECMO. Det innebär att patienten behandlas direkt med ECMO [28] och opereras senare i stabilt skede postnatalt.
Sakrokoccygealt teratom
Sakrokoccygealt teratom är den vanligaste typen av germinalcellstumör. Prevalensen är ca 1:20 000–40 000 födda barn, och flickor drabbas oftare än pojkar (3:1). Tumören diagnostiseras oftast prenatalt med ultraljud. De levande födda barnen har i regel bra prognos efter postnatal resektion. Vid mycket stora tumörer finns dock en betydande perinatal mortalitet på 25–50 procent [29].
Tumörerna kan bli gigantiska i relation till fostrets storlek och väga upp mot 1 kg. De är då mestadels solida och innehåller arteriovenösa shuntar med lågresistent flöde som genom »vaskulär stöld« avleder större delen av hjärtats slagvolym och kan leda till hjärtsvikt och hydrops fetalis, vilket ofta blir letalt [30, 31].
Obstetriska komplikationer drabbar en majoritet av graviditeterna i form av polyhydramnios, dystoci eller tumörruptur vid partus [29].
Sakrokoccygealt teratom bör monitoreras noggrant under graviditeten med täta ultraljudskontroller vid enhet med vana att handlägga dessa komplicerade graviditeter och tillgång till barnkirurger. Foster med hydrops fetalis kan dekompensera fort, och intervention eller förlossning bör ske innan hydrops inträffar. Tumörreducerande operationer med öppen fosterkirurgi vid hydropsutveckling före 30 graviditetsveckor har gjorts på enstaka högspecialiserade centrum i USA, med 50 procents överlevnad [31].
Vid hjärtinkompensation och hotande hydropsutveckling senare i tredje trimestern rekommenderas kejsarsnitt och postnatal excision [32]. Det finns även enstaka rapporter om minimalinvasiv intervention genom sklerosering av tumörens kärlförsörjning med injektion av alkohol eller laserbehandling [33], men risker finns för död eller organskada som följd av ischemi, nekros eller embolisering.
Framtiden
Artificiell placenta. Det har skett betydande framsteg med förbättrade resultat i neonatalvården av extremt prematurfödda barn (<28 graviditetsveckor) under de senaste årtiondena. En möjlig framtida utveckling för de barn som föds före 24 veckor kan vara användande av konstgjord placenta och behållare, som försörjer barnet under ytterligare några veckor och minskar risken för komplikationer förknippade med extrem prematuritet. Olika försök till extrakorporeala livsuppehållande system har testats på prematura djur med varierande framgång de senaste 50 åren. Traditionella artificiella placentor har baserats på arteriovenösa ECMO-system med hjälp av navelsträngen eller infart via halskärlen.
På senare tid har den tekniska utvecklingen med bl a miniatyrisering av ECMO-komponenter och en konstgjord »biobag« visat sig ha potential för att skapa en mer fysiologisk extrauterin miljö. Även om många tekniska utmaningar kvarstår är den experimentella forskningen kring den konstgjorda placentan högintressant, och behandlingen kan bli möjlig i framtiden [34].
Stamcellsterapi. Flera olika studier pågår i världen för att utvärdera prenatal stamcellsterapi till foster som behandling för ett flertal medfödda sjukdomar, bl a immunbristsjukdomar och hemoglobinopatier. Ett exempel på kliniska studier av stamcellsterapi är BOOSTB4 (www.boostb4.eu), en europeisk studie som har till syfte att utvärdera säkerhet och effekt vid prenatal och postnatal transplantation av fetala mesenkymala stamceller vid svåra former av osteogenesis imperfecta. Studien har finansiering från EU:s Horizon 2020-program och koordineras från Karolinska institutet i Stockholm.
Konklusion
Fosterkirurgi är i dag ett möjligt behandlingsalternativ för väl selekterade fall av vissa svåra medfödda missbildningar och sjukdomar (Tabell 1). Vid ryggmärgsbråck är fosterkirurgi en etablerad behandlingsform med god vetenskaplig evidens för effektivitet. Dock är interventionerna förknippade med prematuritetskomplikationer och, vid öppen kirurgi, risk för maternell morbiditet.
Blivande föräldrar till foster med dessa diagnoser har rätt att få korrekt och objektiv information av ett multidisciplinärt team både om att fosterkirurgiska interventioner finns och om dess för- och nackdelar.
EXIT är en livräddande intervention vid förlossning av barn med luftvägshinder. I Sverige finns kompetens för EXIT-operationer och shuntinläggning vid makrocystiska lungmissbildningar samt erfarenhet av stamcellsterapi.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Indikationer för EXIT
CHAOS-syndrom (congenital high airway obstructive syndrome) – larynxatresi
Cervikala tumörer (teratom, lymfatiska missbildningar)
Orofaryngeala tumörer (epignatus, dermoider)
Reversering av iatrogen trakealocklusion efter fosterkirurgi för diafragmabråck
EXIT-till-ECMO
Massiva lungtumörer – CPAM (congenital pulmonary airway malformation; kongenital missbildning av lungvävnaden)
Uttalad bilateral hydrotorax med hydrops fetalis



![Figur 1. 20 veckors foster som opereras för öppet ryggmärgsbråck. Publiceras med tillstånd från Adzick NS [35].](https://lakartidningen.se/wp-content/uploads/EditorialFiles/6E/%5bEM6E%5d/2016-233_1_webb.jpg)