För snart 10 år sedan beskrevs för första gången ett kliniskt syndrom orsakat av autoantikroppar specifika för N-metyl-D-aspartat-receptorn (NMDAR-antikroppar).
NMDAR-antikroppar orsakar den vanligaste limbiska autoimmuna encefaliten.
Av dem som drabbas är 80–90 procent kvinnor, där upp till hälften befinns ha äggstocksteratom.
NMDAR-antikroppar orsakar ett brett syndrom av centralnervösa symtom, med bland annat psykiska symtom, epileptiska anfall, orofaciala och extremitetsdyskinesier, autonom instabilitet och koma.
Utöver kirurgisk behandling av ett eventuellt teratom är behandlingen immunologiskt inriktad.
För snart 10 år sedan beskrevs för första gången förekomst av autoantikroppar specifika för N-metyl-D-aspartat-receptorn (NMDAR-antikroppar) hos fyra unga kvinnor med ett syndrom av minnessvårigheter, psykiatriska symtom, sänkt medvetande och hypoventilation [1]. Samtliga uppvisade ovarieteratom, och syndromet tolkades som ett autoimmunt paraneoplastiskt tillstånd. Den första större fallserien och karaktäriseringen av autoantikropparna publicerades 2008 [2], och 2013 tillkom en fallserie omfattande 577 patienter [3]. Det första svenska fallet beskrevs av oss 2010 [4]. Parallellt med upptäckten av specifika autoantikroppar mot NMDAR har flera andra autoimmuna encefaliter visats bero på immunologisk reaktivitet mot neuronala receptorer för klassiska neurotransmittorer, inkluderande α-amino-3-hydroxi-5-metylisoxazol-4-propansyra-receptorn (AMPAR), γ-amino- smörsyra-B-receptorn (GABAB-R), och leucinrika, gliom-inaktiv 1 (LGI1)-proteinet som är associerat med spänningsberoende kaliumkanaler [5].
I denna artikel presenterar vi sjukdomsbilden hos några av de patienter som under senare tid diagnostiserats med och behandlats för NMDAR-encefalit i Stockholm. Målet är att väcka ökad uppmärksamhet om tillståndet, som med all sannolikhet är underdiagnostiserat, och beskriva våra erfarenheter av utredning och behandling, som i svårare fall kräver avancerad immunterapi.
Fall 0. Indexfall
Den första rapporterade patienten med NMDAR-encefalit, en i dag 56-årig kvinna, togs upp i en fallbeskrivning i Läkartidningen 2010 [4]. Hon insjuknade sommaren 2009 subakut med personlighetsförändring med psykotiska drag och utvecklade senare epileptiska manifestationer. Patienten återinsjuknade hösten 2010, men svarade bra på tidigt insatt behandling med kortison och intravenöst immunglobulin. Behandling med azatioprin initierades, men patienten fick hösten 2011 ett nytt skov och påbörjade då halvårsvis behandlig med rituximab, varefter tillståndet har varit stabilt. Detta belyser att NMDAR-encefalit kan vara ett recidiverande autoimmunt tillstånd, som kräver kronisk immunsuppression, men att prognosen för återhämtning vanligtvis är god.
Fall 1–3
Detta rör tre yngre kvinnor i åldrarna 19–25 år, som alla insjuknade med personlighetsförändring och två med uttalade psykosliknande symtom. För samtliga patienter ställdes diagnosen efter att epileptiska anfall uppkommit under pågående psykiatrisk vård, vilket föranledde överföring till neurologisk klinik. Ingen av patienterna utvecklade status epilepticus eller hade behov av intensivvård. Testning för NMDAR-antikroppar påvisade låga, men positiva titrar i såväl serum (1:10–1:200) som cerebrospinalvätska. Magnetkameraundersökning av hjärnan var hos två utan avvikelse och hos den tredje patienten sågs diskret signalökning i den ena tinningloben. Alla hade lätt ökade celltal i likvor (6–20 celler/106/l). Hos en kvinna hittades med magnetkameraundersökning ett ovarieteratom som avlägsnades kirurgiskt. Samtliga patienter gavs behandling med intravenösa kortikosteroider i hög dos. Alla fick intravenöst immunglobulin och/eller plasmaferes samt rituximab i akutskedet, vilket ledde till klinisk förbättring inom någon eller några veckor, även om kognitiva problem med minnessvårigheter kvarstod under många månader. En av kvinnorna hade haft en misstänkt encefalit 2004, som då tolkades som orsakad av Bartonella (»kattklössjuka«) på bas av serologiska fynd och hade behandlats med doxycyklin, högdos kortikosteroider och intravenöst immunglobulin. Hon förbättrades men kvarstod på antiepileptika under flera år och hade kvarvarande kognitiva svårigheter. Enligt föräldrarna liknade symtombilden 2004 det aktuella insjuknandet och vår bedömning är att hon då sannolikt hade ett första skov. En av de andra kvinnorna hade vårdats för en misstänkt psykos 2012.
Fallbeskrivningarna belyser att sjukdomstillståndet kan ge förhållandevis lindriga symtom, som svarar prompt på behandling, och att skov kan förekomma, ibland med många års mellanrum. Ingen av patienterna har fått nytt skov. Alla har behandlats med rituximab med 6 månaders mellanrum, vilket kommer att glesas ut med tiden.
Fall 4
Fallet rör en 23-årig kvinna med ursprung från Fjärran Östern som insjuknade under hösten 2013 med huvudvärk och förkylningssymtom och observerades 24 timmar på sjukhus för ett misstänkt krampanfall. Hon försämrades snabbt inom loppet av någon vecka med tillkomst av frossa och kräkningar, orofaciala dyskinesier, riklig salivation och personlighetsförändring med misstänkt synhallucinos, paranoida vanföreställningar, utagerande och våldsamt beteende. Hon överfördes från psykiatrin till somatisk vård efter ett generaliserat krampanfall. NMDAR-antikroppar i serum var positiva i en titer på 1:100, och man fann en uttalad cellstegring i cerebrospinalvätska (190 celler/106/l). Tillståndet försämrades trots högdos kortikosteroider, intravenöst immunglobulin och rituximab, med behov av sövning med invasiv ventilation. Trots upprepad plasmaferes visade förnyad testning extremt höga NMDAR-antikroppstitrar (>1:100 000 i serum och >1:500 i cerebrospinalvätska). Magnetkameraundersökning visade på ett polycystiskt ovariesyndrom.
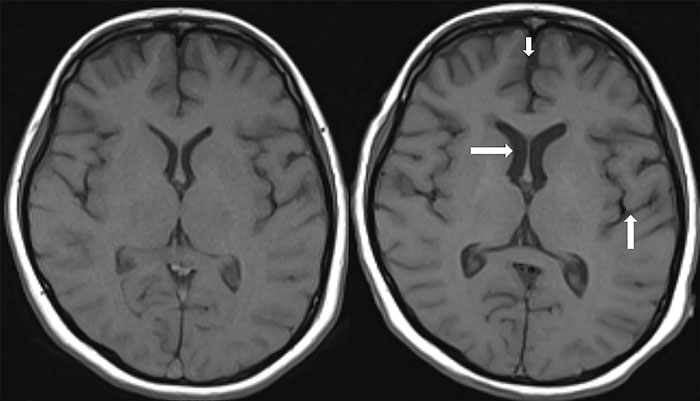
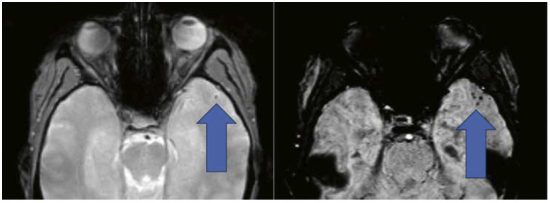
På grund av det livshotande tillståndet beslutades om bilateral ooforektomi, men i den histopatologiska undersökningen kunde inte teratom påvisas. Datortomografi av torax/buk samt helkropps-PET var utan avvikelser. Magnetkameraundersökning av hjärna var initialt utan avvikelser, men patienten utvecklade med tiden frontotemporal atrofi utan fokala signalavvikelser (Figur 1). Initialt sågs på EEG epileptiform aktivitet och senare djup deltaaktivitet, så kallad delta brush, som föreslagits vara specifikt för detta tillstånd [6]. Behandling med pulskurer cyklofosfamid (750 mg/m2) inleddes och hon erhöll även rituximab intratekalt. På försök testades tocilizumab, som i fallrapporter och en mindre studie uppvisat effekt på neuromyelitis optica [7]. Trots denna behandling kvarstod tillståndet kliniskt oförändrat, med mycket höga NMDAR-titrar. Behandling med bortezomib, ett läkemedel mot myelom som slår ut plasmaceller och därmed skulle kunna ha gynnsamma effekter vid terapiresistent autoantikroppsmedierad sjukdom [8], inleddes och gavs som fyra veckovisa kurer. Omkring sex veckor senare började tillståndet stabiliseras och patienten har därefter fortsatt förbättras, så att hon nu har kunnat överföras till neurorehabiliteringsvård.
Total tid på intensivvårdsavdelning med behov av sövning och invasiv ventilation har uppgått till sju månader, vilket patienten har klarat häpnadsväckande väl utan komplikationer som till exempel neuropati och myopati i samband med intensivvård, möjligen på grund av pågående ofrivilliga rörelser i extremiteterna. Under hela förloppet har axonalnervskademarkören NFL (neurofilament light subunit) monitorerats i cerebrospinalvätska. Nivåerna nådde som högst ett värde på drygt 20 000 ng/l fyra månader efter insjuknandet, för att senare sjunka till 2 000–7 000 ng/l, vilket representerar förhållandevis låga nivåer med tanke på tillståndets allvarlighetsgrad. Nivåerna av tau-protein och GFAP (glial fibrillary acidic protein) har legat i stort sett normalt under hela förloppet. Intressant nog har en japansk fallbeskrivning visat att en initialt uttalad frontotemporal hjärnatrofi vid detta tillstånd med uppföljning över flera år kan gå i regress [9].
Fallet belyser att NMDAR-encefalitspektrum inkluderar oerhört svår och terapiresistent sjukdom, men att graden av nervskadande inflammation efter omständigheterna är relativt lindrig. Användningen av bortezomib saknar stöd i pulicerad klinisk litteratur, men resultatet i detta fall gör att behandlingen möjligen kan övervägas när behandling med rituximab och pulskurer cyklofosfamid inte har haft tillräcklig effekt.
Fall 5
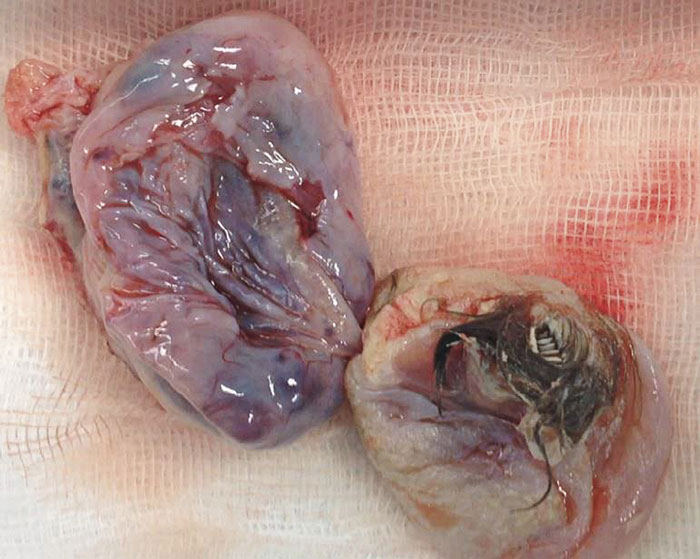
Vårt femte fall rör en nu 20-årig kvinna som 2014 under några få dagar insjuknade med ångest och oro. I anamnesen fanns tidigare kontakt med beroendevården. Tillståndet försämrades med utagerande och delvis våldsamt beteende och hörselhallucinos, som initialt misstänktes för en psykos, eventuellt drogutlöst. Hon intogs i psykiatrisk tvångsvård, men överfördes till somatisk intensivvård efter ett generaliserat krampanfall och medvetandesänkning. Lumbalpunktion visade på en kraftig cellstegring (250 celler/106/l), och på EEG sågs generell deltaaktivitet, medan magnetkameraundersökning av hjärna var utan avvikelser. NMDAR-titrarna var kraftigt förhöjda i såväl serum (1:10 000) som cerebrospinalvätska. Datortomografi av lilla bäckenet visade ett vänstersidigt äggstocksteratom, vilket avlägsnades laparoskopiskt inom två veckor från initialt insjuknande (Figur 2). Hon erhöll initialt behandling med intravenöst immunoglobulin, rituximab, högdos kortikosteroider och plasmaferes. Härefter inleddes behandling med pulskurer cyklofosfamid. Titrarna i serum sjönk till 1:100.
Kliniskt har patienten förbättras långsamt. Hos denna patient förelåg initialt en uttalad autonom dysfunktion, med episoder av bradykardi/asystoli upp till 20 sekunder, som föranledde anläggande av extern pacemaker och behandling med antiepileptika i hög dos. Patientens sjukhistoria belyser ytterligare ett svårt fall av NMDAR-encefalit, med snabb initial försämring, där även autonom dysfunktion förekommit som kan leda till potentiellt livshotande arytmier. Fallbeskrivningar har rapporterat att sådana asystoliepisoder är förknippade med epileptisk EEG-aktivitet och bör föranleda noggrann monitorering och insättning av adekvat antiepileptisk medicinering [10]. Vid svåra fall av NMDAR-encefalit med potentiellt livshotande autonom instabilitet bör intensiv behandling med cyklofosfamid övervägas på ett tidigt stadium utöver rituximab.
Epidemiologi och tumörassociation
Den exakta incidensen av NMDAR-encefalit är fortfarande oklar, men den utgör sannolikt den vanligaste limbiska autoimmuna encefaliten [11]. Uppskattningsvis 80 procent är kvinnor, varav 40–50 procent har en tumör, men med vissa skillnader avseende ålder, kön och etnisk bakgrund [2, 12]. Kopplingen till teratom är mycket stark, och denna tumörform utgjorde 98 procent i ett stort material om 400 patienter [13]. I en histologisk undersökning av 25 äggstocksteratom visade samtliga uttryck av NMDAR [14]. Screening för äggstocksteratom ska därför göras på samtliga kvinnliga patienter där NMDAR-encefalit kan misstänkas. Magnetkameraundersökning har högst känslighet för att upptäcka eventuella teratom [13]. Hos vissa patienter har exploratorisk laparoskopi och borttagning av äggstockar visat mikroteratom, som inte kunnat detekteras vid radiologisk screening [2, 15]. Upprepad screening för äggstocksteratom bör därför övervägas under några år vid uppföljning av patienter där initial screening utfallit negativ [16].
Kliniska symtom
Antikroppar mot NR1-subenheten av NMDAR är associerade med ett karaktäristiskt kliniskt syndrom som utvecklas i olika stadier. Över hälften av patienterna har en prodromalfas med influensaliknande symtom någon vecka innan insjuknandet. Därefter följer en fas med fluktuerande psykiatriska symtom, där ångest, sömnlöshet, rädsla, stereotypa beteenden, vanföreställningar, mani, och paranoida vanföreställningar är vanliga. En majoritet av patienterna bedöms initialt av en psykiater [2]. Hos yngre barn är det vanligt med ångest, vredesutbrott, sömnsvårigheter och hyperaktivitet utan tecken till psykos, som är vanligare hos äldre. Störningar i korttidsminne och annan kognitiv dysfunktion är vanliga, men kan döljas av de psykiatriska symtomen [2]. Talstörningar innefattande allt från minskat verbalt flöde och ekolali (oftast med ekopraxia) till stackatotal och stumhet är vanliga.
I den följande fasen tillkommer mer uttalade neuropsykiatriska manifestationer med växlande agitation och katatoni samt rörelsestörningar med karaktäristiska orofaciala dyskinesier. Även koreoatetos, okulogyr kris, dystoni, stelhet, och opistotonus kan förekomma [13]. Epileptiska anfall kan också uppkomma i detta stadium av sjukdomen. Att skilja onormala rörelser ifrån epileptiska anfall kan vara kliniskt svårt eftersom de kan feltolkas, och behandling med antiepileptika är då verkningslös [17].
Ett intressant och vanligt förekommande fenomen är dissociativa reaktioner på yttre stimuli. Till exempel att patienten motstår öppning av ögonlocken, men samtidigt uppvisar liten eller ingen reaktion på smärtsamma stimuli [18]. Detta dissociativa tillstånd liknar det som orsakas av NMDAR-antagonister (dissociativa anestetika), såsom ketamin och fencyklidin [18, 19]. Med fortsatt försämring följer också tecken till autonom dysreglering, med hypertermi, brady-/takykardi, hyper-/hypotension och hypersalivation [2]. Hypoventilation kan även förekomma innan patienten blir medvetslös och kräva andningsunderstöd. Detta gör också att urträning från mekanisk ventilation kan ta tid trots att patienten förefaller vaken. Symtom på autonom dysfunktion är viktiga att uppmärksamma, eftersom de kan leda till livshotande kardiovaskulär/respiratorisk påverkan (se fall 5 ovan).
Diagnostiska test
Antikroppsanalys ska helst utföras både i serum och i cerebrospinalvätska, där det senare förefaller ha störst prognostisk betydelse [3]. I vissa fall, och särskilt efter behandling, förekommer att antikropparna kan påvisas i cerebrospinalvätska, men inte i serum [12].
Magnetkameraundersökning av hjärnan utfaller hos omkring hälften av dessa patienter normalt [2]. I de fall avvikelser kan noteras är det vanligen i form av ökad signal i hippocampi, lillhjärnan, hjärnbarken eller basala ganglierna på T2- eller FLAIR (fluid attenuated inversion recovery)-viktade bilder [20].
EEG är avvikande hos en överväldigande majoritet av patienterna, vanligen i form av generell, ospecifik, långsam och desorganiserad aktivitet, ibland med epileptisk aktivitet eller anfallsaktivitet [2]. En för tillståndet mer specifik avvikelse är en långsam, kontinuerlig, rytmisk aktivitet i delta-theta-regionen. Detta ses ofta när patienten har rikligt med ofrivilliga rörelser eller befinner sig i ett katatoniskt/dissociativt tillstånd [12]. Avvikelsen kan i svårare fall accentueras så att patienten utvecklar djup deltaaktivitet, »delta brush« [6].
Avvikelser i cerebrospinalvätska noteras hos 80 procent av patienterna initialt, och andelen ökar senare i sjukdomsförloppet [2]. Oftast hittar man en lätt till måttlig cellstegring med övervikt för mononukleära lymfoida celler och lätt ökad proteinkoncentration. I drygt hälften av fallen finns det cerebrospinalvätske specifika oligoklonala band. Alla patienter ska uppvisa intratekalt detekterbara nivåer av NMDAR-antikroppar [2].
Patogena mekanismer och antikropparnas roll
Det finns övertygande kliniska och laboratoriemässiga bevis för att NMDAR-antikroppar är sjukdomsframkallande [2]. Som nämnts ovan korrelerar antikroppstitrar, främst i cerebrospinalvätska, med klinisk svårighetsgrad och prognos där låga nivåer orsakar psykos, oro, minnesstörningar och minskad känslighet för smärta, och vid högre nivåer ses ofrivilliga rörelser, dissociativ anestesi och ett tillstånd av okänslighet för stimuli, katatoni och koma [13]. Detta tillstånd uppvisar flera likheter med missbruk av NMDA-receptorantagonisterna ketamin eller fencyklidin, som kan ge onormala orofaciala och extremitetsrörelser, autonom instabilitet och epileptiska anfall [18, 21], och är analogt med experimentella djurstudier [19, 22].
Tillståndets reversibilitet, oavsett hur länge symtomen har pågått, talar för en immunmedierad neuronal dysfunktion i stället för en irreversibel skada (degeneration). Detta tillsammans med avsaknad av T-cellinfiltrat skiljer denna sjukdom från klassiska former av paraneoplastiska encefaliter, som i större utsträckning medieras av komplement och cytotoxiska T-cellssvar mot intracellulära neuronala antigener [13].
Behandling
Behandlingen är immunologiskt inriktad, utöver kirurgisk exstirpation av ett eventuellt teratom (se Fakta 1). Första linjens immunterapi består av högdos kortikosteroider, intravenöst immunglobulin och/eller plasmaferes. Andra linjens immunterapi innefattar främst rituximab och/eller cyklofosfamid. Om patientens tillstånd försämras under de första veckorna trots behandling och/eller om antikroppstitrarna är höga, bör andra linjens behandling övervägas på ett tidigt stadium. En ännu obesvarad fråga är vilken roll andra linjens behandling, främst rituximab, har för att minska recidivrisken på längre sikt hos patienter som svarat bra på initial terapi. Utifrån de patienter som presenteras här är det uppenbart att sjukdomen kan gå med upprepade skov, åtminstone i fall där teratom inte påträffas.
Med erfarenhet av vår först beskrivna patient har vår inställning varit att behandla alla tidigt med andra linjens immunterapi för att konsolidera behandlingssvar och minska risken för återfall. Även om prognosen för återhämtning är god, är tillståndet plågsamt för patient och anhöriga, och neurokognitiv återhämtning kan ta lång tid. I avvägningen mellan risk och nytta förefaller rituximab i monoterapi vara ett enkelt och förhållandevis ofarligt läkemedel i detta sammanhang. Uppföljande studier behövs för att försöka fastställa om uppföljande rituximabbehandling är motiverad och vilka patienter som är i behov av sådan behandling.
Återhämtningsfasen
Återhämtningen från NMDAR-encefalit sker i omvänd ordning jämfört med hur sjukdomen initialt utvecklats. Sålunda vaknar patienten långsamt ur sin medvetandesänkning, autonoma funktioner börjar stabiliseras, andningen återhämtar sig och dyskinesierna minskar. Patienterna kan börja följa enkla uppmaningar innan någon språklig förmåga kommer i gång. Under denna period kan de ha intermittenta psykotiska symtom och vara affektlabila. Det tar lång tid för socialt beteende och högre kognitiva funktioner att återhämta sig och stundom blir återhämtningen aldrig helt fullständig. De flesta patienter behöver en längre tid med fysisk och inte minst kognitiv rehabilitering samt noggrann uppföljning av sin epilepsi, om sådan förekommer [2, 12]. Återfall förekommer hos cirka en fjärdedel av patienterna [2, 12]. De kan vara åtskilda i intervall på enstaka månader till flera år, dock vanligtvis med väsentlig återhämtning mellan skoven.
Spontan neurologisk förbättring har rapporterats, men den sker dock sannolikt till priset av längre sjukhusvistelse och långsammare återhämtning. I Japan kunde man identifiera NMDAR-antikroppar från 4–7 år gamla sparade prov [16]. Trots brist på konsekvent immunterapi eller tumörborttagning uppvisade tre patienter en gradvis återhämtning, medan en avled.
I tidigare nämnd fallserie på 577 patienter återhämtade sig 81 procent väl (modifierad Rankinskala, mRS, 0–2), och 5 procent dog [3]. Där såg man tydligt att andra linjens behandling medförde bättre prognos hos de patienter som inte svarade på initial terapi. Tidig behandling var också en positiv prognostisk faktor.
Sammanfattning
NMDAR-encefalit utgör en av de vanligaste orsakerna till autoimmun encefalit, där de initiala symtomen är utpräglat neuropsykiatriska och kan misstolkas som någon ren psykisk sjukdom. Samtliga patienter vi har kännedom om hade initialt haft kontakt med psykiatrin. Kännedom om tillståndet och korrekt diagnostik är nödvändig för att orsaksinriktad behandling ska kunna initieras. Tillståndet kan vara livshotande till följd av autonom påverkan på hjärta och andning, vilket motiverar noggrann monitorering.
Som belyses av de patienter som här presenteras, bör NMDAR-encefalit misstänkas hos framför allt yngre personer som inom loppet av dagar eller veckor utvecklar personlighetsförändring med psykotiska eller gränspsykotiska drag. Neurologiska sjukdomstecken kan initialt vara subtila, men inkluderar i senare faser för tillståndet typiska rörelsestörningar, där orofaciala- och extremitetshyperkinesier är mest karaktäristiska, samt även epileptiska manifestationer. Diagnosen kan fastställas med påvisning av NMDAR-antikroppar i serum och cerebrospinalvätska. I några av våra fall har antikroppsnivåerna varit låga, och förnyad testning kan bli nödvändig. Stöd för diagnosen ges av fynd av lindrig–måttlig cellstegring och/eller oligoklonala band i cerebrospinalvätska och EEG med långsam, oorganiserad, ibland rytmisk aktivitet som inte korrelerar med dyskinesierna. För initial behandling har högdoskortikosteroider samt intravenöst immunglobulin/plasmaferes använts i de publicerade fallserierna. Det är för närvarande inte fastställt om intravenöst immunglobulin eller plasmaferes är mest effektivt vid behandling av NMDAR-encefalit, men plasmaferes förefaller vara en effektivare behandling vid steroidresistenta skov av demyeliniserade sjukdom [23].
Det är viktigt att utesluta och avlägsna ovarieteratom i förekommande fall, och om initial screening är negativ bör upprepade kontroller övervägas. För närvarande saknas stöd för kronisk immunsuppression. Patienten i vårt indexfall uppvisade regelbundna skov fram tills behandling med rituximab inleddes och vi har därför valt att ge denna behandling till samtliga patienter. Initialt har behandlingsintervallet varit 6 månader, men avsikten är att successivt glesa ut intervallen, särskilt i de fall där ett bakomliggande teratom har avlägsnats. Fortsatt uppföljning är viktig för att vinna ny kunskap om hur behandlingen bör läggas upp långsiktigt. Orsaken till NMDAR-encefalit utan association till teratom är i dag okänd. Ett intressant observandum är att tre av våra patienter har en genomgången eller kroniskt aktiv hepatit B- eller C-virus-infektion, vilket skulle kunna indikera en relevant miljöfaktor. Det är fortfarande oklart om det ökande antal patienter vi diagnostiserat under senare tid beror på ökad medvetenhet om tillståndet, eller om incidensen har ökat.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Behandlingsalternativ vid NMDAR-encefalit
Första linjens behandling
Kortikosteroider, t ex Solu-Medrol, 1 g intravenöst i 5 dagar
Plasmaferes fem gånger varannan dag
Intravenöst immunoglobulin, t ex Privigen, 2 g/kg uppdelat på 3–5 dagliga doser
Andra linjens behandling
Rituximab (Mabthera) 1 000 mg intravenöst, eventuellt med upprepning efter sex månader
Cyklofosfamid (Sendoxan) 750 mg/m2 en gång i månaden under sex månader eller tills påtaglig klinisk effekt uppnås