Immunterapibehandlingar med immunkontrollpunktshämmare har blivit godkända för flera olika cancerformer. Tusentals patienter erhåller nu onkologisk immunterapi årligen i Sverige.
Biverkningar av immunkontrollpunktshämmare är oftast lindriga men kan bli mycket allvarliga eller till och med dödliga. Tidig och korrekt diagnostik, rätt handläggning och multidisciplinärt samarbete är avgörande.
I två artiklar ges en översikt över de vanligast förekommande immunrelaterade biverkningarna. Denna, den andra delen, är inriktad på dermatologiska, endokrinologiska och reumatologiska biverkningar.
I två artiklar ges en översikt över de vanligaste immunrelaterade biverkningarna relaterade till onkologisk immunterapi med CTLA-4-, PD-1- eller PD-L1-hämmare. I den första delen är fokus på biverkningar som kan uppstå i gastrointestinala organ, lungor och njurar.
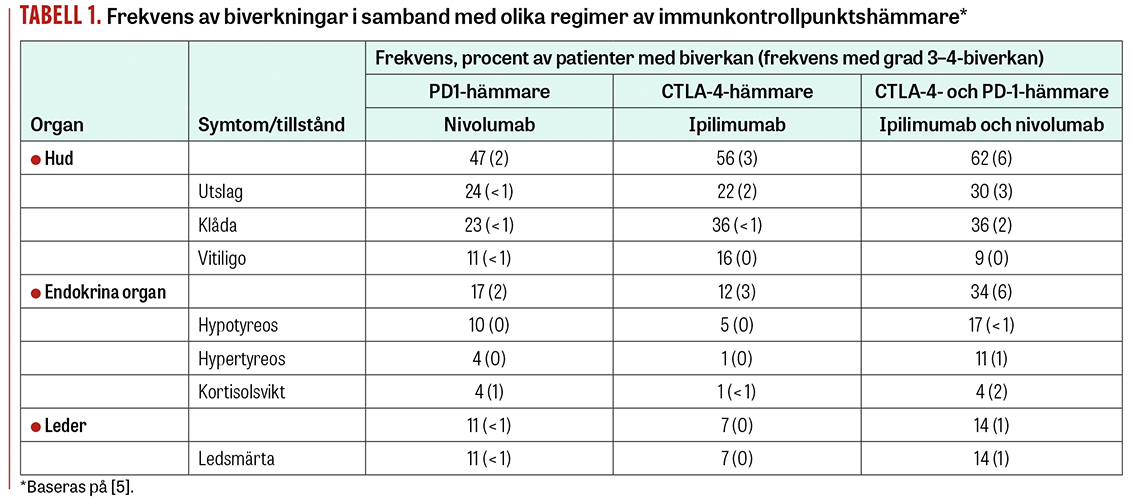
Denna, den andra delen, är inriktad på dermatologiska, endokrinologiska och reumatologiska biverkningar. Handläggningarna som beskrivs följer rekommendationer från European Society for Medical Oncology (ESMO), American Society for Clinical Oncology (ASCO) samt svenska riktlinjer som finns tillgängliga på webbplatsen för Regionala cancercentrum (RCC) [1-3]. Biverkningarna graderas enligt etablerade kriterier (Common terminology criteria for adverse events [CTCAE], version 5) (Tabell 1) [4, 5]. I faktarutorna återfinns beskrivande förlopp.
Hudbiverkningar
Hudbiverkningar (Fakta 1) är vanligt förekommande vid behandling med immunkontrollpunktshämmare (»checkpointhämmare«) och kan ses hos hälften eller fler av patienterna (Tabell 1) [5].
Hudbiverkningar debuterar ofta tidigt men kan även uppkomma efter behandlingsavslut. Utslag av makulopapulär typ och klåda är den vanligaste typen, följd av vitiligo. Lichenoida reaktioner och psoriasis förekommer också, liksom i sällsynta fall även blåsdermatoser som bullös pemfigoid (Figur 1, bild A). Även om bullös pemfigoid inte är den vanligaste immunrelaterade hudbiverkningen, så är incidensen signifikant förhöjd jämfört med normalbefolkningen, där blåsdermatoser är mycket ovanliga.
Hudbiverkningar är i majoriteten av fallen lindriga (grad 1–2). Utslag och klåda graderas utifrån hudutbredningen: <10 procent av hudytan (grad 1), 10–30 procent av hudytan (grad 2), >30 procent av hudytan (grad 3) (Figur 1, bild B) [4]. Graderingen utgår även från typ av hudbiverkan: till exempel motsvarar blåsdermatoser på >30 procent hudytan med elektrolytrubbning grad 4 [4].
Dermatologbedömning och eventuell hudbiopsering bör ske tidigt i förloppet samt före behandlingsstart vid känd hudsjukdom som psoriasis, då det finns en risk för försämring vid immunterapi. Lokalbehandling med mjukgörare, lokala steroider (grupp II–IV) och antihistaminer brukar ge god effekt. Insättning av steroider (0,5–1 mg prednisolon/kg × 1) och uppehåll i behandlingen med immunkontrollpunktshämmare tills hudsymtomen förbättras bör övervägas vid hudbiverkningar grad 2–3. Byte från steroider till annan immunmodulerande terapi bör övervägas vid försämring av hudbiverkningar. Alarmsymtom för allvarliga hudbiverkningar inkluderar progredierande hudbiverkningar, blåsor i hud och/eller slemhinnor, hudavlossning och/eller smärta i huden samt allmänpåverkan med eller utan organpåverkan.
Mycket allvarliga hudbiverkningar (SCAR, severe cutaneous adverse reactions) som Stevens–Johnsons syndrom/toxisk epidermal nekrolys eller DRESS (drug reaction with eosinophilia and systemic symtoms) är mycket sällsynta, men de bedöms som uttalade redan vid <10 procents hudengagemang (grad 3) och mycket uttalade vid 10–30 procents påverkan av hudytan (grad 4) [4]. Inläggning och intravenöst metylprednisolon 2 mg/kg × 1 ska alltid initieras vid SCAR. Patienterna behöver då omedelbar och multidisciplinär handläggning.
Endokrinologiska biverkningar
Endokrinologiska biverkningar av immunkontrollpunktshämmare (Fakta 2) är relativt vanliga och drabbar upp mot en tredjedel av patienterna (Tabell 1) [5].
Den vanligaste endokrinologiska biverkan är tyreoidit, som i början ofta kännetecknas av en initial kortvarig fas med hypertyreos (högt fT3/fT4 och lågt TSH) som sedan normaliseras alternativt övergår i en ofta permanent hypotyreos (lågt fT3/fT4 och högt TSH). Den bakomliggande orsaken är att aktiverade T-celler angriper sköldkörtelvävnaden, vilket initialt leder till en utsvämning av sköldkörtelhormoner för att sedan ofta övergå i minskad produktion. Hypertyreosen är oftast asymtomatisk eller lindrig och behöver då ej behandlas; betablockad kan i vissa fall ges för att lindra hjärtklappning. I sällsynta fall av grad 3–4-hypertyreos ska högdos steroider och tyreostatika övervägas. Vid overt hypotyreos behöver levotyroxin ofta sättas in, till att börja med i låga doser som sedan oftast behöver trappas upp. Patienter med tyreoidit kan som regel skötas i öppenvård. Behandlingsutsättning eller kortikosteroider rekommenderas inte vid sköldkörtelbiverkan grad 1–2, då sköldkörtelhormonbrist oftast kvarstår oavsett.
Hypofysit är en ovanligare men välkänd biverkan (Tabell 1). Inflammationen leder till olika grader av hypofyshormonsvikt och mer sällan symtomframkallande hypofysförstoring (huvudvärk, synpåverkan). Tidigt i förloppet har patienterna ofta vaga och diffusa symtom, som huvudvärk, trötthet, svaghet, illamående och yrsel, men oupptäckt förvärras dessa successivt och ACTH-brist kan kulminera i en livshotande binjurebarkskris. Tidig diagnos och snabb handläggning är därför vitalt. MR hypofys rekommenderas i utredningen men får ej fördröja behandling. Högdos steroider rekommenderas om patienten har uttalade symtom, framför allt på hypofysförstoring (kraftig huvudvärk, synpåverkan). Misstänkt ACTH-svikt behandlas skyndsamt med peroralt eller intravenöst hydrokortison, beroende på kliniskt status. Patienter med grad 3–4-symtom kräver som regel sjukhusvård, då vitalparametrar behöver övervakas och vätska tillföras. Intorkning, hypotoni och hyponatremi är vanligt förekommande. Vid grad 1–2-symtom kan patienten i stället handläggas polikliniskt. Förutom hydrokortisonsubstitution ges levotyroxin vid TSH-svikt och könshormoner om gonadaxeln ej återhämtar sig på några månader. Gonadaxeln återhämtar sig relativt ofta, medan ACTH-bristen vanligtvis blir bestående. Immunterapin ska avbrytas i det akuta läget men kan återupptas när patienten stabiliserats.
Endokrinologiska biverkningar sköts tillsammans med endokrinolog. Detta gäller även vid mindre vanliga endokrinologiska biverkningar som primär binjurebarkssvikt, insulinberoende diabetes mellitus och hypoparatyroidism.
Reumatologiska biverkningar
Reumatologiska biverkningar har rapporterats hos upp mot 15 procent av patienter behandlade med immunkontrollpunktshämmare (Tabell 1). Frekvensen kan dock vara mycket högre; många patienter utvecklar lindriga symtom och biverkningarna kan ofta missas. De kan uppstå tidigt efter insättning av immunterapi och upp till 2 år efter att den har avslutats. De är lika vanliga hos män som hos kvinnor. Det är vanligt med artriter (mono-, oligo- eller polyartrit), myosit, siccasyndrom och reumatisk polymyalgi. Vaskuliter, sklerodermi och systemisk lupus erythematosus har också beskrivits. Utredning via reumatologen innefattar bedömning av symtom, blodprov (som SR, CRP, RF, anti-CCP) och i vissa fall även radiologiska undersökningar (som MR och ultraljud).
Reumatologiska immunterapirelaterade symtom kan skilja sig från klassiska reumatologiska sjukdomar, både gällande klinisk fenotyp och behandlingsrespons. Till exempel kan många patienter som utvecklar immunterapirelaterade artriter behöva mycket höga kortisondoser, betydligt högre än vad artritpatienter brukar behöva. Dessutom saknar de flesta patienter autoantikroppar.
Det är också viktigt att understryka att reumatologiska biverkningar oftare blir kroniska jämfört med andra immunterapirelaterade biverkningar, och därför behövs ofta en längre immunsupressiv behandling. Symtomatisk behandling med kortison och konventionella sjukdomsmodifierande antireumatiska läkemedel, såsom metotrexat, sulfasalazin och hydroxiklorokin används relativt ofta.
Vid refraktär inflammation kan biologiska läkemedel användas, till exempel TNF-alfa-hämmare och IL-6-eller CD20-blockad.
Omhändertagande av patienter med reumatiska biverkningar ska skötas multidisciplinärt, med både onkolog och reumatolog.
Multidisciplinärt teamarbete
Vid behandling med immunterapi är det multidisciplinära omhändertagandet av största vikt. Vid multidisciplinär konferens görs en helhetsbedömning av eventuell nytta och risker. Här är det viktigt att väga in samsjuklighet, som autoimmuna sjukdomar som kan öka risken för att utveckla biverkningar. Autoimmuna sjukdomar kan då vara en faktor som bidrar till att en annan behandling väljs. Om ingen annan behandling finns att tillgå brukar immunterapin ges trots autoimmunitet, men patienten behöver då informeras om ökad biverkningsrisk och vårdteamet vara extra vaksamt vid uppföljningen. Transplanterade patienter bedöms däremot, på grund av risken för organavstötning, i regel ej vara kandidater för immunterapi. Även annan samsjuklighet vägs in för att bedöma om patienter tros orka med behandlingen och ha resurser för att hantera eventuella biverkningar.
Kontaktsjuksköterskan har en viktig roll i att utbilda patienten, de närstående och andra vårdgivare avseende immunterapi och dess biverkningar [6]. Informationen till varje patient behöver vara individanpassad, och eventuella stödinsatser ska sättas in vid behov för att patienten ska kunna fullfölja sin behandling enligt plan. Patienten bör även få skriftlig information om behandlingen, inklusive biverkningar, samt kontaktuppgifter till mottagningen att förvara i väskan eller plånboken för att vid behov kunna visa upp i kontakt med sjukvård. Patienterna ska instrueras att kontakta sin kontaktsjuksköterska utan dröjsmål även vid relativt lätta symtom för bedömning av om dessa ska undersökas närmare och behandlas.
Ett proaktivt förhållningssätt är avgörande för att minska risken för svårare biverkningar och möjliggöra att patienten ska kunna fortsätta sin behandling. Bedömningen grundar sig på kontinuerlig uppföljning där bedömning av symtom och blodprov rekommenderas inför varje ny behandling.
Att patienten känner sig delaktig och trygg med samarbetet i teamet är en viktig förutsättning. Hantering av biverkningarna behöver därför vara ett teamarbete mellan patienten, kontaktsjuksköterskan, den behandlande läkaren och vid behov andra specialister. På Karolinska universitetssjukhuset har även införts ett multiprofessionellt fallbaserat utbildningsforum som äger rum en gång per månad, där olika immunrelaterade biverkningar diskuteras. Genom denna samverkan byggs samlad kunskap upp, och ett nätverk har bildats med specialister inom bland annat onkologi, dermatologi, endokrinologi, reumatologi, gastroenterologi, nefrologi och radiologi som är inriktade på dessa biverkningar.
Diskussion
Detta är den andra av två artiklar om immunrelaterade biverkningar. Sådana biverkningar kan förekomma i flera olika organ och vävnader.
I dessa två artiklar har de vanligast förekommande biverkningarna beskrivits, men det ska understrykas att det även finns andra sällsynta men allvarliga biverkningar, till exempel kardiella, neurologiska och hematologiska biverkningar. Det ska även poängteras att många patienter mår bra under behandling och inte har några nämnvärda biverkningar. Förekomst av biverkningar är dock något som, intressant nog, är associerat med ett bättre behandlingssvar, vilket är logiskt, då immunbiverkningar är en indikation på att en aktivering av immunsystemet har skett.
Hos cancerpatienter finns det ofta flera indikationer för behandling med kortikosteroider, till exempel smärta och illamående, och om insättning övervägs är det viktigt att vara medveten om att kortikosteroider kan motverka immunkontrollpunkthämmarnas effekt. På grund av detta rekommenderas det vid start av immunterapin att patienter inte står på en högre kortikosterroiddos än motsvarande 10 mg prednisolon/dygn för att inte motverka immunaktiveringen. Dock verkar insättning av kortikosteroider för att behandla immunrelaterade biverkningar, det vill säga när immunaktiveringen satts igång, inte minska den antitumorala effekten. En del patienter som får biverkningar behöver stå på höga kortisondoser under en längre tid. Hos dessa är det viktigt att ha i åtanke att biverkningar relaterade till kortikosteroider kan uppstå, som stegrat blodsocker, urkalkning av skelett, förtvining av muskler, viktuppgång samt psykiska besvär. Även här behövs det kunskap och uppföljning för att hjälpa patienterna på bästa sätt.
Det viktigaste budskapet i dessa artiklar är att många cancerpatienter får en bra effekt av immunterapi, men om inte olika biverkningstillstånd behandlas korrekt och i tid kan det få allvarliga följder för patienterna. Det är därför viktigt att det inom läkarkåren finns en baskunskap om immunbiverkningar, då flera specialiteter kan komma att bli involverade i dessa patienter.
Läs även:
Biverkningar i samband med immunterapi mot cancer, Del 1
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Immunterapirelaterad hudbiverkan
En patient som nyligen avslutat 1 års behandling med PD-1-hämmare började känna av nytillkommen ihållande klåda på ryggen. Initialt sågs inga utslag, och han rekommenderades att smörja de kliande områdena 2 gånger per dag med mjukgörande kräm och fick även antihistamintabletter mot klådan. Biverkan bedömdes som grad 1. Efter 2 veckor hade det dock inte skett någon förbättring av klådan, och nu sågs även mindre makulopapulära utslag på bålen. Han fick via onkologen kräm med lokala steroider (grupp II). Det blev dock inte bättre, och han fick liknande små makulopapulära utslag även på armar och ben. Han remitterades till dermatologen som tog biopsi, som visade en bild som vid kronisk inflammation med infiltration av perivaskulära lymfocyter. Med tanke på utslagens utbredning (>30 procent av hudytan) bedömdes biverkan som grad 3. Han förskrevs lokala steroider (grupp III) och förbättrades successivt. Närmaste halvåret har han fortsatt uppföljning hos dermatologen.
FAKTA 2. Immunterapirelaterad hypofysit
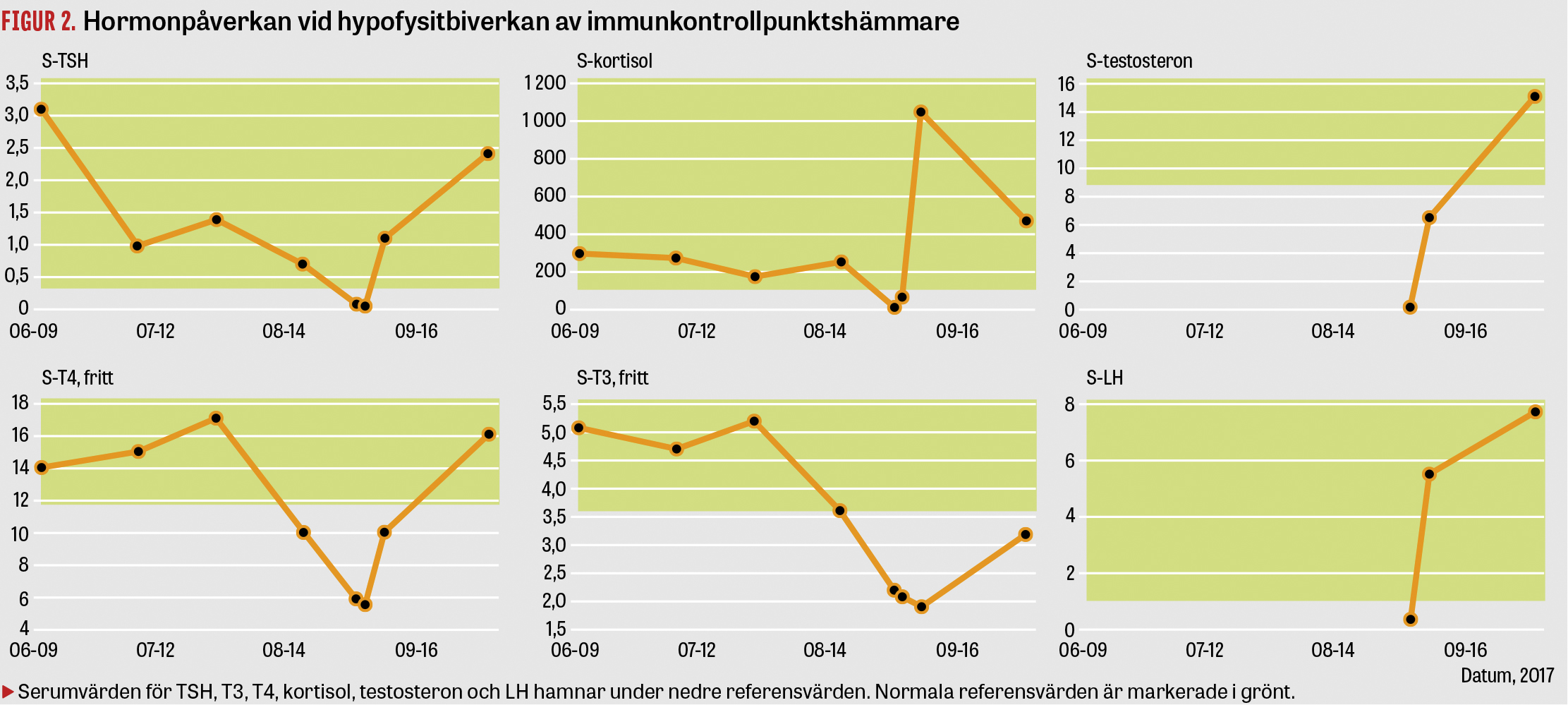
En patient som erhöll PD-1- och CTLA-4-hämmare började efter 3 månader känna av trötthet, huvudvärk och förkylningssymtom. I samband med detta noterades det i blodprov inför kur ett odetekterbart kortisol, lågt TSH, fT3 och fT4 samt hyponatremi. Han uppmanades via onkologmottagningen att söka akut på misstanke om immunterapiutlöst hypofysit. Hypofysit konstaterades, då kompletterande blodprov visade lågt ACTH, LH och testosteron (Figur 2) och MR hjärna visade en lätt förstorad hypofys. Vitala parametrar var stabila, men han lades in för observation och fick natriumkloriddropp och intravenöst metylprednisolon 1 mg/kg × 1. Efter 2 dagar med metylprednisolon skedde i samråd med endokrinkonsult byte till peroralt hydrokortison 30 mg × 2. Patienten förbättrades snabbt och kunde skrivas ut efter en vårdtid på 2 dygn. Vid hemgången ordinerades han tablett levotyroxin 25 µg × 1 och erhöll en testosteroninjektion. MR hjärna 1 månad efter utskrivning visade normaliserad hypofysstorlek. Då hans biverkan bedömdes som grad 3 återupptogs inte immunterapin.
Patienten fick en kvarstående ACTH-brist och står på hydrokortison 10 mg × 2, medan testosteron och levotyroxin har satts ut, då funktionen i TSH och gonadaxel restituerats.
FAKTA 3. Immunterapirelaterad reumatologisk biverkan
En patient som erhöll PD-L1-hämmare började efter 3 månader känna av nytillkomna artralgier och remitterades via onkolog till reumatologmottagning. Patienten bedömdes av reumatolog ha utvecklat en symmetrisk polyartrit med engagemang av handleder, metakarpofalangealleder (MCP), knä- och fotleder. Inflammationsparametrar, SR och CRP var enbart lätt förhöjda, och test för autoantikroppar (reumatoid faktor [RF] och anti-CCP-antikroppar) var negativa. Ultraljudsundersökning av leder visade uttalade synoviter i flera leder, framför allt i handleder och MCP-leder. Prednisolon i måttlig dos (20 mg × 1) sattes in. Patienten kom tillbaka 2 veckor senare och uppgav en signifikant förbättring beträffande ledvärk, svullnad och stelhet. Biverkan bedömdes som grad 2, och han fortsatte med immunterapin. Försök gjordes att trappa ut prednisolon, men artritsymtomen förvärrades varje gång han satte ut det. Ett halvår senare står han därför fortfarande på prednisolon 10 mg × 1.
(uppdaterad 2022-01-26)