Incidensen av dengue ökar globalt. Vid feber och hjärtpåverkan efter resa till endemiskt område bör denguefeber övervägas.
Kardiell påverkan förekommer vid denguefeber och kan i sällsynta fall manifestera sig som livshotande arytmi.
Bradyarytmier vid denguefeber är i regel övergående men kan kräva tillfällig behandling med läkemedel och temporär pacemaker.
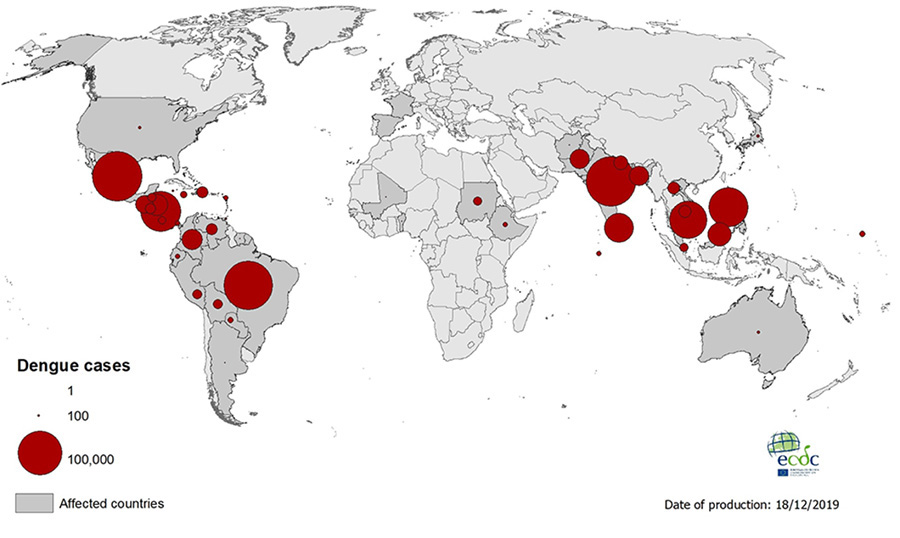
Dengueviruset är ett enkelsträngat RNA-virus ur familjen Flaviviridae, genus Flavivirus, som resulterar i akut och övergående febersjukdom [1]. Viruset sprids mellan människor genom bett av den dagaktiva Aedesmyggan, främst Aedes aegypti (Figur 1). Dengue utgör en ansenlig global sjukdomsbörda då 3,9 miljarder människor i mer än 125 länder lever i endemiskt område, framför allt i Asien (Figur 2). Den årliga incidensen av dengueinfektion uppskattas till 390 miljoner, varav 96 miljoner kliniskt evidenta infektioner [2].
Hjärtengagemang i samband med denguefeber inbegriper ett kliniskt brett spektrum med myokardit, nedsatt ejektionsfraktion och arytmier inklusive atrioventrikulärt block (AV-block) [3]. Ett fall beskrivs (Fakta 1).
Vanligtvis är hjärtpåverkan, inklusive bradyarytmier, övergående, men läkemedel (atropin och isoprenalin), temporär transvenös pacemaker och transkutan pacing kan ibland behöva tillgripas [4-6]. I Sverige smittskyddsanmäls ca 150 denguefall årligen varav majoriteten har smittats i Thailand, följt av övriga Asien, men även ett fåtal individer smittade i södra Europa finns rapporterade [7]. Aedesmyggan förekommer nu på samtliga kontinenter med undantag för Antarktis, och incidensen såväl som den geografiska spridningen av dengue har ökat de senaste 50 åren och fortsätter att öka [8]. Detta tillskrivs bland annat ökad global handel med fordon och däck. Aedes aegypti förökar sig i vattenfyllda behållare, ofta i nära anslutning till hushållen, där regnvattenfyllda uttjänade däck också utgör ett betydande habitat för mygglarverna. I frånvaro av vatten kan dessa larver förbli livsdugliga under många månader, och följaktligen kan vektorn spridas globalt genom internationell däckhandel. Ökat resande, otillräcklig vektorkontroll, höjd global medeltemperatur och urbanisering anses också bidra till dengueinfektionens spridning [9, 10].
Det finns ett vaccin (CYD-TDV, Dengvaxia), som dock har begränsad skyddseffekt och som inte rekommenderas till seronegativa individer på grund av risken för »antibody-dependent enhancement« (se nedan). Resenärer till endemiska områden rekommenderas i stället heltäckande klädsel, myggnät och myggmedel [11].
I en svensk kontext är dengue en differentialdiagnos till febersjukdom efter tropikresa. Man beräknar att en fjärdedel utvecklar symtom, där den vanligaste manifestationen är ett ospecifikt feberinsjuknande. För de 5 procent som utvecklar allvarlig sjukdom föreligger utan behandling en mortalitet över 20 procent, som med korrekt handläggning kan reduceras till mindre än 0,5 procent [2, 12].
Symtom och sjukdomsförlopp
Tidigare talade man om tre olika kategorier av symtomatisk dengueinfektion: denguefeber, hemorragisk denguefeber samt dengue-chocksyndrom. Klassifikationen reviderades 2009 till att i stället innefatta »dengue utan varningstecken«, »dengue med varningstecken« respektive »allvarlig dengue«. Med den modernare klassifikationen hoppas man underlätta tidig identifiering av potentiellt allvarliga sjukdomsförlopp, som kännetecknas av ökad kapillär permeabilitet, plasmaläckage och påföljande hypovolem chock [13].
Inkubationstiden är 4–10 dagar, och sjukdomsförloppet kan indelas i tre faser där den initiala fasen karaktäriseras av plötsligt påkommen feber under 2–7 dagar. Ibland förekommer ett bifasiskt feberförlopp. Under denna fas kan även noteras huvudvärk, illamående, hudutslag, rodnad och muskel- och ledvärk. Dengue kallas även för »breakbone fever« med anledning av just den uttalade led- och muskelvärken [14]. Hepatomegali samt palpationsömhet över levern noteras ofta efter ett par dagars feber, och om torniquettestet (fynd av petekier vid venstas) utfaller positivt anses detta öka sannolikheten för att det febrila tillståndet rör sig om en dengueinfektion. Den tidigaste avvikelsen i laboratoriesvar är vanligen en tilltagande leukopeni, men även stegrade leverenzymer noteras ofta under den febrila fasen [15, 16]. Individer som tillfrisknar efter denna fas bedöms ha »dengue utan varningstecken«. Parallellt med att patientens temperatur börjar normaliseras kan fas 2 inträda. Denna fas benämns den kritiska fasen, varar 1–2 dygn och karaktäriseras av en ökad kapillär permeabilitet, vilket kan monitoreras indirekt genom stegrad hematokrit. Tillståndet benämns »dengue med varningstecken« vid tillkomst av minst ett av följande symtom: buksmärta, kräkningar, slemhinneblödning, rastlöshet eller slöhet, hepatomegali eller hematokritstegring med hastigt påkommen trombocytopeni. Härifrån kan tillståndet regrediera spontant, alternativt progrediera till »allvarlig dengue« som kännetecknas av ett avsevärt plasmaläckage. Detta manifesteras som pleuravätska, ascites eller hypovolem chock med disseminerad intravasal koagulation och blödningssymtom. Vid allvarlig dengue föreligger minst ett av följande:
- plasmaläckage som leder till chock, och/eller vätskeackumulering med eller utan andningspåverkan,
- allvarlig blödning,
- allvarlig organdysfunktion såsom leverpåverkan, påverkan av centrala nervsystemet eller hjärtpåverkan.
Tredje fasen benämns konvalenscensfasen och pågår 1–2 dygn. Denna fas karaktäriseras av stabilisering av tillståndet, avtagande symtom samt resorption av plasma från extravaskulärrummet [13].
Hjärtpåverkan
EKG-avvikelser vid dengue är ofta övergående och ospecifika och inkluderar förmaksflimmer, ST-segmentförändringar och bradyarytmier inklusive AV-block [4, 5, 17]. Kardiell synkope under pågående dengueinfektion till följd av höggradigt AV-block såväl som icke-ihållande ventrikeltakykardi har beskrivits [18, 19]. Antalet studier är begränsat. I en studie uppvisade i en sjukhuskohort 26,7 procent av 120 dengueinfekterade patienter förhöjt troponin I. Av dessa 120 patienter uppvisade vid inskrivning 10 patienter sinusbradykardi, 4 patienter AV-block grad I och 2 patienter högersidigt skänkelblock. Dessa EKG-förändringar gick i samtliga fall i regress före utskrivning [20].
De patofysiologiska mekanismerna bakom hjärtpåverkan är flera. Koronar hypoperfusion, ödem sekundärt till plasmaläckage, myokardit, påverkad vaskulär tonus och elektrolytrubbningar anses bidra. Även proinflammatoriska mediatorer påverkar hjärtmuskeln med kontraktilitetsnedsättning [21]. Isolerad perikardit i samband med dengueinfektion är ovanlig [22], men perikardvätska har noterats mer frekvent och tros vara kopplad till det generella plasmaläckage som förekommer vid allvarlig dengue [22, 23].
Sekundärinfektion
Dengueviruset förekommer i fyra skilda men besläktade serotyper, DENV-1–4. Infektion med en serotyp medför troligen livslång immunitet mot denna serotyp men endast 2–3 månaders korsimmunitet för övriga serotyper [24]. Ny infektion med en annan serotyp benämns sekundärinfektion och medför en ökad risk för allvarligare sjukdomsförlopp. Detta tillskrivs »antibody-dependent enhancement«, där befintliga antikroppar snarast faciliterar virusupptag till celler, vilket ökar graden av infekterade värdceller och leder till akut högre virustitrar. Detta tros utlösa ett starkare inflammatoriskt svar, som i sin tur kan bidra till en ökad kapillär permeabilitet [25-27].
Diagnostik
Diagnostik av dengueinfektion utförs i Sverige av Folkhälsomyndigheten med prov från serum eller venblod och görs antingen genom detektion av virus-RNA genom PCR med omvänd transkription under febril, viremisk sjukdomsfas eller genom serologisk diagnostik baserad på detektion av IgM (ELISA) och IgG (indirekt immunfluorescens). Serokonversion mellan parade prov betraktas som en bekräftelse på akut infektion. IgM kan påvisas redan efter ett par dagars feber. Vid sekundärinfektion noteras ofta en tidig stegring av IgG [11, 13].
Behandling
Tidig identifiering och insättning av understödjande behandling är avgörande för utgången vid allvarlig dengueinfektion. Det finns i dag inget antiviralt läkemedel. Behandlingen utgörs i första hand av vätskeersättning med isotona kristalloider [13]. Profylaktisk trombocyttransfusion hos i övrigt hemodynamiskt stabila patienter anses inte vara nödvändig [28]. Paracetamol är att föredra som symtomlindrande och febernedsättande, medan icke-steroida antiinflammatoriska läkemedel (NSAID) bör undvikas med anledning av den ökade blödningsrisken [13]. Vid allvarlig bradyarytmi ska patienten vårdas på hjärtenhet med telemetri. Patienter som uppvisar chockbild med sviktande organfunktioner kan vara i behov av intensivvård. Läkemedelsbehandling med atropin eller isoprenalin, transkutan pacing samt temporär transvenös pacing kan behöva tillgripas. Dengueorsakad bradykardi är vanligtvis övergående, och indikation föreligger då inte för permanent pacemaker [4, 5, 29].
Konklusion
Denguefeber kan i sällsynta fall orsaka höggradigt AV-block och kräva vård på hjärtenhet. Prognosen är vanligen god, och man bör därför avvakta med permanent pacemaker. Hjärtpåverkan vid denguefeber kräver interdisciplinärt samarbete mellan infektionsläkare, kardiolog och i förekommande fall intensivvårdsläkare. Mot bakgrund av globalisering och klimatförändringar är kunskap om denguefeber viktig även i den svenska sjukvården.
Potentiella bindningar eller jävsförhållanden: Peter Magnusson har erhållit arvode från Abbott, Alnylam, Astra Zeneca, Bayer, Boehringer Ingelheim, Internetmedicin, Lilly, MSD, Novo Nordisk, Octopus Medical, Orion Pharma, Pfizer, Vifor Pharma och Zoll. Gustav Mattsson har erhållit arvode från Alnylam, MSD och Internetmedicin.
Fakta 1. Fallbeskrivning
En 54-årig väsentligen frisk kvinna sökte akutmottagningen med anledning av fem dagars huvud- och nackvärk, illamående och feber. Vid tre tillfällen sedan insjuknandet hade hon plötsligt fallit ihop under oklara omständigheter. Anamnestiskt framkom inga episoder av bröstsmärta och 12-avlednings-EKG var normalt. Dagen före akutbesöket hade patienten återvänt från Punjab, Indien, där hon under tio dagar hälsat på släktingar. Ingen i hennes omgivning hade upplevt liknande besvär.
På akutmottagningen var patienten trött men orienterad. Blodtrycket var normalt, 124/52 mm Hg, puls 96 slag/minut, saturation 96 procent på luft, andningsfrekvensen 18/minut och patientens temperatur var 39,5°C. Fysikaliskt status inklusive neurologi var intakt. Plötsligt drabbades patienten av övergående medvetandeförlust, och telemetri visade totalt AV-block utan ersättningsrytm under 7 respektive 34 sekunder, varefter patienten fördes till hjärtintensivvårdsavdelningen. Laborativt sågs normalt CRP (1,3 mg/l) och leukocyter (LPK) (4,7 × 109/l), men sänkt koncentration av trombocyter (TPK) 95 × 109/l (referensvärde 165–387 × 109/l) samt förhöjda levertransaminaser: ALAT på 7,9 µkat/l (referensvärde ≤0,75 µkat/l) och GT 1,9 µkat/l (referensvärde 0,15–1,2 µkat/l).
Initialt misstänktes meningoencefalit, och behandling med meropenem och aciklovir påbörjades, men man avstod från lumbalpunktion på grund av trombocytopenin. Infektionskonsult bedömde patienten, som fortsatt var orienterad. Nackstyvhet förelåg ej, och fokala neurologiska bortfall saknades. En hudrodnad som bleknade vid tryck noterades på buken samt eventuellt viss småprickighet på flankerna. Den kliniska presentationen ansågs inte typisk för meningit eller encefalit, men behandlingen fick kvarstå med anledning av en svårtolkad symtombild. Virusinfektion misstänktes, i första hand dengue med tanke på epidemiologi, trombocytopeni och transaminasstegring. Malariasnabbtest var negativt, och utstryk analyserades utan fynd av plasmodier. Prov för diagnostik av zika-, nipah-, Krim–Kongo-, chikungunya- och denguevirus skickades till Folkhälsomyndigheten.
Under vårdtiden sjönk TPK till som lägst 70 × 109/l och ALAT steg till 8,8 ukat/l, medan LPK och CRP förblev normala. EKG visade inga tecken på myokardit. Troponin T 4 ng/l (referensvärde <15 ng/l) och NT-proBNP <50 ng/l (referensvärde <150 ng/l) var normala.
Under de första två vårddygnen hade patienten hög feber och utvecklade diffus buksmärta framför allt högersidigt, men datortomografi av torax och buk var invändningsfria. Ekokardiografi var normal och utan ökad mängd perikardvätska. Ett elektroencefalogram genomfördes också, utan patologiska fynd. På telemetrin sågs ytterligare episoder av totalt AV-block som uppgick till uppemot 30 sekunder utan ersättningsrytm. Transkutana pacingplattor applicerades och kopplades till hjärtstartare men behövdes inte användas då bradykardin upphörde. Det fördes ett resonemang om transvenös pacemaker, men man valde att avvakta på grund av den komplicerande trombocytopenin och det faktum att episoderna upphörde.
Meningoencefalitbehandling seponerades efter ett vårddygn i samband med att rt-PCR påvisade dengue-RNA i serum. Komplettering med serologi visade IgG-titer på 10 240 samt ELISA IgM OD-värde (optisk densitet) 4,0, vilket bedöms förenligt med sekundärinfektion. Patientens höggradiga AV-block bedömdes sekundärt till infektionen. Fortsatt telemetriövervakning var invändningsfri, laborativt sågs förbättring och patienten återgick till hemmet efter ytterligare ett par dagars observation.
Vid uppföljning tre veckor efter utskrivning var patienten fortsatt välmående och hade inte haft några ytterligare episoder av synkope.