Ultraljud av tyreoidea vid endokrinologisk sjukdom är ett komplement till palpation och laboratorieprov.
Ultraljud av tyreoidea har ökat kvaliteten på diagnostik och uppföljning av patienterna.
Det är viktigt att göra ultraljud på rätt indikation för att undvika överdiagnostik av förändringar i tyreoidea.
Vid detektion av incidentalom har vi själva kunnat utreda dessa för ställningstagande till vidare utredning med finnålsaspiration på endokrinologisk mottagning.
Ultraljud vid endokrinologisk mottagning kan ske på ett säkert sätt, men kräver utbildning för att inte öka belastningen på röntgenavdelningen.
Patienterna har kunnat ges besked om fynden i tyreoidea direkt vid mottagningsbesöket.
I Sverige har patienter med misstänkt tyreoideasjukdom i första hand genomgått palpation och, i samband med besök på endokrinologisk mottagning, vid behov fått remiss till röntgen för ultraljud av tyreoidea [1]. I Skåne har användningen av ultraljud av tyreoidea successivt ökat de senaste åren. I Danmark och Europa genomför man sedan många år ultraljud av tyreoidea i samband med besök på endokrinologisk mottagning, vilket ger möjlighet att redan vid besöket lämna besked till patienten samt planera eventuell vidare utredning.
Ultraljudsresan i Malmö började i Odense för 10 år sedan med auskultation hos endokrinolog Lazlo Hegedüs som är en världsauktoritet på området. Efter detta införskaffades en ultraljudsapparat till vår mottagning. De senaste åren har intresset ökat, framför allt hos yngre kollegor, och vi använder numera regelbundet förenklat ultraljud av tyreoidea som ett komplement till palpation. Utvecklingen har skett i samarbete med röntgenkliniken. Yngre kollegor har under sin utbildning haft möjlighet att genomföra ultraljud av tyreoidea i samband med mottagningsbesök och senare vid behov diskutera sina fynd varje vecka vid en ultraljudsrond på kliniken. Ultraljud har en plats i utredningen av Graves sjukdom, subakut tyreoidit, gestationell hypertyreos, postpartumtyreoidit och amiodaroninducerad tyreotoxikos samt vid bedömning av struma med eller utan avgränsade knölar.
Utredning av endokrinologisk sjukdom i tyreoidea
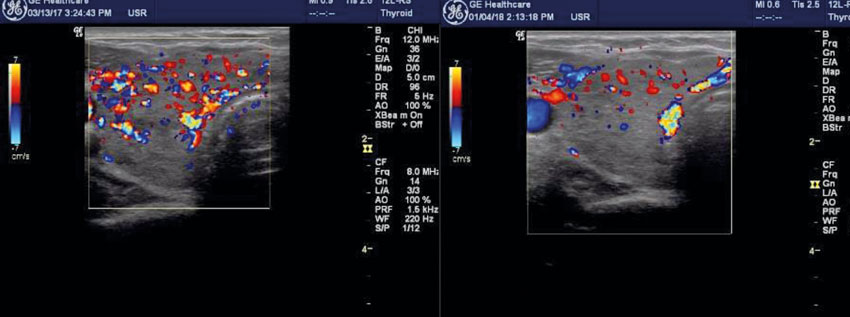
Diagnosen Graves tyreotoxikos ställs vanligtvis med hjälp av tyreoideapalpation med fynd av en diffus struma samt förhöjda nivåer av tyreoideahormoner (fT4, fT3), sänkt TSH-nivå och förhöjda nivåer av tyreoideaantikroppar (TSH-receptorantikroppar [TRAK], tyreoideaperoxidas [TPO]-antikroppar) [1]. Enligt internationella riktlinjer bör man med ultraljud bekräfta att det föreligger ett omväxlande isoekogent och hypoekogent parenkym och ett förhöjt blodföde mätt med doppler [2]. I samband med undersökning kan man utesluta eller påvisa adenom samt bedöma deras risk för malignitet enligt EU-TIRADS (European thyroid imaging and reporting data system) och ta ställning till eventuell finnålspunktion (se nedan), vilket rekommenderas i internationella riktlinjer. I uppföljningen av medicinsk behandling med tyreostatika (metimazol eller propyltiouracil) används förhöjda nivåer av tyreoideaantikroppar, TRAK, som ett mått på kvarstående aktiv sjukdom. Sjukdomsaktiviteten kan också bedömas genom bestämning av blodflödet med dopplerultraljud, och i samband med detta parenkymets utseende, och vara ett stöd för att bedöma utläkning av Graves tyreotoxikos (Figur 1). Ultraljud av tyreoidea kan ge stöd för diagnosen Graves tyreotoxikos när TRAK saknas. Med ultraljud är det lättare att bedöma tyreoideas storlek, vilket kan vara viktigt vid val av behandling då stor tyreoidea minskar chansen till utläkning, varför annan behandling bör övervägas, såsom tyreoidektomi eller radiojodbehandling.
I postpartumperioden kan det vid frånvaro av förhöjda nivåer av TRAK vara svårt att skilja debut av Graves tyreotoxikos från postpartumtyreoidit med förhöjda tyreoideahormoner. Här kan ultraljud av tyreoidea vara till hjälp i differentialdiagnostiken, då parenkymet vid en utsvämningstyreoidit har ett annat utseende än vid Graves tyreotoxikos och oftast ett normalt blodföde bestämt med doppler.
Gestationell hypertyreos beror på hCG-stimulering av tyreoidea under slutet av första trimestern, vilken är självbegränsande och inte kräver någon specifik behandling. Tillståndet kan dock vara svårt att skilja från Graves tyreotoxikos i tidig graviditet, speciellt om tyreoideaantikroppar saknas. Här kan ultraljud av tyreoidea underlätta differentialdiagnostiken, då man oftast finner normalt parenkym och normalt blodföde bestämt med doppler, till skillnad från vid Graves tyreotoxikos.
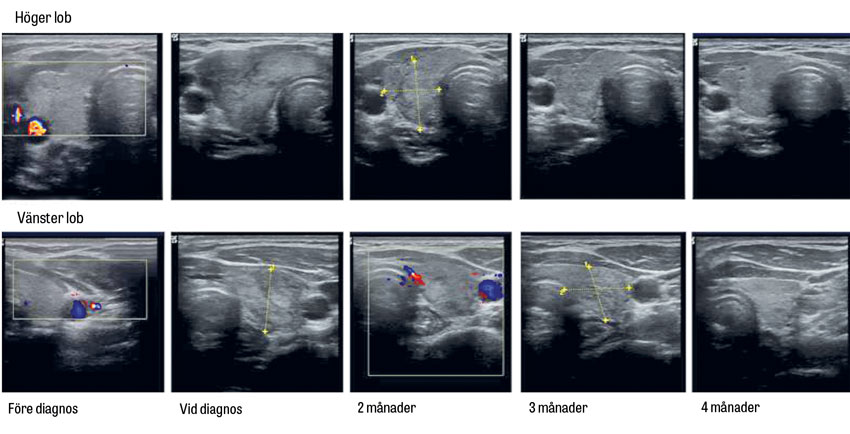
Diagnosen subakut tyreoidit kan vara lätt att ställa om patienten är ömmande på halsen vid palpation, men ganska svår vid frånvaro av typiska palpationsfynd. Förhöjd sänka och förändrade tyreoideaprov ökar träffsäkerheten. Vid ett asymmetriskt palpationsfynd kan ultraljud påvisa en bakomliggande malignitet. I uppföljningen av en patient som behandlas med prednisolon i nedtrappningsdos kan utläkning av parenkymet följas med ultraljud av tyreoidea (Figur 2).
Amiodaron (Cordarone), som används i förebyggande syfte vid förmaksflimmer och ventrikulära arytmier, kan ge mycket svårbehandlade tyreotoxikoser. Där kan ultraljud av tyreoidea ge vägledning inför val av behandling: påvisandet av ett adenom eller ökat dopplerblodflöde talar för ökad syntes av tyreoideahormon, vilket innebär att behandling i första hand påbörjas med tyreostatika i hög dos. Om man finner ett normalt dopplerflöde i kombination med ett väsentligen normalt parenkym talar det för en utsvämningstyreotoxikos, vilken i första hand behandlas med kortikosteroider. Ofta föreligger dock en blandad bild som kräver båda behandlingarna.
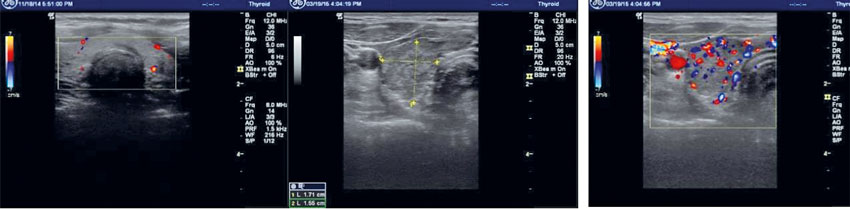
Kronisk autoimmun tyreoidit diagnostiseras genom påvisande av förhöjd TSH-nivå och i tidig fas normala nivåer av tyreoideahormoner som efter hand sjunker. Majoriteten av fallen har förhöjda nivåer av TPO-antikroppar och/eller tyreoglobulin (TG)-antikroppar. Om TPO- och TG-antikroppar saknas kan en finnålspunktion av parenkymet ge en typisk bild med infiltration av immunkompetenta celler. Ultraljud av tyreoidea har dock fördelen att vara icke-invasivt.Man finner oftast en förstorad tyreoidea med en typisk bild av små runda avgränsade hypoekogena områden (schweizerostliknande) och i tidigt skede ett ökat dopplerflöde som med tiden avtar när parenkymet blir alltmer fibrotiskt med minskande storlek hos tyreoidea (Figur 3). När diagnosen är klar sker uppföljning med provtagning av tyreoideahormoner och TSH för optimering av substitutionsbehandling med levotyroxin. Några fler ultraljudsundersökningar krävs vanligtvis inte.
Sammanfattningsvis utgör ultraljud på endokrinologisk mottagning vid uppföljning av Graves tyreotoxikos ett komplement till enbart palpation av tyreoidea och provtagning, då man med ultraljud har möjlighet att följa sjukdomsaktiviteten i parenkymet och ta beslut om hur länge behandling med tyreostatika ska pågå. Vid subakut tyreoidit kan man med hjälp av ultraljud bedöma utläkning av parenkymet och avpassa hur lång tid behandling med kortikosteroider ska ges. Gestationell tyreotoxikos är ett självbegränsande tillstånd, men med ultraljud kan det vara lättare att avgränsa mot Graves tyreotoxikos, särskilt om TRAK inte kan påvisas. Ibland kan diagnosen amiodaronorsakad tyreotoxikos underlättas med ultraljudsbedömning av parenkymet och blodflöde, men ofta får man ändå utifrån klinik och prov ge både tyreostatika och kortikosteroider. Då autoimmun tyreoidit är en vanlig sjukdom som kräver livslång substitutionsbehandling med levotyroxin kan det vara viktigt att ställa rätt diagnos vid avsaknad av tyreoideaantikroppar.
Risk för identifiering av tyreoideaincidentalom
Vid frikostig användning av ultraljud ökar risken för att upptäcka incidentalom i tyreoidea, varför man bör vara strikt med indikationen. I Sverige har vi tillsatt jod i salt sedan 1936, och joderingen ökades på 1960-talet. En studie har visat att större delen av befolkningen i Sverige har normalt jodstatus [3], vilket sannolikt påverkat förekomsten av struma och adenom i tyreoidea då vi numera har en minskande incidens av toxisk knölstruma [4]. I vårt grannland Danmark upphörde man med jodering av livsmedel under en period, vilket ökade frekvensen av adenom i tyreoidea samt toxisk knölstruma [5]. Efter återinförande av jodering av salt minskade detta problem [6]. I Europa finns det studier som visar att användning av ultraljud i stor skala ökar risken för upptäckt av tyreoideaincidentalom, som i vissa studier upptäckts hos upp till 67 procent av de undersökta individerna [7]. Indikationerna för ultraljud bör därför vara väl definierade för att undvika fler undersökningar för patienterna och därmed krav på ökade sjukvårdsresurser (Fakta 1).
Om man finner ett adenom så bör en första bedömning avse risk för bakomliggande malignitet, vilken kan göras utifrån utseende och storlek. Den europeiska tyreoideaföreningen (ETA) rekommenderar användning av EU-TIRADS [8], som anger risk för bakomliggande malignitet på basen av utseende och storlek på en skala 1–5, där 1 innebär avsaknad av knöl och 2–5 en ökande risk (Fakta 2). Detta ligger då till grund för behov av finnålspunktion. Fördelen med EU-TIRADS jämfört med rekommendationerna från den amerikanska tyreoideaföreningen (ATA) [9] är att kontrollerna oftast avslutas helt om resultatet av finnålsaspiration är normalt.
Aspirat från tyreoidea bedöms av cytolog enligt Bethesda-klassifikationen [10] (Fakta 3) och utgör grunden för den fortsatta handläggningen. Sedan mer än ett år tillbaka har endokrinologiska mottagningen i Malmö, i samarbete med röntgenkliniken, på försök genomfört finnålsaspiration av tyreoideaförändringar som upptäckts på vår mottagning, vilket har resulterat i att röntgenkliniken till viss del kunnat avlastas och att patienterna kunnat få besked av patientansvarig läkare om resultat och om avslutande av kontroller eller förnyad punktion.
Om cytologsvaret varit Bethesda 1 eller 3 genomförs ytterligare punktion, men efter tre punktioner med dåligt utbyte eller oklart fynd remitteras patienterna oftast till endokrinkirurg för ställningstagande till hemityreoidektomi för att få en definitiv diagnos. Vid låg risk för malignitet har vi i utvalda fall i stället för kirurgi rekommenderat patienten nytt ultraljud på vår mottagning efter 6–12 månader.
Vid Bethesda 4–6 skickas alltid remiss till kirurgen för ställningstagande till hemityreoidektomi eller total tyreoidektomi.
Sammanfattningsvis har detektion av tyreoideaincidentalom inte ökat belastningen på röntgenkliniken, då vi själva har kunnat utreda dessa för ställningstagande till vidare utredning med finnålsaspiration samt genomföra denna på endokrinologisk mottagning. Patienterna har kunnat ges besked om fynden direkt vid mottagningsbesöket, eller efter några veckor vad gäller fynd efter finnålsaspiration.
För att genomföra ultraljud vid en endokrinologisk mottagning på ett säkert sätt krävs strukturerad utbildning av mottagningens ST-läkare med instruktion om apparaten och tolkning av bilder, vilken sker på ultraljudsrond på kliniken, samt någon form av certifiering (som vid riktat ultraljud på akutmottagning). För att fördjupa kunskapen rekommenderas kurser i samband med internationella endokrinologkonferenser. Nationella utbildningsprogram för endokrinologer kan vara en väg framåt.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Indikationer för ultraljud
För läkare som primärt handlägger knölar i tyreoidea (distriktsläkare, kirurger, öronläkare, endokrinologer):
- Nyupptäckt knöl/struma i tyreoidea efter palpation. Vid sänkt TSH <0,2 mE/l i upprepade prov, överväg i första hand tyreoideaskintigrafi.
- Tillväxt av tidigare känd knöl
- Känd struma med eller utan sidoskillnad som tillväxer
- Kallt upptag vid tyreoideaskintigrafi
- Incidentalom i tyreoidea efter DT, MR eller PET
Tilläggsindikationer för endokrinologer som har tillgång till och gör ultraljud på mottagning:
- Graves sjukdom
- Amiodaronorsakad tyreotoxikos
- Subklinisk/lindrig klinisk hypotyreos utan autoantikroppar
- Differentialdiagnostik av gestationell hypertyreos eller Graves hypertyreos
- Postpartumtyreoidit
- Subakut tyreoidit
Fakta 2. Klassifikation enligt EU-TIRADS
EU-TIRADS 1: Inga visualiserbara noduli – ingen finnålsaspiration.
EU-TIRADS 2: Ingen risk för malignitet – endast finnålsaspiration vid cysta som ger symtom (kan eventuellt punkteras på endokrinologisk mottagning).
EU-TIRADS 3: 2–4 procents risk för malignitet – finnålsaspiration om storlek >2 cm, annars avslutas kontrollerna. Om finnålsaspiration visar Bethesda 2 avslutas kontrollerna.
EU-TIRADS 4: 6–17 procents risk för malignitet – finnålsaspiration om storlek >1,5 cm, annars avslutas kontrollerna. Om Bethesda 2 avslutas kontrollerna.
EU-TIRADS 5: 26–87 procents risk för malignitet – finnålsaspiration om storlek >1 cm. Om Bethesda 4–6 remiss till kirurgen. Vid benign cytologi ny finnålsaspiration efter 3 månader. Förändringar <1 cm följs på mottagning, och om tillväxt sker görs ny finnålsaspiration.
Fakta 3. Bethesda-klassifikationen
Bethesda 1
Det finns för lite material för bedömning. Planera för ny finnålsaspiration. Om fortsatt dåligt utbyte efter totalt 2–3 punktioner så remitteras patienten till kirurgen för ställningstagande till hemityreoidektomi.
Bethesda 2
Benignt fynd, vilket innebär att man kan avsluta utredningen förutom vid EU-TIRADS 5 (se Fakta 2). 0–3 procents risk för malignitet.
Bethesda 3
Material finns att bedöma, men man kan inte helt säkert utesluta bakomliggande malignitet. Ny finnålsaspiration planeras. Om förnyad punktion återigen visar Bethesda 3 kan möjligen ytterligare en punktion genomföras, annars remitteras patienten till kirurgen för ställningstagande till hemityreoidektomi. 5–15 procents risk för malignitet.
Bethesda 4
Follikulär neoplasi eller misstanke om follikulär neoplasi. Remiss till kirurgen. 15–30 procents risk för malignitet.
Bethesda 5
Misstanke om malignitet (papillär tyreoideacancer, medullär tyreoideacancer, metastatisk cancer, lymfom). Remiss till kirurgen. 60–75 procents risk för malignitet.
Bethesda 6
Malignt fynd (papillär tyreoideacancer, lågt differentierad tyreoideacancer, medullär tyreoideacancer, anaplastisk tyreoideacancer, skivepitelcancer, blandformer av cancer, metastaserande cancer, non-Hodgkins lymfom, övrigt). Remiss till kirurgen. 97–99 procents risk för malignitet.