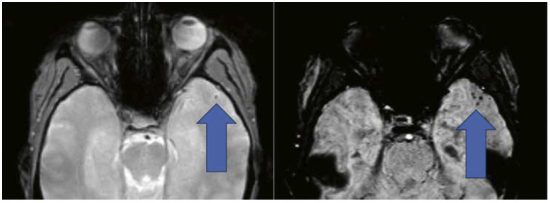
I Sverige finns uppskattningsvis drygt 100 000 personer med Alzheimers sjukdom i tidigt stadium (lindrig kognitiv störning och lindrig demenssjukdom) – den patientgrupp läkemedelsbolag inriktar sig på för att komma in med behandling så tidigt som möjligt i förloppet.
Efter flera misslyckanden har nu sjukdomsmodifierande behandling visats kunna fungera vid Alzheimers sjukdom. Nyligen (6 januari 2023) godkändes lecanemab, en humaniserad monoklonal antikropp, av den amerikanska läkemedelsmyndigheten FDA [1]. Lecanemab botar inte sjukdomen, men en studie visar cirka 27 procents minskad försämring i kognition och funktion jämfört med placebo [2]. Studien visar på en del biverkningar (exempelvis vasogent ödem och mikroblödningar), som dock rapporterats vara hanterbara.
Lecanemab kommer sannolikt att godkännas även av den europeiska läkemedelsmyndigheten EMA för behandling inom EU. Beslut om prissubvention behandlas därefter på landsnivå. Två viktiga aspekter som bör lyftas fram är lämplig patientpopulation för behandling samt samhällets betalningsvilja. Det måste visas att kostnaden för läkemedel som används till stora patientpopulationer är hanterbar och rimlig samt står i proportion till värdet av de hälsofördelar som levereras.
Vid lanseringen av aducanumab – den första antikropp som godkändes av FDA – försökte företaget kombinera en stor potentiell målgrupp med ett mycket högt pris [3]. Till skillnad från aducanumab visar lecanemab effekt på kliniska utfall. Antalet personer med tidig Alzheimers sjukdom är globalt tiotals miljoner [4]. I Sverige är en försiktig skattning att cirka 100 000 personer kan uppfylla kriterier för behandling [5].
Diagnostisk kapacitet måste förberedas, då detta förmodligen kommer att medföra stora förväntningar på diagnostik och behandling. I primärvården kan blodbaserade biomarkörer i kombination med kognitiva test fungera som »filter« för att identifiera patienter som är potentiellt lämpliga för behandling. Kapaciteten är dock begränsad på många håll. På specialistnivå blir utmaningarna ännu större. Förutom läkemedelskostnaden måste man beakta kostnader för diagnostik, läkemedelshantering samt uppföljande undersökningar för att följa effekt och biverkningar.
Enligt uppgift i USA har listpriset för lecanemab satts till 26 500 dollar (cirka 265 000 kronor) per terapiår [6]. Om detta pris tillämpas på hela den berättigade patientpopulationen i Sverige skulle den årliga läkemedelskostnaden för lecanemab bli 26,5 miljarder, vilket kan jämföras med att den totala kostnaden för receptbelagda läkemedel i Sverige var 33 miljarder 2021 [7].
Kostnaden för ett enskilt läkemedel skulle alltså (använt fullt ut inom godkänd indikation) motsvara cirka 80 procent av de totala läkemedelsutgifterna. Eftersom många patienter kommer att behandlas i många år (inga stoppregler finns ännu) kommer kostnaderna att öka över tid.
Detta scenario är orimligt. Ett högt pris kan leda till att regionerna minskar antalet behandlade patienter, eller till och med vägrar ersättning.
Ett lägre pris skulle möjliggöra bredare tillgång till behandling och skapa fler möjligheter att samla in data om lecanemab i rutinvård, vilket kan ge värdefull vägledning för att maximera kliniska fördelar och begränsa biverkningar. Kvalitetsregistret Svedem [8] ger oss dessutom unika förutsättningar att systematiskt följa upp behandlingen.
Om prissättnings- och ersättningsmekanismerna misslyckas med att skapa tillgång för patienter till nya behandlingar kan det få negativa återverkningar för framtida forskning och investeringar.
Det är hoppfullt att sjukdomsmodifierande behandling äntligen kan fungera vid Alzheimers sjukdom. Pris- och ersättningsdiskussionen är därför viktig och kan förhoppningsvis resultera i ett rimligt pris.
(uppdaterad 2023-01-31)