TTF (tumour treating fields) är en ny, nationellt godkänd utrustning, som inducerar alternerande elektriska fält och används vid behandling av hjärntumören glioblastom.
Behandlingen kan vara inskränkande i vardagen, och data från det nationella registret för CNS-tumörer visar att mer än hälften av patienterna avbryter TTF på grund av dålig användningsgrad eller egen önskan.
Genomsnittlig behandlingstid enligt registret är 164 dagar.
Jämfört med matchade kontroller visar data från registret en trend med längre överlevnad för patienter som behandlas med TTF; dock är skillnaden inte statistiskt signifikant.
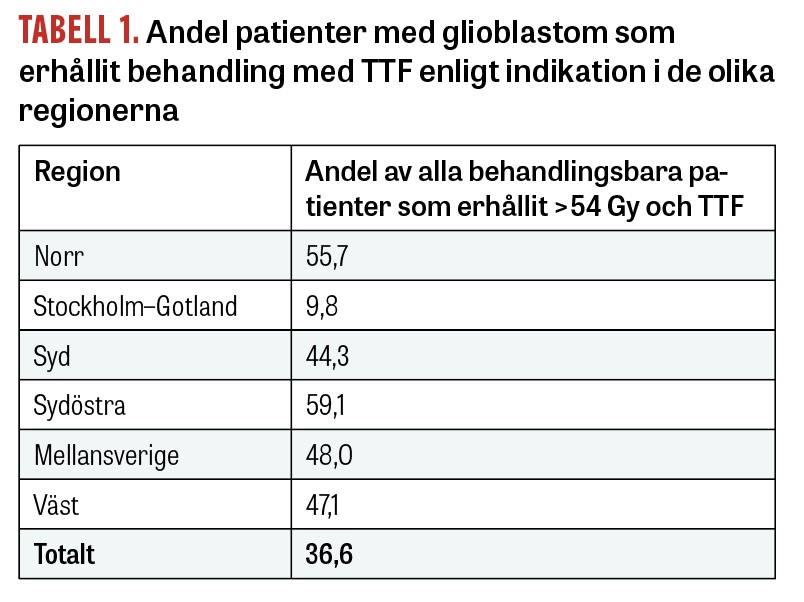
Det finns en stor regional variation i andelen patienter som erbjudits behandlingen.
Bland primära maligna hjärntumörer är höggradiga gliom (WHO grad 3‒4), särskilt glioblastom (WHO grad 4), de vanligaste, och ca 500 personer diagnostiseras varje år i Sverige. Det är en sjukdom med allvarlig prognos som medför stor risk för påverkan på individens personlighet. Närstående är också utsatta, då relationen till den sjuke ofta påverkas långt innan personen avlider. Det är viktigt att man optimalt utnyttjar de tillgängliga, men begränsade, behandlingsmöjligheter som finns för att bevara patientens livskvalitet och om möjligt förlänga livet. Det är också angeläget att patienten själv får möjlighet att ta del av information om möjligheter och risker med de behandlingar som står till buds för att kunna vara delaktig i besluten kring sin egen behandling.
När en kombination av strålbehandling och cytostatika (temozolomid) infördes för drygt 15 år sedan noterades en överlevnadsvinst för patienter som tolererade behandlingen, vilket även ses vid analys av svenska data [1]. För patienter med nedsatt allmäntillstånd kan förkortad strålbehandling med eller utan temozolomid eller enbart temozolomid vara ett bättre alternativ [2]. Trots ett mycket stort antal studier har inget bättre behandlingsalternativ ännu introducerats.
Sedan 2018 har en ny behandlingsform godkänts i Sverige för glioblastom: »tumour treating fields« (TTF eller Optune), där man utnyttjar elektriska fält för att behandla tumörer [2, 3]. TTF avger lågintensiva, medelfrekventa (200 kHz) och växlande elektriska fält via så kallade gelplattor (transducer arrays) som appliceras på skalpen ovanför tumören. Teorin bakom behandlingen är att de elektriska fälten stör tumörcellernas delning. Behandlingen pågår kontinuerligt, och rekommendationen är att apparaturen ska vara påkopplad minst 18 timmar per dygn för att ge tillräcklig effekt. För god kontakt mellan huden och gelplattorna ska huvudet rakas regelbundet (Figur 1). I regel behöver patienten hjälp med vissa delar av behandlingen.
Studien som låg till grund för godkännandet av TTF, den så kallade EF-14-studien, visade på knappt 5 månader förlängd överlevnad när glioblastompatienter behandlades med TTF i tillägg till standardbehandling med strålbehandling och temozolomid [4]. Behandlingskonceptet tycks även ha positiva effekter vid andra tumörformer, och TTF är godkänd i USA för behandling av mesoteliom.
Nationella vårdprogramgruppen för CNS-tumörer rekommenderar sedan 2018 att TTF erbjuds till patienter med glioblastom som uppfyller de kriterier som användes i EF-14-studien, det vill säga supratentoriella glioblastom utan tecken på tumörprogress efter avslutad initial behandling (strålbehandling och temozolomid) [2]. Behandlingen kan fortsätta när tumören progredierar, men ska avslutas vid en andra progress eller efter maximalt 2 års behandlingstid. TTF rekommenderas även internationellt för behandling av glioblastom [5], och är godkänd i USA, Kanada, Israel och Japan. I Europa är behandlingen godkänd i Sverige, Tyskland, Österrike och Schweiz. Trots dessa rekommendationer är TTF inte tillgänglig i många av dessa länder och är fortfarande inte en del av standardbehandlingen/kontrollarmen i kliniska studier.
Metod
Detta är en fall‒kontrollstudie av data från det nationella kvalitetsregistret för CNS-tumörer. Alla patienter med glioblastom som erbjudits behandling med TTF från den 1 januari 2018 till den 1 mars 2022 har inkluderats. Indikationen för TTF är supratentoriellt glioblastom som planeras för postoperativ strålbehandling med en stråldos upp till 60 Gy (30 fraktioner) samt samtidig och adjuvant temozolomidbehandling. I vissa fall kan tolerans hos riskorgan göra att stråldosen måste sänkas till 54 Gy. I vår analys betraktas de patienter som fått 54 Gy som likvärdiga vad gäller indikation. Patienter som behandlats med TTF har jämförts med matchade kontroller. Matchningen gjordes 1:1, med följande kriterier: ålder (18–50, 51–60 och 61–80 år), kön, funktionsstatus (WHO grad 0, 1–2 eller 3–4) vid start av strålbehandling, omfattningen av operationen (biopsi, partiell resektion eller radikal resektion), given stråldos (ingen, <54 Gy eller >54 Gy) och MGMT-status (genen för O6-metylguanin-DNA-metyltransferas: metylerad, icke-metylerad eller ej angiven). Både fallen och kontrollerna har erhållit temozolomidbehandling. Överlevnadstid räknades från patienternas operationsdatum. Kontrollerna valdes så att ingen hade avlidit innan TTF-behandling påbörjats i motsvarande fall. Skillnad i överlevnad undersöktes med ett log rank-test. Testen utfördes med hjälp av statistikprogrammet SPSS, version 28.0.
Studien är godkänd av Etikprövningsgmyndigheten (avdelningen i Umeå), dnr 2020-06886.
Resultat
Antal patienter och behandlingstid
Genomgång av CNS-registret visade att 236 patienter erbjudits TTF under åren 2018‒2022, och 154 (65 procent) av de tillfrågade accepterade behandlingsförslaget. Vid analysen noterades att 141 patienter slutligen inledde behandlingen. Antalet patienter som enligt kvalitetsregistret behandlats med TTF stämmer väl med data från företaget. I det nationella vårdprogrammet stipuleras att TTF ska erbjudas patienter som genomgått strålbehandling med 60 Gy tillsammans med temozolomid, det vill säga inte dem som planerats erhålla kortare strålbehandling. Registreringarna visade att 14 av patienterna hade erhållit en lägre stråldos än 54 Gy. Behandlingstiden var i median 164 dagar, och 30 procent av patienterna avslutade behandlingen inom 90 dagar. Registrerad behandlingstid varierade mellan 0 och 774 dagar. 4 patienter hade en längre registrerad behandlingstid än 700 dagar.
Orsaker till att behandlingen avslutades var tumörprogress (44 procent), patientens önskan att avbryta (44 procent) och dålig följsamhet (9 procent). Biverkningar var lindriga, och endast 3 procent av patienterna avbröt på grund av lokal hudirritation.
Stor regional variation
I studien jämfördes antalet patienter som erhållit strålbehandling med en dos på minst 54 Gy med det antal som också startat behandling med TTF. Endast 37 procent (203 av 555) av de patienter som uppfyllde behandlingskriterierna erbjöds behandling, och för 17 procent av patienterna saknades data. Andelen patienter som erhållit TTF uppvisade tydliga skillnader mellan olika regioner, med en variation mellan 9,8 och 59,1 procent av möjliga behandlingsbara patienter (Tabell 1). Det fanns ingen korrelation till befolkningstäthet eller storlek på ansvarig klinik.
Livskvalitet
Patienter i CNS-registret erhåller speciella validerade livskvalitetsenkäter (EORTC-QLQ30) 3 och 12 månader efter operation. Bland enkätfrågorna finns två övergripande frågor om hur patienten beskriver sin hälsa och sin totala livskvalitet under den senaste veckan, graderat från 0 (sämst) till 7 (bäst). Svaren vägs samman i ett index som kallas »global hälsa och livskvalitet« och graderas från 0 (sämsta möjliga hälsa och livskvalitet) till 100 (bästa dito).
Vid analysen jämfördes patienterna som behandlats med TTF (53 vid 3 månader och 61 vid 12 månader) och deras matchade kontroller (35 vid 3 månader och 29 vid 12 månader). Vid både 3 och 12 månader låg medianen för global hälsa och livskvalitet på 67 i båda grupperna, men andelen inskickade enkäter var mindre över tid i kontrollgruppen. Studien kunde inte bekräfta farhågan att TTF försämrar livskvaliteten.
Överlevnad
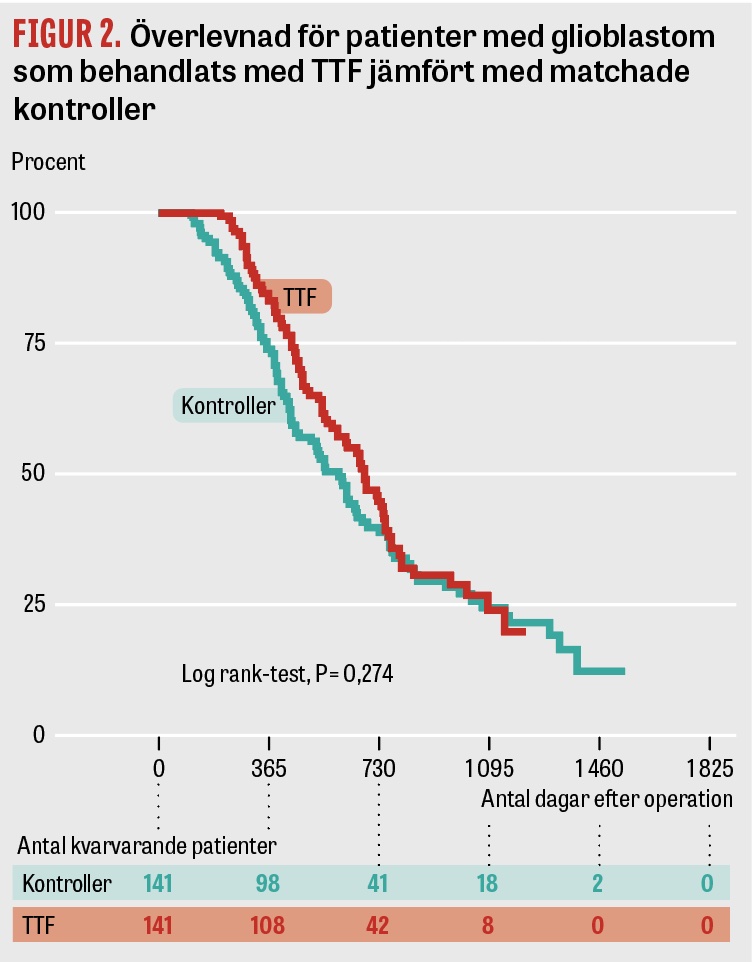
I Figur 2 redovisas överlevnaden för TTF-behandlade patienter och de matchade kontrollerna. Matchningen gav två grupper med 141 patienter i vardera. Medianöverlevnaden var 596 dagar i gruppen som inte fått behandling med TTF och 680 dagar i den TTF-behandlade gruppen. Skillnaden var dock inte signifikant (P = 0,274).
Diskussion
TTF är en ny behandling för glioblastom. Behandlingen har få somatiska biverkningar, men är samtidigt ett nytt behandlingskoncept som påverkar patientens vardag på ett annat sätt än tidigare behandlingar. Behandlingen är kontinuerlig, och det krävs dagligt omhändertagande som kan upplevas besvärligt och stigmatiserande. Behandlingen är godkänd av NT-rådet och rekommenderas i nationellt vårdprogram, baserat framför allt på en publicerad randomiserad studie som påvisat en överlevnadsvinst på 5 månader med behandlingen. Vi har gått igenom data från det nationella kvalitetsregistret avseende användning, behandlingseffekt och påverkan på livskvalitet av TTF i rutinbehandling för glioblastom i Sverige efter godkännandet 2018.
Det mest överraskande fyndet är den stora regionala variationen i användningen. Denna kan ha flera orsaker: till exempel kan läkarens personliga uppfattning om TTF:s inverkan på livskvalitet påverka om behandlingen erbjuds eller inte. Skillnaderna kan också bero på tillgång till resurser och enskilda klinikers prioriteringar, då behandlingskostnaden är hög, drygt 100 000 kr per behandlingsmånad. Längre avstånd till vården för nödvändigt stöd under behandling i hemmet verkar inte vara en komplicerande faktor, då data visar att användningen är större i regioner med gles befolkning och långa avstånd till sjukhus än i den mest tättbefolkade och största sjukvårdsregionen.
De direkta somatiska behandlingsrelaterade biverkningarna är i regel lindriga och är mycket sällan anledning till att behandlingen avslutas. I patientrapporterade data från registret ses inte heller någon försämrad livskvalitet med behandlingen. Upplägget med kontinuerlig behandling under lång tid upplevs troligen som belastande av många patienter, att döma av det stora antalet som tackar nej eller avbryter behandlingen på egen begäran. Särskilt kognitiva svårigheter och motoriska bortfall ger svårigheter att hantera behandlingen på egen hand. Således verkar en del patienter uppleva att TTF inskränker livskvaliteten, medan andra lyckas integrera behandlingen väl i vardagslivet och känner en styrka i att själv aktivt vara en del av behandlingen mot sin tumörsjukdom.
Våra data visar en numeriskt längre överlevnad i den TTF-behandlade gruppen, men den är inte statistiskt signifikant. Vi har matchat utifrån kända prognostiska faktorer, såsom ålder, funktionsstatus, MGMT-status och omfattning av kirurgi. Vi har valt kontroller som levde åtminstone tills TTF-behandling påbörjats i motsvarande fall, vilket leder till en underskattning eftersom kontrollfallen kunde avlida dagen därpå och då förstås inte skulle ha varit aktuella för TTF. Svårigheten att definiera en rimlig annan tidpunkt i förhållande till behandlingsstart gör att vi ändå valt denna metod. En mycket liten andel av patienterna hade tumörer med IDH (isocitratdehydrogenas)-mutation, och detta bedöms inte ha påverkat resultatet.
Slutsatser
TTF ska i dag enligt gällande riktlinjer vara en integrerad del av behandlingen av patienter drabbade av glioblastom i Sverige och internationellt. EF-14-studien visade en överlevnadsvinst på 5 månader med TTF, vilket är den största uppmätta överlevnadsvinsten i en kontrollerad studie på den aktuella patientpopulationen. Data från CNS-registret visar en icke signifikant och numerärt längre överlevnad för de TTF-behandlade patienterna jämfört med en kontrollgrupp som matchats avseende de viktigaste prognostiska faktorerna. Detta talar för en möjlig överlevnadsvinst vid behandling med TTF, även i en populationsbaserad grupp i rutinanvändning.
En tämligen stor del av patienterna erbjuds inte behandling med TTF eller tackar nej till den. Många patienter avbryter behandlingen efter eget önskemål eller på grund av dålig följsamhet till protokollet (minst 18 timmar per dag). Registret visar en stor regional variation i hur många patienter som erbjudits behandlingen, trots att det finns en stark regional enighet om det nationella vårdprogrammet, där TTF ingår som rutinbehandling av glioblastom. Ur ett patientperspektiv är det av betydelse att alla patienter erhåller adekvat information om tillgängliga behandlingar för att därefter kunna fatta ett eget beslut. Vi rekommenderar därför en fortsatt diskussion i vårdprogramgruppen och i alla regioner för att se till att TTF erbjuds på ett jämlikt sätt i hela landet.
Potentiella bindningar eller jävsförhållanden: Sara Kinhult är nationell koordinator för studien CC90010-GBM-002, som drivs av Bristol-Myers Squibb . Ersättning för uppdraget har betalats till VE onkologi vid Skånes universitetssjukhus. Roger Henriksson har varit moderator för vetenskapliga symposier om hjärntumörer där Novocure varit sponsor, samt erhållit ekonomisk ersättning för deltagande i ett internationellt vetenskapligt råd för Novocure.