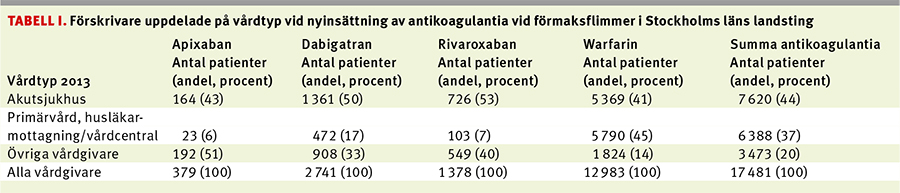
Sedan introduktionen av NOAK (non-vitamin K antagonist oral anticoagulants) som trombosprofylax vid förmaksflimmer har det skett en markant ökning av antalet diagnostiserade patienter med förmaksflimmer i Stockholms läns landsting.
Andelen som är behandlade med antikoagulantia har samtidigt ökat från 47 till 58 procent. Vid nyinsättning är NOAK lika vanliga som warfarin i nuläget.
Förskrivningen av ASA sjunker kraftigt.
NOAK-förskrivningen har varit avvaktande avseende de äldsta patienterna med hög risk för stroke, blödning och nedsatt njurfunktion.
Förmaksflimmer är en viktig riskfaktor för stroke. Under 2012 drabbades närmare 7 000 patienter med förmaksflimmer i Sverige av stroke [1]. Stroke som drabbar patienter med förmaksflimmer räknas allmänt som kardioembolisk men en okänd andel kan ha annan orsak. I Sverige beräknas 2,9 procent av den vuxna befolkningen ha förmaksflimmer [2]. Behandling med antikoagulantia minskar avsevärt strokerisken vid förmaksflimmer men medför en ökad risk för allvarlig blödning [3]. Riskskattning med CHADS2 har ersatts av skattning med CHA2DS2-VASc, som även ger poäng för vaskulär sjukdom, ålder 65–74 år och kvinnligt kön, för att bättre bedöma risken för stroke hos lågriskpatienter med förmaksflimmer [4]. Vi har funnit att 85 procent av patienterna med icke-valvulärt förmaksflimmer i Stockholms läns landsting har tydlig indikation för antikoagulantia enligt CHA2DS2-VASc (det vill säga ≥ 2 poäng) [5]. Vid CHA2DS2-VASc = 1 poäng rekommenderas att överväga behandling med antikoagulantia [4] vilket ökar den behandlingsbara andelen av förmaksflimmerpopulationen till 94 procent [5]; dock utgör kvinnligt kön ensamt inte behandlingsindikation. Ställningstagande till antikoagulantiabehandling innebär även beaktande av blödningsrisk och andra patientfaktorer, varför alla patienter med förmaksflimmer som indikation för antikoagulantia inte kan/bör behandlas.
Warfarin (Waran, Warfarin Orion) har sedan länge varit förstahandsbehandling för att förebygga stroke vid förmaksflimmer [3, 6]. Den individuella doseringen med målet att hålla PK(INR) mellan 2,0 och 3,0 syftar till att optimera förhållandet mellan antitrombotisk effekt och risken för blödningar för varje individ [3, 6]. Nytta–riskbalansen för warfarin är starkt beroende av hur stor andel av tiden som PK(INR) ligger inom terapeutiskt intervall [7, 8]. Goda rutiner för warfarindosering har stor betydelse för resultatet [9].
NOAK – fortfarande relativt oprövade
Tre NOAK (non-vitamin K antagonist oral anticoagulants) har nu godkänd indikation och subvention för förebyggande av stroke vid icke-valvulärt förmaksflimmer på basen av stora internationella studier som jämför medlen med warfarin [10-12]. Det är trombinhämmaren dabigatran (Pradaxa) samt faktor Xa-hämmarna rivaroxaban (Xarelto) och apixaban (Eliquis). De är viktiga tillskott till behandlingsarsenalen men är ännu relativt eller mycket oprövade i vanlig sjukvård, varför de bör introduceras med omsorg och god uppföljning.
I Stockholm pågår sedan 2010 ett multidisciplinärt arbete för strukturerat införande av NOAK. Som hjälp till förskrivare och annan vårdpersonal i landstinget publiceras löpande rekommendationer och råd kring hanteringen av nya antikoagulantia (Janusinfos rekommendationer). Warfarin är i nuläget rekommenderat förstahandsalternativ för trombosprofylax vid förmaksflimmer i Stockholm. Behandling med NOAK kan vara lämplig för vissa patienter och i vissa situationer [13]. Socialstyrelsens nationella riktlinjer [14] likställer warfarin och NOAK medan det europeiska kardiologsällskapet (ESC) förordar NOAK före warfarin [4]. Av intresse är att de nya amerikanska riktlinjerna ger warfarin ett visst försteg före NOAK [15]. För patienter med mekanisk klaffprotes eller signifikant mitralisstenos är warfarin för närvarande det enda rekommenderade medlet. Dabigatran har studerats på denna indikation, men visade sig vara mindre effektivt än warfarin hos dessa patienter även vid högre dos än vid förmaksflimmer och trots kontroller för att undvika låga plasmahalter [16].
Alla tre NOAK har visat likartat eller bättre förebyggande av stroke och likartad eller lägre risk för allvarlig blödning jämfört med warfarin (PK(INR)-mål 2,0–3,0) i multinationella studier med 6 000–9 000 patienter per behandlingsgrupp och 1,6–2 års medianuppföljning [10-12]. Risken för hjärnblödning var i studierna lägre med alla tre NOAK jämfört med warfarin. Risken för allvarlig gastrointestinal blödning var däremot högre med dabigatran i normaldos (150 mg × 2) och med rivaroxaban jämfört med warfarin [10-12]. Warfarinbehandlingens kvalitet har varierat påtagligt mellan regioner i de pivotala förmaksflimmerstudierna, och resultaten kan därför inte enkelt generaliseras till länder med välfungerande warfarinbehandling, som Sverige [2, 7, 17-19]. Dessutom garanterar inte resultat i en kontrollerad och noggrant uppföljd klinisk prövning samma effekt och säkerhet i sjukvården.
Dabigatran, rivaroxaban och apixaban är alla direktverkande och har kort anslagstid med full effekt inom 1–4 timmar efter intag, men de har sinsemellan olika farmakodynamik och olika farmakokinetik. Biotillgängligheten varierar från 3–7 procent (dabigatran) till över 90 procent (rivaroxaban taget med föda), och proteinbindning och distibutionsvolym skiljer sig åt. Alla tre NOAK kan behöva dosreduceras vid sänkt njurfunktion, och de är inte studerade hos patienter med uppskattad glomerulär filtration (eGFR) < 25–30 ml/minut [20-24], varför vi avråder från behandling med NOAK av dessa patienter. Dabigatran elimineras mest (80 procent) och apixaban minst (25 procent) via njurarna [20-24]. För äldre patienter med sänkt njurfunktion, patienter med dyspeptiska besvär och/eller patienter med ischemisk hjärtsjukdom anser vi att dabigatran är mindre lämpligt än faktor Xa-hämmarna [20]. För patienter med leversjukdom eller leverpåverkan finns färre restriktioner med dabigatran än med faktor Xa-hämmarna, vilka i stor utsträckning elimineras hepatiskt/biliärt [20-24]. NOAK är kontraindicerade för patienter med mekanisk hjärtklaffprotes och har inte prövats i nämnvärd utsträckning på patienter med signifikanta klaffvitier, samtidig cancersjukdom eller på dem som är över 80 år.
Läkemedelsinteraktioner är, liksom vid warfarinbehandling, en viktig aspekt vid behandling med NOAK. Alla NOAK interagerar via P-glykoprotein med amiodaron/dronedaron och kalciumantagonister vilka används vid förmaksflimmer samt med ett antal andra läkemedel [20-24]. Faktor Xa-hämmarna interagerar dessutom med läkemedel som hämmar eller inducerar CYP3A4 [20, 21, 23, 24]. Kunskaperna om läkemedelsinteraktioner med NOAK och dessas kliniska betydelse är ännu begränsade.
Samtliga NOAK har relativt kort halveringstid (8–15 timmar) vid normal njurfunktion. Dabigatran och apixaban ges två gånger per dag medan rivaroxaban ges en gång dagligen. En endosregim är bekväm för patienten men innebär större svängningar i antikoagulerande effekt under doseringsintervallet och kan även vara mindre förlåtande avseende ordinationsföljsamhet eftersom effekten försvinner relativt snabbt efter en utebliven dos [20-24]. Dabigatrans kapslar innehåller allergena färgämnen, och de får inte avlägsnas från sin blisterförpackning på grund av fuktkänslighet [22].
Specifik antidot saknas ännu för alla tre NOAK även om arbete med att utveckla sådana pågår. Elimineringen av dabigatran kan påskyndas med hemodialys medan protrombinkomplexkoncentrat (PCC) troligen (inte dokumenterat ännu) har förmåga att motverka effekter av FXa-hämmarna [25]. Alla som kan komma i kontakt med NOAK-behandlade patienter i akuta situationer och inför olika interventioner bör ha kunskap om läkemedlen [20, 26-28]. Patienterna måste vara välinformerade och följas upp väl. Antikoagulantiabrickor ska användas även av NOAK-behandlade patienter.
ASA har ofta givits till förmaksflimmerpatienter som man av olika anledningar inte vågar eller vill behandla med antikoagulantia. För apixaban och warfarin finns dokumentation som visar en väsentligt bättre strokeprofylax, utan betydelsefullt fler blödningar, jämfört med ASA [3, 29, 30]; antikoagulantiabehandling bör därför prioriteras före ASA om ingen viktig indikation för ASA föreligger [14].
Vid val av NOAK som alternativ till warfarinbehandling bör skillnader mellan läkemedlen och patientspecifika egenskaper inklusive övrig behandling beaktas. För samtliga NOAK bör doseringen anpassas för vissa patientkategorier och till exempel vid misstanke om betydelsefull interaktion med annat läkemedel. Samtidig trombocythämmande behandling ökar blödningsrisken; NOAK bör enligt vår mening inte kombineras med potenta ADP-receptorhämmare som tikagrelor (Brilique) eller prasugrel (Efient).
Övervakning av NOAK-effekter anses inte behövas, men det innebär en förenklad syn på antikoagulantiabehandlingens balansgång mellan effekt och säkerhet. Speciella test krävs för bedömning av behandlingsintensiteten för dosjustering och/eller i akuta situationer [19, 20, 25, 31, 32]. För dabigatran finns publicerade data från RE-LY-studien som visar vilket intervall av plasmakoncentrationer som medför minst risk att drabbas av stroke eller allvarlig blödning [33], analogt med PK(INR)-intervallet för warfarin. För rivaroxaban och apixaban saknas motsvarande dokumentation. Av intresse är att plasmakoncentrationerna av dabigatran varierar avsevärt (20-faldigt) mellan patienter med doser enligt rekommendationerna i Fass och i många fall är i lägsta laget [34]. En klok användning av validerade test kan i framtiden leda till en bättre och säkrare NOAK-behandling. Erfarenheterna av att hantera utebliven effekt eller allvarliga blödningar och invasiva ingrepp under NOAK-behandling är ännu mycket begränsade [25].
Läkemedlens effekt och biverkningar är givetvis beroende av patienternas följsamhet till ordinationen. Bristande följsamhet är ett problem vid flera kroniska sjukdomar. I de pivotala studierna var behandlingsavbrotten fler med dabigatran jämfört med warfarin, något fler med rivaroxaban och något färre med apixaban [10-12]. I kliniska prövningar är förutsättningarna för hög följsamhet bättre än i rutinsjukvården, och risken finns att de förenklade rutinerna vid behandling i sjukvården och avsaknad av kontroller för NOAK medför en försämrad följsamhet. Vid behandling med NOAK är det extra viktigt med information om vikten av god följsamhet vid regelbundna kontakter med patienten.
En kohortstudie har belyst populationen med förmaksflimmer i Stockholms läns landsting, inklusive dem som endast återfanns i primärvården, samt patienternas behandling före införandet av NOAK [5]. Valda resultat återges nedan. Föreliggande rapport syftar till att belysa hur antalet patienter med förmaksflimmer förändras över tid samt hur användningen av antikoagulantia vid förmaksflimmer i Stockholms läns landsting har påverkats i och med introduktionen av NOAK.
Metod
I denna kohortstudie används, liksom tidigare [5], registrerade diagnoser och uthämtade läkemedel från Stockholms läns landstings administrativa vårddatalager, VAL. Databasen innehåller pseudonymiserade data, det vill säga avidentifierade data där personnummer ersatts av ett krypterat id-nummer, med diagnoser från all primärvård, sjukhusbaserad öppenvård och slutenvård i landstinget [5]. För sjukhusen innehåller databasen samma data som Socialstyrelsens nationella patientregister [5]. Sedan juli 2010 ingår även individbaserade data över uthämtade recept i VAL [5]. Här ingår även recept från privata specialister som ersätts enligt nationella taxan. För kvalitetsuppföljning och forskning kring förmaksflimmer har VAL länkats till diagnoser och åtgärdskoder från Socialstyrelsens patientregister, läkemedelsutköp från Socialstyrelsens läkemedelsregister från 2005 och socioekonomiska data över utbildning, inkomst och födelseland från Statistiska centralbyrån [5].
Två populationer identifierades från ovanstående databaser:
Förmaksflimmerpatienter. Alla levande individer i Stockholms läns landsting som någon gång under perioden 2006–2010 respektive 2009–2013 haft en vårdkontakt med diagnos förmaksflimmer utan tidigare förekomst av diagnoskoder för mitralisstenos eller mekanisk klaff analyserades. Från data över uthämtade recept undersöktes hur många av dessa som under 2010 respektive 2013 någon gång hade hämtat ut warfarin, NOAK eller lågdos-ASA (Trombyl).
Riskstratifiering med CHA2DS2-VASc gjordes för alla individer med förmaksflimmer i landstinget 2009–2013. Ålder den 31 december 2013 användes för detta ändamål. Komorbiditet definierades som minst en förekomst av respektive diagnos i någon vårdform till och med den 31 december 2013. Se Fakta 1 för definitioner av komorbiditet.
Förmaksflimmerpatienter med nyinsättningar av warfarin, NOAK och ASA. Alla individer i Stockholms läns landsting med minst en förekomst av förmaksflimmerdiagnos 2003–2014 som hämtat ut warfarin, dabigatran, rivaroxaban, apixaban respektive ASA under perioden 1 april 2011–31 mars 2014, men som inte hämtat ut respektive läkemedel under de 9 månaderna närmast före detta tidsintervall (inkörningsperiod), identifierades från VAL. Varje preparat räknades separat, och en enskild individ kunde därför förekomma flera gånger.
Resultat
Förmaksflimmer och antikoagulantiabehandling
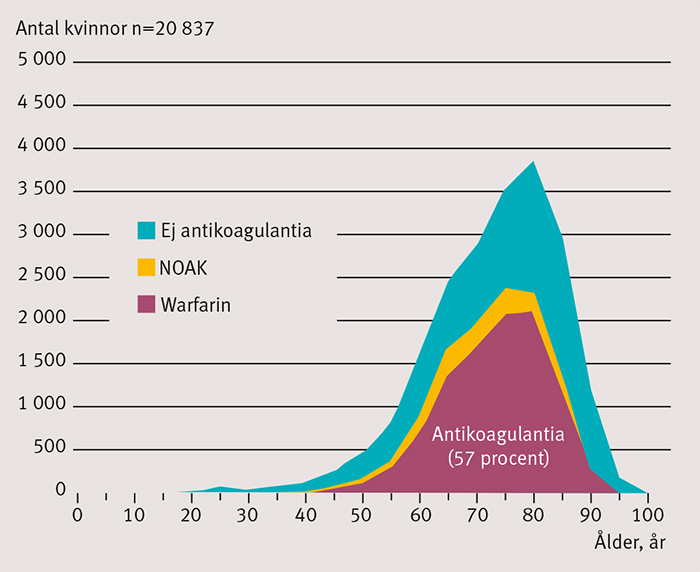
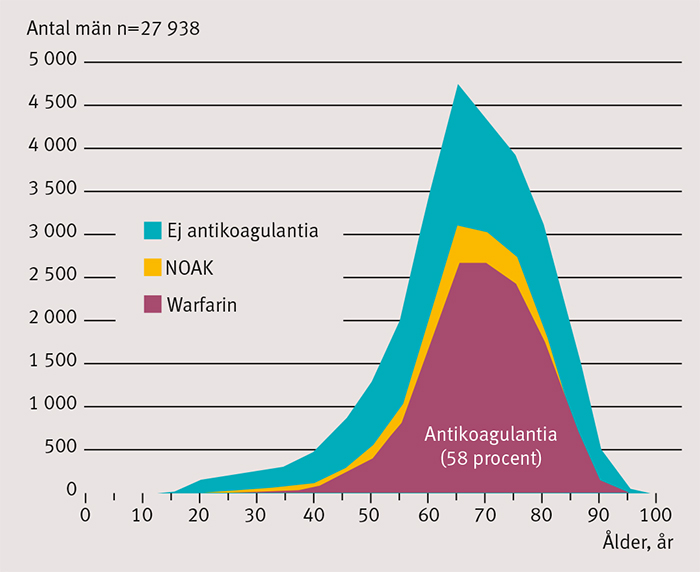
Av de 43 353 individerna med förmaksflimmerdiagnos 2006–2010 hade 47 procent hämtat ut warfarin under 2010. Kvinnor var i lägre utsträckning behandlade än män (kvinnor 44 procent, män 50 procent) [5]. Antalet personer med diagnosen förmaksflimmer hade stigit till 48 775 under perioden 2009–2013. Det innebär en ungefärlig prevalens av förmaksflimmer på 3,0 procent i den vuxna befolkningen i Stockholms läns landsting 2013. Av dessa hämtade 52 procent ut warfarin under 2013 medan 8 procent hämtade ut något NOAK-preparat – det senare gällde huvudsakligen individer under 80 år. Totalt var 58 procent antikoagulantiabehandlade 2013, varav lika stor andel män som kvinnor (Figur 1). Antalet antikoagulantiabehandlade i åldersgruppen 65–74 år hade ökat från 58 procent år 2010 till 67 procent år 2013. ASA-användningen minskade från 42 procent år 2010 till 29 procent år 2013.
Nyinsättningar av NOAK
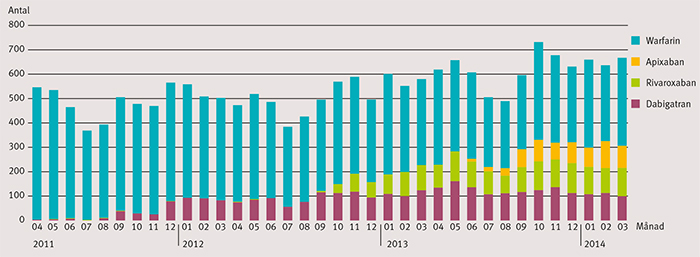
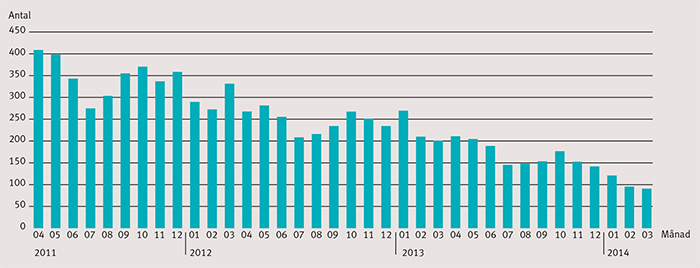
I VAL identifierades 14 088 individer som hade påbörjat behandling med warfarin, 3 078 med dabigatran, 1 732 med rivaroxaban, 666 med apixaban respektive 8 786 med ASA. Antalet personer som påbörjat antikoagulantiabehandling har ökat sedan början av 2011, och i början av 2014 förskrevs NOAK i närmare hälften av fallen, med en relativt jämn fördelning mellan de tre nya preparaten (Figur 2). Under samma period har nyinsättningarna av ASA minskat kraftigt (Figur 3).
Nyinsättningar av NOAK gjordes i första hand på akutsjukhusen och av privata specialistmottagningar (vilka utgjorde huvuddelen av »övriga vårdgivare«) (Tabell I). I primärvården förskrevs huvudsakligen warfarin vid nyinsättning, men även på akutsjukhusen förskrevs warfarin till 70 procent av patienterna (Tabell I).
Riskprofilen hos de patienter som påbörjat behandling med respektive antikoagulantium eller ASA kan ses i Figur 4. NOAK hade huvudsakligen hämtats ut av patienter med lägre strokerisk (enligt CHA2DS2-VASc) än de som hämtat ut warfarin eller ASA.
Diskussion
Det är viktigt att minska risken att drabbas av stroke hos patienter med förmaksflimmer. Vilken plats warfarin respektive NOAK kommer att ha som tromboembolisk profylax hos patienter med förmaksflimmer i framtiden är ännu oklart. Våra tidiga resultat från Stockholms läns landsting visar en markant ökad förekomst av patienter med diagnosen förmaksflimmer i registren sedan 2010, liksom en ökande andel som behandlas med antikoagulantia (där NOAK nu står för nästan hälften av nyinsättningarna) samt en kraftigt minskande förskrivning av ASA till patienter med förmaksflimmer. NOAK förskrivs framför allt till individer under 80 år samt till dem med 0–4 poäng enligt CHA2DS2-VASc, medan warfarin och ASA dominerar hos de äldsta och sjukaste med den högsta risken för stroke. NOAK-behandling har huvudsakligen initierats på sjukhus eller av privata specialistmottagningar och sällan i primärvården, vilket harmonierar med de aktuella rekommendationerna i landstinget. Framöver förväntas primärvården kunna ta över behandlingsansvaret för en del av dessa patienter samt även initiera behandling med NOAK i okomplicerade fall.
Introduktionen och marknadsföringen av NOAK har uppenbarligen ökat intresset för förmaksflimmer och har säkert bidragit till den ökade förekomsten av förmaksflimmerdiagnos som vi nu ser. Tillkomsten av 1 poäng vardera för vaskulär sjukdom, ålder 65–74 år och kvinnligt kön i riskskattningen med CHA2DS2-VASc har tydligt vidgat indikationerna för (NO)AK-behandling av patienter med förmaksflimmer [5]. NOAK synes vara ett vanligt alternativ till yngre patienter med låg–måttlig risk, och kvinnor får numera antikoagulerande behandling lika ofta som män. Förskrivningen av lågdos-ASA minskar påtagligt efter den omvärdering av detta behandlingsalternativ som skett nationellt och internationellt under senare år. Således befinner vi oss i en mycket dynamisk fas av omhändertagandet av patienter med förmaksflimmer.
Det finns ofta skillnader mellan resultaten från en klinisk prövning med noggrann selektion och tät uppföljning av patienterna och de resultat man kan förvänta sig i vardagssjukvård [35]. Frågan är hur väl studieresultaten för NOAK kan överföras till svensk sjukvård [19]. Kommer vi att ha samma goda behandlingseffekter med NOAK som med warfarin avseende risken att drabbas av stroke eller dö? Kommer vi att se färre hjärnblödningar hos dem som behandlas med NOAK jämfört med warfarin (om grupperna kan jämföras)? Kommer doseringarna att anpassas för patienter med komplicerande faktorer, som njursjukdom, eller interagerande läkemedelsbehandling? Kommer behandling av allt fler patienter med låg strokerisk att vara till godo för dessa patienter? Hur låg strokerisk är rimlig att motivera behandling med (NO)AK? Hur blir följsamheten till NOAK-behandling på lång sikt? I Sverige har vi med våra register och epidemiologisk metodik goda möjligheter att jämföra effekt och säkerhet hos NOAK och warfarin i vanlig sjukvård [36], och sådan uppföljning av behandlingspersistens samt risk för tromboembolism och blödning med de olika preparaten pågår i Stockholms läns landsting.
Utmaningar under de närmaste åren blir att öka kunskaperna om vilket läkemedel som passar bäst till respektive patient, vilka doser som bör användas samt hur behandlingarna bör följas upp avseende effekt, säkerhet och följsamhet. De nya medlen är inte okomplicerade eller ofarliga, och de bör hanteras med samma respekt som warfarin. Många patienter med förmaksflimmer är gamla och multisjuka med hög blödningsrisk. (NO)AK-behandling minskar strokerisken hos dessa patienter men medför fler blödningar. Användningen av NOAK har varit försiktig i denna patientgrupp, men samtidigt är det hos patienter över 80 år utan antikoagulantiabehandling som den stora strokebördan finns [37].
Handläggningen i samband med olika akuta tillstånd, blödningar eller invasiva procedurer kommer att ställa krav på bättre laboratoriediagnostik, väl underbyggda rutiner vid allvarlig blödning samt uppdateringar av vårdprogram i stora delar av den somatiska vården. I Stockholms läns landsting har studier inletts för att vid behov kunna monitorera NOAK med läkemedelsanalyser och nya koagulationstest. Målsättningen är att förbättra den akuta handläggningen av patienter med allvarliga blödningar eller behov av invasiva ingrepp samt att kunna individualisera doseringarna av NOAK hos patienter som kan förväntas ha andra dosbehov än de vanliga, t ex äldre med sänkt njurfunktion och/eller polyfarmaci. För dabigatran finns underlag för sådan individualisering [33], och vi har funnit en mycket stor variabilitet i koncentration och effekt även hos patienter som dosanpassats enligt aktuella rekommendationer [34]. Det blir en längre väg att vandra för rivaroxaban och apixaban, där det saknas publicerade data om relationerna mellan testresultat och riskerna för stroke respektive allvarlig blödning. En klok användning av metoder för att monitorera även NOAK bör kunna förbättra både effekt och säkerhet vid behandling med dessa läkemedel.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Gerd Lärfars, Håkan Wallén, Rickard Malmström, Jan Hasselström och Sven-Åke Lööv, Stockholm, är, liksom författarna, ledamöter i projektet »Införande av nya orala antikoagulantia i Stockholms läns landsting«, deltar i arbetet med bakgrundsdokumentation och står bakom rekommendationerna.
Jamilette Mirande Tellez, Thomas Cars och Sten Ronge, Stockholm, har bidragit med programmering och statistik.
Fakta 1. Definitioner av komorbiditet (ICD-kod)
Förmaksflimmer (I48)
Diabetes (E10–E14)
Hjärtsvikt (I50)
Hypertoni (I10–I15)
Ischemisk stroke, arteriell embolism och stroke, ospecificerad (I63, I64, I679, I693, I694, I698, I67-, I69-, Z866, Z867, G450, G451, G452, G453, G458, G45.9, G45-, I74)
Mekanisk klaff (FCA60, FCA70, FDC10, FGE00, FGE10, FGE20, FGE96, FJF00, FJF10, FJF12, FJF20, FJF96, FKD00, FKD10, FKD20, FKD96, FMD00, FMD10, FMD12, FMD13, FMD20, FMD30, FMD40, FMD96)
Mitralisstenos (I050, I052, I342)
Vaskulär sjukdom (I20-I25, I70, I739)