I uppdaterade riktlinjer för läkemedelssäkerhet nämns behovet av fler metoder för uppföljning av riskminimerande åtgärder.
Aggregerad statistikbeställning från nationella hälsodataregister kan användas för att resurseffektivt utvärdera kontraindikationer.
I Sverige följs kontraindikationer för cyproteronbehandling av patienter med meningeom.
Läkemedelsverket, i samarbete med övriga läkemedelsmyndigheter inom EU, bevakar fortlöpande säkerheten kring läkemedel. Vid upptäckt av nya risker finns olika nivåer av riskminimerande åtgärder.
Den vanligaste och enklaste åtgärden är uppdatering av läkemedlets produktinformation under sektion 4.8, »Biverkningar«. Nästa steg är informationen under sektion 4.4, »Varningar och försiktighet«, där åtgärder för att minska risken eller minska skadeverkan av risken beskrivs. En uppdatering av sektion 4.3, »Kontraindikationer« utgör en ytterligare skärpning för att minska risken genom att utesluta en definierad grupp av patienter som på gruppnivå bedömts sakna en positiv nytta–riskbalans vid läkemedelsanvändningen. Beroende på riskens allvarlighetsgrad kan en uppdatering av produktinformationen förstärkas genom att skicka ut informationen till alla tänkbara förskrivare genom så kallade DHPC-brev (Direct healthcare professional communication).
Om inte risken bedöms kunna minskas genom uppdatering av produktinformationen så kan innehavaren av försäljningstillståndet åläggas att skapa ytterligare informationsmaterial, vilka definieras som villkor i läkemedlens godkännande, så kallade villkorade utbildningsmaterial.
Utvärdering av riskminimerande åtgärder
Inom det europeiska regelverk som definierar processer för läkemedelsgodkännande betonas att man ska utvärdera riskminimerande åtgärder. Historiskt sett har detta oftast skett genom att förskrivare tillfrågas i enkätform. Svarsfrekvensen brukar generellt vara låg (<10 procent) [1], och vid en genomgång 2023 bedömdes att upp till en tredjedel av enkätstudierna inte var konklusiva [2]. I den nyligen uppdaterade riktlinjen betonas att man behöver använda kompletterande metoder för att utvärdera riskminimerande åtgärder [3].
Vi skulle vilja illustrera med ett exempel på införd kontraindikation. Cyproteron godkändes första gången 1978 för hämning av könsdriften vid sexuella avvikelser och/eller hypersexualitet hos män, eller för behandling av uttalad hirsutism hos kvinnor i fertil ålder. Cyproteron är också i lägre doser och i kombination med etinylestradiol godkänt för behandling av måttlig till svår akne relaterad till androgenkänslighet. Effekter av gulkroppshormon ger påverkan på meningeom [4]. Epidemiologiska studier har visat på en ökad risk för diagnostisering av meningeom hos patienter som behandlats med cyproteron [5, 6].
I november 2009 fastställde Pharmacovigilance Working Party, dåtidens arbetsgrupp för läkemedelssäkerhet inom EU, risken för meningeom vid långvarig behandling med cyproteron i doser >25 mg dagligen, och varningar och kontraindikation införs för behandling av patienter med aktuellt eller tidigare behandlat meningeom.
I april 2020 rekommenderade Pharmacovigilance Risk Assessment Committee (PRAC), nuvarande europeiska läkemedelssäkerhetskommittén, att doser över 10 mg till kvinnor enbart skulle användas om andra alternativ eller doser inte fungerat. I samband med detta skickas även ett DHPC-brev till berörda läkare [7]. Cyproteron i lägre doser (≤2 mg) och kombinationer har inte visat någon ökad risk för meningeom, men har av försiktighetsskäl samma kontraindikation.
Förra året publicerades en webbaserad enkätstudie med frågor kring kunskapen om indikationer för cyproteronbehandling. I studien tillfrågades 10 579 förskrivare av cyproteron; 613 (6 procent) besvarade hela enkäten, varav 73 procent korrekt angav att man skulle avsluta behandling av patienter som utvecklat eller haft meningeom [8]. Studien tolkades som att kunskapen om kontraindikation finns. Undersökningen inkluderade dock inte svenska förskrivare, men väl europeiska, och svarsfrekvensen var som ofta låg.
Aggregerad statistik som komplement
Vid frågeställningar om just kontraindikation kan man utnyttja nationella hälsodataregister för att få en uppfattning om omfattningen av samtidig behandling av receptuttagna läkemedel och kontraindicerad diagnos i de fall de återfinns i registren. Läkemedelsverket gjorde därmed en beställning av aggregerad statistik till Socialstyrelsen av antal incidenta och prevalenta individer (äldre än 10 år) uppdelade per kalenderår för diagnosen meningeom och uttag av läkemedel med cyproteron.
Diagnosen meningeom söktes dels i Patientregistret som två vårdtillfällen eller läkarbesök inom ett år med huvuddiagnos ICD-10 D32* under perioden 2005–2022 men utan vårdtillfällen med aktuell diagnos 2000–2004, där första vårdtillfälle enligt detta kriterium räknas som första diagnostillfälle. Sökning gjordes även i Cancerregistret med ICD-kod C70* och med tumörens morfologiska diagnos enligt ICD-O-3-koder under perioden 2005–2022 men inte 2000–2004.
Läkemedelsregistret användes för att bland patienter med meningeom identifiera individer med en första förskrivning av cyproteron (antingen enbart cyproteron (ATC-kod G03HA01) eller cyproteron med östrogen (G03HB01) mellan 2005 och 2023, men fria från cyproteronbehandling året före. I aggregerad statistikbeställning är det minsta antal individer som kan redovisas 4 eller fler; mindre antal redovisas som småtal (1–3).
Antalet personer som tagit ut recept med cyproteron (ATC-kod G03HA01) har under perioden legat konstant runt 1 000 per år, varav ca 70 procent män.
Antalet personer med kombinationsbehandling med cyproteronöstrogen (ATC-kod G03HB01) har däremot sjunkit från cirka 8 000 år 2010 till drygt 4 000 personer år 2023, och gruppen utgörs av kvinnor.
Mellan år 2005 och 2022 har totalt 13 036 patienter diagnostiserats med meningeom, varav 9 361 (72 procent) är kvinnor. Bland dem som diagnostiserats har 21 till 63 personer (1,6–4,8 promille) tagit ut recept på cyproteron eller cyproteron och östrogen någon gång efter diagnosen.
Vi har använt nationella register för att studera förekomst av samtidig behandling med cyproteron för patienter som har haft eller har diagnosen meningeom. Data utgörs av en aggregerad statistikbeställning från Socialstyrelsen, och redovisningen av värden mellan 1 och 3 som en enhet medför minskad precision. Det ger dock en fingervisning om storleksordningen. Detta tillvägagångssätt har vägts emot det extra arbete som skulle krävas om uppföljningen gjordes som en forskningsstudie med mikrodata: etikprövning, beställning av data på individnivå från flera olika register, dataöverföring, datarensning och analys i säker miljö på Läkemedelsverket. Det extra arbete som skulle läggas på hälso- och sjukvården för att besvara en enkätstudie vars tolkning är beroende av svarsfrekvens, vilken erfarenhetsmässigt brukar vara låg, bedömdes inte vara kostnadseffektiv.
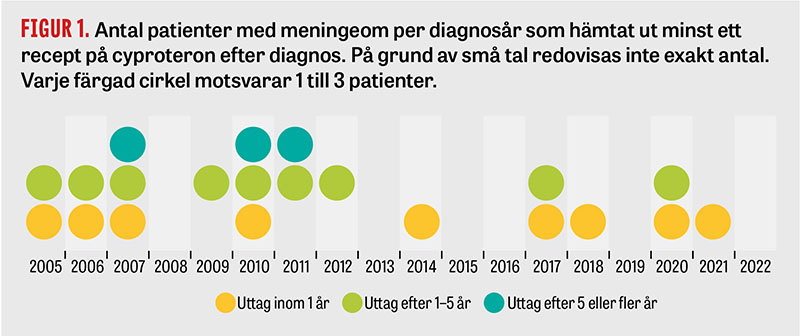
Resultatet talar för att det förekommer enstaka patienter (beroende på redovisningen av småtal mellan 21 och 63 patienter) som behandlats med cyproteron trots att de har meningeom (Figur 1). Felkodning av meningeom i registren skulle kunna vara en förklaring, men är kanske inte så trolig i det här fallet, då vi krävt två vårdtillfällen eller läkarbesök med registrerad meningeomdiagnos. En anledning till behandling trots meningeom skulle kunna vara att behandlande läkare inte känner till att patienten har meningeom eller inte känner till att meningeom är en kontraindikation för behandling med cyproteron, men kunskapen kan också ha funnits och behandlingen skett efter att risken har vägts i förhållande till den enskildes behov.
Det kan också noteras att majoriteten av uttagen har gällt kombinationen cyproteron (2 mg) och etinylestradiol, som innebär att det tar längre tid innan man kommer upp i de kumulativa doser som har visats öka risken, men uppdelning i ATC-koder har inte gjorts i denna enkla studie. Över lag följer förskrivare kontraindikationen. För det fåtal patienter som trots kontraindikation fått cyproteron förskrivet skulle det behövas en journalgranskning för att fastställa kontraindikation och orsak till behandling.
I detta exempel ger antalet inte anledning till ytterligare regulatoriska åtgärder, och aggregerad statistikbeställning från nationella hälsodataregister förefaller vara en resurseffektiv metod för att följa upp att den svenska förskrivarkåren följer den rekommendation som anges i produktinformationen angående risken med cyproteronbehandling hos patienter med tidigare eller aktuellt meningeom.
Framtida arbete
För att kunna följa fler av de riskminimerande åtgärder som läkemedelsmyndigheter inför behöver vi resurseffektiva metoder. Statistikbeställning av aggregerade hälsodata kräver inte lika mycket arbete som regelrätta studier, men är mindre precis och kan inte användas för läkemedel som förordnats på rekvisition. Just följsamheten till kontraindikationer förefaller vara lämplig att följa med aggregerad statistik från hälsodataregister, men behöver studeras med fler exempel och utveckling av kriterier för vilket brytvärde som ska anses vara acceptabelt.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.