Escherichia coli som producerar ESBLCARBA, vilket bryter ner karbapenemer, har blivit allt vanligare utomlands. Stammar som producerar NDM-1 uppfattas som ett stort hot, eftersom de är multiresistenta och ökar snabbt globalt.
De fall av NDM-1 som tidigare påvisats i Sverige har isolerats från patienter som blivit koloniserade i samband med resa eller vård utomlands. Vi presenterar här det första kända fallet av sepsis med NDM-1-producerande E coli i Sverige.
Det krävs en hög beredskap på samtliga vårdenheter för att hantera en ökad förekomst av multiresistenta tarmbakterier. Karbapenemer bör användas restriktivt för att undvika selektion av ESBLCARBA-producerande stammar.
ESBL (extended-spectrum beta-lactamases) är enzymer som inaktiverar betalaktamantibiotika och som kan finnas hos bl a tarmbakterierna Klebsiella pneumoniae och Escherichia coli. ESBLA bryter ner cefalosporiner (t ex Zinacef och Claforan) och ESBLCARBA även karbapenemer (t ex Tienam och Meronem). Infektioner med ESBLCARBA-producerande stammar är svårbehandlade, eftersom enzymerna medför resistens mot de preparat som är förstahandsval vid allvarliga infektioner med dessa bakterier. Stammarna är i hög utsträckning resistenta även mot flera andra antibiotikaklasser, exempelvis kinoloner, trimetoprim och aminoglykosider, men i de flesta fall är de känsliga för kolistin, tigecyklin och fos-fomycin.
Ännu finns otillräcklig kunskap om hur infektioner med dessa bakterier ska behandlas, men det råder enighet om att kombinationsbehandling med två eller flera antibiotika är mer effektiv än monoterapi.
Plasmider som kodar för ESBLCARBA kan överföras mellan bakterier av samma eller olika arter. Det finns flera olika typer av ESBLCARBA, t ex KPC, OXA, VIM, IMP och NDM. Den som rönt störst uppmärksamhet på senare tid är NDM-1 (New Delhi metallobetalaktamas-1). Det första kända fallet av NDM-1-producerande K pneumoniae isolerades 2008 från en svensk patient, som nyligen hade fått sjukhusvård i New Delhi, Indien, på grund av en glutealabscess [1]. I Indien och andra delar av Asien finns NDM-1 endemiskt och har hittats i bl a dricksvattnet [2]. I en studie från Pakistan var så mycket som 14 procent av öppenvårdspatienter och 27 procent av inneliggande patienter bärare av NDM-1-producerande bakterier i tarmen [3].
Under det senaste året har det också rapporterats om fynd av ESBLCARBA-producerande tarmbakterier hos slaktdjur [4].
ESBLCARBAär sedan mars 2012 en anmälnings- och smittspårningspliktig infektion enligt smittskyddslagen. Den 1 mars 2013 hade totalt 25 NDM-1-producerande isolat påvisats. Frånsett det fall som rapporteras nedan har det uteslutande rört sig om fall med isolat från sår, tarm eller urin [Petra Edquist, Smittskyddsinstitutet, Stockholm, pers medd; 2013]. Internationellt har NDM-1-producerande E coli och K pneumoniae påvisats som orsakande agens vid sepsis, urinvägs-, sår- och bukinfektioner samt ventilatorassocierade pneumonier [5].
Fallbeskrivning
En man född på 1920-talet med sedan tidigare mekanisk aortaklaff, ischemisk hjärtsjukdom, biventrikulär pacemaker, förmaksflimmer, hjärtsvikt och njurinsufficiens (habituellt kreatininvärde ca 200 µmol/l) hade vårdats på Helsingborgs lasarett under slutet av oktober månad 2012 på grund av sepsis med växt av Staphylococcus aureus i blododlingarna. Patienten var bosatt i villa med sin fru. Han hade hjälp av hemtjänst och bar blöja på grund av feces- och urininkontinens. Det fanns inga djur i hemmet, och han hade inte varit utomlands de senaste åren.
På grund av flera faktorer avstod man från att utreda patienten vidare med transesofagealt ultraljud avseende endokardit. Antibiotikabehandling gavs i 14 dagar med kloxacillin (Ekvacillin). Han hade vid vårdtillfället en tillfällig KAD som avvecklades före utskrivningen. Då patienten ansågs medicinskt färdigbehandlad, vårdplanerades han och flyttades till ett korttidsboende.
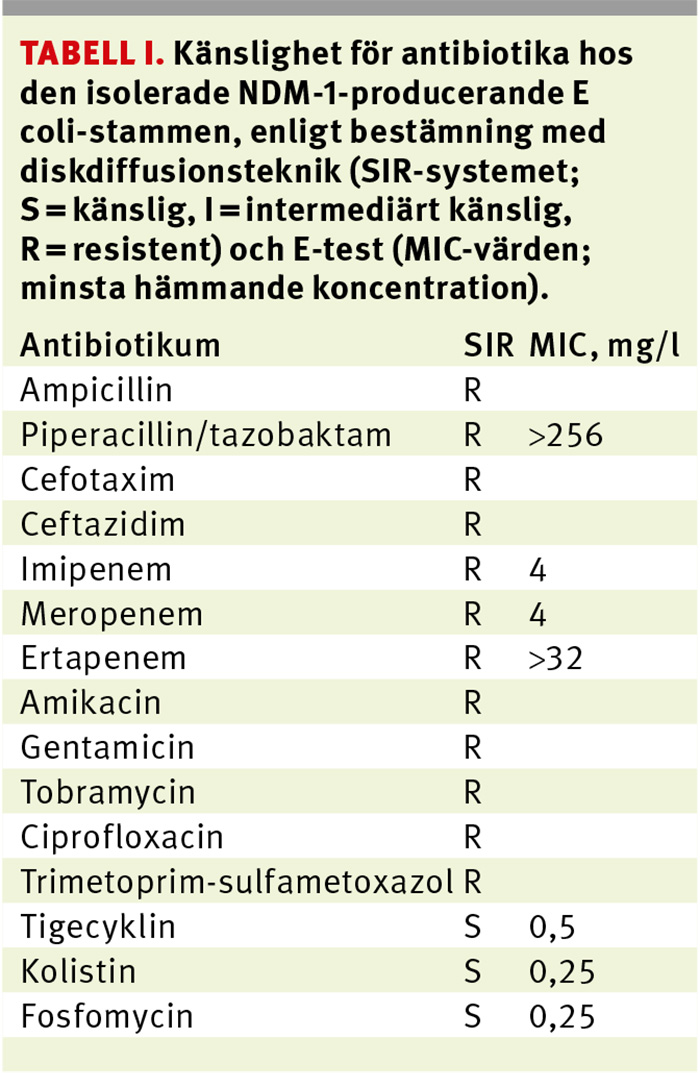
Cirka 1 månad senare sökte patienten akut på Helsingborgs lasarett på grund av feber. Han var vid ankomsten feberfri men påverkad i vitala parametrar med hypotoni, takypné och konfusion. Han hade haft KAD av och till sedan föregående vårdtillfälle, och en sådan hade avvecklats på korttidsboendet 2 dagar före sjukhusbesöket. Man misstänkte därför urinvägsinfektion, och empirisk sepsisbehandling sattes in med cefotaxim (Claforan). I blododlingarna tagna vid ankomst växte karbapenemresistenta E coli, som producerade ESBLCARBA av typ NDM-1. Ingen urinodling togs innan antibiotikabehandling sattes in. Efter blododlingssvaret odlade man från rektumsekret, där E coli med samma resistensmönster som i blod påvisades. Bakterien var känslig endast för tigecyklin, kolistin och fosfomycin (Tabell I).
När blododlingssvaret med resistensbestämning anlänt ersattes cefotaxim med tigecyklin (Tygacil). Efter en initial dos 100 mg ordinerades 50 mg × 2. Total behandlingstid med tigecyklin var 14 dagar. På grund av njursvikt avstod man från kolistinbehandling. Patienten förbättrades kliniskt och skrevs efter 21 dagars vårdtid ut till hemmet med insatser från hemtjänsten.
En dryg vecka efter utskrivning inkom patienten återigen till sjukhus efter ett mindre falltrauma i hemmet, och han lades in på infektionskliniken. Patienten hade ingen feber eller andra tecken på infektion, men återigen växte NDM-1-producerande E coli i blododlingarna med samma resistensmönster som vid föregående vårdtillfälle. Denna gång dubbelbehandlades patienten med tigecyklin 50 mg × 2 och kolistin (Tadim) 1 miljon IE × 2 i totalt 14 dagar. Ingen kreatininstegring eller andra biverkningar noterades under behandlingen. Blod och urinodlingar utföll negativa ca 10 dagar in i behandlingsförloppet, och patienten kunde skrivas ut i sitt habitualtillstånd.
Smittspårning initierades av Smittskydd Skåne tillsammans med enheten för vårdhygien på Helsingborgs lasarett. Personer på samma vårdboende och de patienter som patienten delade rum med vid föregående vårdtillfälle på lasarettet screenades med fecesodling. Hittills har ytterligare ett fall av kolonisation med NDM-1-producerande E coli påvisats hos en person på samma boende. Stammen är identisk med den som isolerades från patienten, enligt genetiska analyser utförda på Smittskyddsinstitutet (PCR [polymeraskedjereaktion] och PFGE [pulsfältsgelelektrofores]).
Diskussion
Vår fallrapport är ett exempel på det ökande problemet med antibiotikaresistens hos gramnegativa bakterier. Fallet är unikt, eftersom det är det första av sepsis med NDM-1-producerande E coli i Sverige och eftersom patienten inte hade vistats utomlands före insjuknandet. Ytterligare en person på boendet visade sig vara bärare av samma bakteriestam, vilket talar för en spridning inom vården.
Flera studier har visat att friska utlandsresenärer ofta blir bärare av ESBLA-producerande E coli i tarmfloran, och på samma sätt sprids troligen ESBLCARBA-producerande stammar lätt mellan länder [6]. Dagens semestervanor med frekventa utlandsresor gör att mörkertalet av människor som är koloniserade av multiresistenta tarmbakterier i samhället är stort. Det är ytterst angeläget att det finns en beredskap och plan för vårdhygieniska åtgärder vid konstaterade fall för att förhindra utbrott på sjukhus och andra vårdinstutitioner. Men eftersom förekomsten av multiresistenta bakterier i tarmfloran inte ger några symtom och inneliggande patienter inte rutinmässigt screenas för förekomst av resistenta stammar, är bärarskapet i de flesta fall inte känt. Därför är det av vikt att basala hygienrutiner ständigt efterföljs för att förhindra spridning av resistenta bakterier på sjukhus och vårdhem.
Begränsad evidens för behandling
Evidensen för hur infektioner med ESBLCARBA-producerande E coli och K pneumoniae ska behandlas är i dag mycket begränsad och baseras på fallrapporter, resultat från okontrollerade retrospektiva kliniska studier och in vitro-studier. Kombinationsbehandling har i flera kliniska studier varit förknippad med lägre mortalitet än monoterapi, även då bakterierna är känsliga för de enskilda preparaten [7]. Behandlingsalternativen för infektioner med NDM-1-producerande bakterier är få på grund av hög förekomst av kopplad resistens mot flera antibiotikaklasser, men majoriteten av stammarna är känsliga för tigecyklin, kolistin och fosfomycin [8].
Tigecyklin är en tetracyklinanalog med bakteriostatisk effekt som verkar genom hämning av bakteriernas proteinsyntes. Preparatet har varit förknippat med högre mortalitet än jämförelsepreparat vid allvarliga infektioner och rekommenderas endast när det inte finns andra alternativ [7]. Tigecyklin är inte är godkänt för behandling av urinvägsinfektioner.
Kolistin har använts i hög utsträckning vid infektioner med ESBLCARBA-producerande stammar och ofta i kombination med tigecyklin, en karbapenem eller en aminoglykosid [9, 10]. Fortfarande råder dock osäkerhet om hur preparatet ska doseras optimalt med avseende på effekt och njurtoxicitet, som är vanligt förekommande men i regel reversibel [11].
Parenteralt fosfomycin används internationellt vid behandling av multiresistenta stammar när andra alternativ saknas [10], men några kliniska studier av behandlingseffekten finns inte, och preparatet är inte registrerat i Sverige.
Karbapenemer måste användas restriktivt
Det är viktigt att det finns en hög beredskap på samtliga vårdenheter i landet för att hantera ökad förekomst av multiresistenta tarmbakterier. Laboratorierna måste ha fungerande rutiner för att detektera ESBLCARBA och annan uppseglande resistens. Vårdhygienen måste vara anpassad för att förhindra spridning av resistenta stammar vid konstaterade fall, vilket kräver tillräckligt antal isoleringsrum på sjukhusen och rimlig arbetsbelastning för personalen. Basala hygienrutiner måste fungera tillräckligt väl för att förhindra smittspridning utgående från asymtomatiska bärare av resistenta bakterier.
Behandlande läkare måste vara medvetna om den ökade risken för resistens vid gramnegativa infektioner hos patienter som nyligen vistats i områden med hög förekomst av ESBL eller som har andra riskfaktorer för resistenta bakterier. Det kan kräva anpassning av empirisk terapi för kritiskt sjuka patienter, eftersom fördröjd effektiv behandling är förknippad med ökad mortalitet i dessa fall. Varje infektionsläkare måste ha viss kunskap om hur infektioner med ESBLCARBA-producerande stammar ska behandlas.
Samtidigt är det angeläget att även fortsättningsvis använda karbapenemerna restriktivt för att minska risken för selektion av ESBLCARBA-producerande E coli och K pneumoniae. Det kommer att ha allt större betydelse, eftersom en ökande andel av våra patienter är bärare av karbapenemresistenta stammar. Genom att undvika onödig användning av karbapenemer kan vi fördröja ökningen av ESBLCARBA i Sverige.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Läs även Kommentar:
ESBL-CARBA kan bli ett problem i svensk sjukvård