Prematuritetsretinopati (ROP) gör årligen 20 000 barn blinda eller gravt synskadade.
I Sverige drabbas framför allt barn födda före 28 gestationsveckor, men vid mindre utvecklad vård drabbas även mer mogna barn.
Syrgasbehandling och dålig tillväxt är betydande riskfaktorer.
Neonatal viktutveckling kan användas för att förutspå prematuritetsretinopati.
Hämmad neurovaskulär tillväxt i retina följs i svåra fall av patologisk kärlnybildning, näthinneavlossning och blindhet.
Laserbehandling kan oftast förhindra blindhet.
Anti-VEGF-behandling används allt oftare men evidens saknas för bland annat säkerhet.
Forskningen bör inriktas på prevention som främjar det prematurfödda barnets tillväxt och utveckling.
För tidigt födda barn har ökad risk för synproblem på grund av prematuritetsretinopati (ROP) och hjärnskador. Årligen blir cirka 20 000 barn blinda eller gravt synskadade på grund av prematuritetsretinopati världen över. I länder med väl utvecklad neonatalvård drabbas framför allt de mest omogna barnen. I vissa länder i Asien, Östeuropa och Latinamerika där neonatalvården blivit tillräckligt bra för att omogna barn ska överleva men inte bra nog för att förhindra allvarlig ROP, och där screeningsystem och behandlingsmöjligheter saknas, är blindhet på grund av ROP ett stort problem [1].
Prematuritetsretinopati har länge betraktats som en kärlsjukdom som beror på syrgasbehandling, men det är inte bara blodkärlen som drabbas, och syrgas är bara en av riskfaktorerna. Normalt växer retinas blodkärl ut från synnervspapillen vid cirka 14 veckors gestationsålder och i fullgången tid är vaskulariseringen klar. Kärltillväxten stimuleras av en »fysiologisk hypoxi« som uppstår då den perifera delen av retina mognar, och denna hypoxi stimulerar bland annat vaskulär endotelial tillväxtfaktor (VEGF) [2].
Vid prematuritetsretinopati ser man en fördröjd retinal vaskularisering som i allvarligare fall följs av okontrollerad kärltillväxt som kan leda till näthinneavlossning och blindhet. Nedsatt retinal funktion vid elektroretinografi har rapporterats på barn som haft ROP, och nya undersökningsmetoder som optisk koherenstomografi, som visualiserar ögats olika lager, har visat att även neural vävnad är påverkad. Prematuritetsretinopati kan således betraktas som en neurovaskulär sjukdom [3].
Patogenes och riskfaktorer
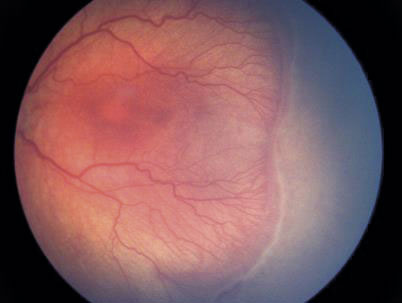
Prematuritetsretinopati har två faser. Fas 1 startar direkt efter födelsen och karakteriseras av hämmad kärltillväxt och förlust av redan bildade blodkärl. I fas 2, efter cirka 30 veckors postmenstruell ålder, uppträder de synliga förändringarna med en skarp avgränsning mellan vaskulariserad och avaskulär näthinna och, i svårare fall, ohämmad kärltillväxt i detta område (Figur 1).
De bäst kända riskfaktorerna är låg gestationsålder och syrgasbehandling. Man vet fortfarande inte vilka nivåer av syremättnad som är optimala. Där syrgas ges utan kontroll kan även fullgångna barn bli blinda. Ju mer omoget barnet är vid födelsen desto större är risken för synhotande prematuritetsretinopati. Perifera delar av retina är outvecklade och det omogna barnet har begränsad förmåga att ställa om sin energiomsättning från anaerob glykolys till oxidativ fosforylering av fett som behövs för att tillgodose det ökade energibehovet efter födelsen [4-6]. Mycket för tidigt födda barn har svårigheter att tillgodogöra sig tillräckligt med näring under de första veckorna efter födelsen och har en långdragen relativ viktnedgång.
På senare år har forskning visat ett starkt samband mellan dålig neonatal viktutveckling och låga koncentrationer av insulinliknande tillväxtfaktor 1 (IGF-1) och senare utveckling av prematuritetsretinopati (Figur 2) [7].
Under fosterstadiet är IGF-1 en viktig tillväxtfaktor vars produktion styrs av tillgången på glukos från mamman. IGF-1 kan ses som en indikator på näringstillstånd. Fett används inte som energi av fostret i någon större omfattning men det sker en selektiv överföring via placenta av framför allt långkedjiga fleromättade fettsyror som har betydelse för struktur och funktion av membran, för neuronal funktion och metabolism. Långvarig parenteral nutrition är en riskfaktor för prematuritetsretinopati [8], och betydande mängder fett tillförs under en period när fettillförseln normalt är liten. Nu använda lipidlösningar saknar eller har lågt innehåll av de långkedjiga fleromättade fettsyror som har avgörande betydelse för uppbyggnad och funktion av retina, hjärna och andra organ.
Det verkar saknas samband mellan postnatalt tillförd nutrition och IGF-1 i serum och utveckling av vikt (standardavvikelse) före 30 veckor postmenstruell ålder, vilket indikerar att barnen har problem att tillgodogöra sig tillförd näring dessförinnan [9]. Efter cirka 30 veckor stiger IGF-1 ofta och tillväxten ökar samtidigt som prematuritetsretinopati börjar blir synlig i ögonbotten. I den andra fasen uppstår hypoxi i den perifera avaskulära näthinnan när metabolismen där ökar, och VEGF stimulerar kärlnybildning.
Således karakteriseras första fasen av hyperoxi och varierande syrgasnivåer tillsammans med näringsunderskott, låga IGF-1-nivåer och dålig tillväxt, medan den andra fasen präglas av ökande generell tillväxt och retinal hypoxi, patologisk kärlnybildning och näthinneavlossning.
Det krävs en viss mängd IGF-1 för VEGF-stimulerad kärltillväxt i ögat [10]. Redan på 1950-talet visade Bo Hellström i en musmodell att nyfödda möss som exponerades för syrgas fick mer patologisk kärlnybildning när de började andas vanlig luft om de fått lite mat under syrgasbehandlingen än om de ätit normalt [11].
Infektioner som svampinfektioner [12] och sepsis [13] är riskfaktorer för allvarlig prematuritetsretinopati och genetiska faktorer har betydelse [14].
Prematuritetsretinopati uppträder ofta tillsammans med andra prematuritetsrelaterade tillstånd som neurologiska problem, dålig tillväxt av hjärnan, nekrotiserande enterokolit, intraventrikulär blödning och bronkopulmonell dysplasi [15].
Klassifikation
Klassifikationen av sjukdomens olika stadier baseras på det man ser vid oftalmoskopi: hur långt ut från synnervspapillen som det finns retinala blodkärl, hur gränsen mellan vaskulariserad och avaskulär näthinna ser ut och eventuell förekomst av patologisk kärlnybildning där (Figur 1).
Centrala förändringar innebär att en stor del av näthinnan saknar blodkärl och är allvarligare än perifera förändringar. Dilaterade och slingriga centrala kärl är ett illavarslande tecken som kallas plussjukdom (Figur 3), och indikerar att barnet behöver behandlas [16].
Screening
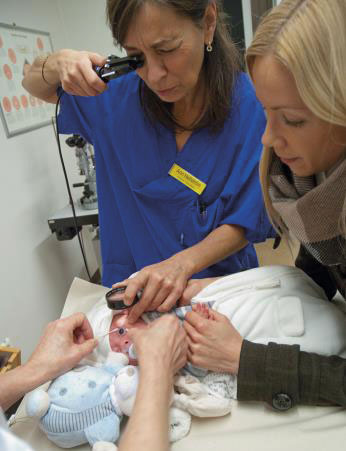
För att upptäcka prematuritetsretinopati krävs regelbundna ögonundersökningar (screening). På grund av att risken för synhotande prematuritetsretinopati varierar med bland annat vårdens kvalitet krävs olika inklusionskriterier för screening i olika populationer. I Sverige ögonundersöks alla barn som fötts med <31 veckors gestationsålder (Figur 4), och det är ovanligt att barn med en gestationsålder på >28 veckor behöver behandlas för prematuritetsretinopati.
Sedan 2008 finns ett nationellt kvalitetsregister (SWEDROP) med vars hjälp man kunnat modifiera gällande screeningkriterier [17, 18]. En populationsbaserad studie av neonatal morbiditet hos extremt prematurfödda barn i Sverige (EXPRESS) genomfördes 2004–2007. Av barn födda med gestationsålder <27 veckor utvecklade 73 procent ROP och 35 procent svår ROP [19], men man fann stora regionala skillnader [20]. Den rapporterade incidensen är avhängig både neonatalvårdens och screeningens kvalitet, och nationella kvalitetsregister som SWEDROP kan bidra till förbättrad vård.
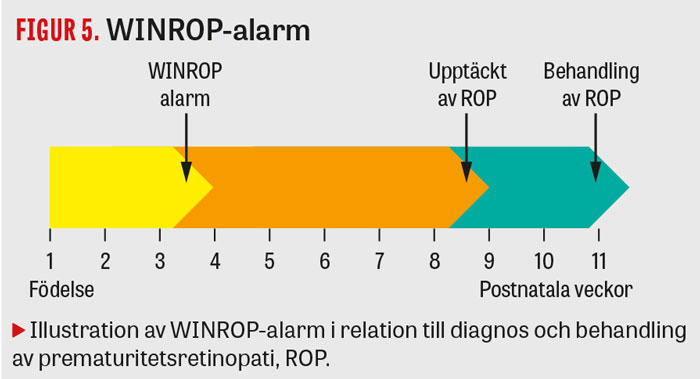
Ögonundersökningarna är ofta smärtsamma, och mindre än 5 procent av dem som undersöks utvecklar svår prematuritetsretinopati och behöver behandling. I genomsnitt görs 5–6 undersökningar per barn under ett par månaders tid [18]. Om urvalskriterierna kunde förfinas genom att även andra riskfaktorer än gestationsålder vägdes in i en bedömning av barnets risk för behandlingskrävande prematuritetsretinopati skulle barnen kunna besparas många undersökningar. I detta syfte utvecklades algoritmen WINROP (weight, IGF-1, neonatal, ROP) som med hög sensitivitet och något lägre specificitet, baserat på veckovis utveckling av vikt och serum-IGF-1, kan förutspå allvarlig ROP veckor till månader innan svår ROP konstateras (Figur 5) [7].
WINROP visade sig fungera lika bra baserat på enbart veckovisa vikter, utan blodprov för IGF-1, från födelsen fram till 32 veckors postmenstruell ålder, alltså under den första fasen av ROP [21]. WINROP har validerats på mer än 10 000 barn i bland annat Sverige [22], USA och Kanada [23], Brasilien [24], Schweiz [25] samt Mexiko [26]. Sensitiviteten har varit mycket hög i populationer liknade den svenska men i andra har man funnit lägre sensitivitet vilket kan bero på att andra riskfaktorer som till exempel okontrollerad syrgasbehandling har större betydelse där. WINROP, som finns tillgänglig på nätet utan kostnad, används på många kliniker som ett komplement till ordinarie screening. Andra liknande prediktionsmodeller baserade på viktutveckling har utvecklats men inte validerats i större populationer [27-29].
Behandling med laser ges efter väl definierade kriterier och syftar till att förhindra näthinneavlossning [30], men är destruktiv och förstör den perifera avaskulära näthinnan. I ökande omfattning världen över används också »off-label«-injektioner med anti-VEGF-antikroppar in i glaskroppen trots att forskning saknas om säkerhet med denna behandling som sänker cirkulerande VEGF på mycket omogna individer under flera månader [31].
Långtidseffekter
Både prematuritetsretinopati och mycket för tidig födelse i sig påverkar ögonens struktur och funktion. Det är ofta omöjligt att avgöra i vilken grad en synnedsättning beror på ögon- och/eller hjärnskada. Karakteristiskt för cerebral synnedsättning är visuella perceptionsproblem som svårigheter att bedöma nivåskillnader, hitta en sak bland många, orientera sig eller att känna igen ansikten.
I EXPRESS-studien har barnen följts upp till 6,5 års ålder. Då var 2 procent av dem blinda, ytterligare 3 procent var synskadade och totalt 9 procent hade synskärpa <0,5. I kontrollgruppen var inga blinda, 0,7 procent synskadade och 1 procent hade synskärpa <0,5. Glasögon hade ordinerats till 36 procent av de prematurfödda barnen, och 17 procent skelade. I kontrollgruppen bar 6 procent glasögon och ingen skelade [32].
Destruktion av den perifera näthinnan med laser minskar synfältets utbredning, men denna påverkan har visat sig vara mindre än befarat [33]. Retinas stavar utvecklas intensivt under tredje trimestern. Persisterande stavdysfunktion har setts vid elektroretinografi (ERG) på barn som haft prematuritetsretinopati [3]. Vid optisk koherenstomografi har man sett avsaknad av eller onormalt liten foveal avaskulär zon liksom förtjockad central retina på grund av att inre lager inte migrerat från fovea på ett normalt sätt. Man har inte funnit något samband mellan dessa förändringar och synskärpa i barndomen [34].
Prevention och behandling i framtiden
Behandling med laser kan i allmänhet förhindra blindhet men är destruktiv för näthinnan och bidrar inte till att näthinnan utvecklas normalt. Anti-VEGF-behandling används allt mer trots brist på studier om dosering och säkerhet hos prematurfödda, och dess plats som behandlingsalternativ behöver utforskas bättre.
Prevention är förstås att föredra. Redan i dag skulle blindhet kunna förhindras på ett stort antal barn om syrgastillförseln kontrollerades och populationsanpassade screening- och behandlingsprogram infördes där de saknas. Dessvärre är det brist på ögonläkare med kompetens att utföra ROP-undersökningar. En lovande lösning som redan används är telemedicin, där ögonbottenfotografier tagna med vidvinkelkamera skickas till särskilda »reading centres« där bedömning sker [35]. Att eftersträva lägre syremättnad före 34 veckor postmentruell ålder och högre därefter har rapporterats minska både incidens och svårighetsgrad av ROP [36].
Andra preventiva strategier syftar till att förbättra den postnatala energibalansen och därmed tillväxten. De mycket omogna barnen tolererar begränsade mängder av näring och har problem att tillgodogöra sig den, varför det inte räcker att öka mängden. Lipider överförs i ringa mängd intrauterint, men under tredje trimestern sker en selektiv placentär transport av långkedjiga omega-6- och omega-3-fettsyror, framför allt arakidonsyra (ARA) och dokosahexaensyra (DHA), vars koncentrationer sjunker snabbt efter prematur födelse [37]. Omega-3-fettsyran DHA inkorporeras i neuronal vävnad särskilt i retinas stavar under tredje trimestern och har avgörande betydelse för deras funktion och även för generell metabolism. Betydelsen av arakidonsyra under tredje trimestern är mindre känd. Tillförsel av långkedjiga fleromättade omega-3-fettsyror till möss minskade syrgasorsakad retinopati [38], och för närvarande pågår en klinisk prövning där arakidonsyra och dokosahexaensyra ges peroralt så snart barnet kan ta emot föda.
IGF-1 verkar kunna öka utnyttjandet av näring vid svält [39] och är essentiell för tillväxt av hjärnan och resten av kroppen under fosterstadiet [40]. En fas 2-multicenterstudie av effekten av tillförsel av IGF-1 och dess bindarprotein IGFBP-3 på ROP-utfall pågår. Påverkan på annan morbiditet och hjärntillväxt studeras också.
Kliniska studier undersöker även om betablockeraren propranolol och kolhydraten inositol kan minska uppkomsten av proliferativ ROP.
Konklusion
Prematuritetsretinopati är en sjukdom som framför allt ses hos mycket omogna barn med stora svårigheter att anpassa sig till ett extrauterint liv. Brist på energi, viktiga näringsämnen och tillväxtfaktorer samt för utvecklingsstadiet ofysiologisk och fluktuerande syrsättning bidrar, liksom infektion/inflammation. Tillgänglig behandling är destruktiv. Forskningen bör inriktas på åtgärder som främjar normal tillväxt och utveckling direkt efter födelsen.
Potentiella bindningar eller jävsförhållanden: Prevention av ROP genom tillförsel av IGF-1 täcks av ett patent som ägs av Premacure AB, Uppsala. Ann Hellström är medicinsk konsult för Shire Pharmaceuticals, som äger Premacure AB. Ann Hellström och Anna-Lena Hård äger aktier i Premalux AB, som har finansiella intressen i Premacure AB.
Läs även författarintervjun med Ann Hellström.