Sammanfattat
Under perioden 1990–2009 har patienter med kongenitalt diafragmabråck i Stockholm behandlats enligt strategin skonsam ventilation, preoperativ stabilisering och ECMO vid behov.
Sammanlagt har 184 patienter med svenskt personnummer och ytterligare 10 utländska patienter behandlats under perioden.
Både överlevnaden till utskrivning och långtidsöverlevnaden efter 1–20 år var utomordentligt höga i ett
internationellt perspektiv. Detta gällde såväl hela materialet som specifika riskgrupper.
Om resultaten på nationell basis ska förbättras rekommenderar vi centralisering av vården.
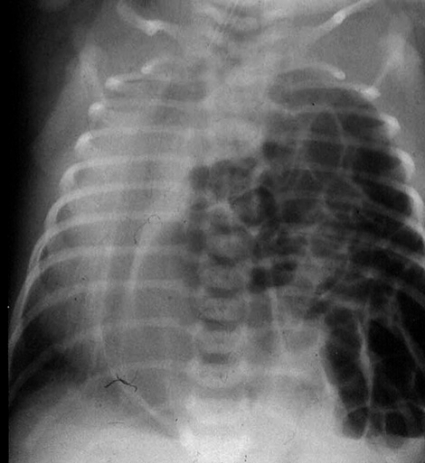
Kongenitalt diafragmabråck [1] drabbar 1 på 2 500–4 000 levande födda barn [2-4]. 90 procent av defekterna finns i den posterolaterala delen av diafragma, s k Bochdalek’s hernia, och i 80 procent av fallen på vänster sida (Figur 1). Av alla neonatala missbildningar är kongenitalt diafragmabråck en av dem som länge förknippats med låg överlevnad, och tillståndet är än i dag en av de största utmaningarna inom barnkirurgin, barnintensivvården och neonatologin [5]. Det beror till stor del på den lunghypoplasi och pulmonella hypertension som ses hos dessa patienter [6, 7].
Missbildningen är komplex och inkluderar såväl defekt i diafragma som lunghypoplasi, innefattande färre bronkiella förgreningar, färre alveoler, underutvecklad vaskularisering och hypertrofi av glatta muskelceller i arterioli. Vasospasm leder till pulmonell hypertension och höger–vänstershunt [8]. Effekten av detta är ytterligare försämring av syresättningen och ökad vasokonstriktion i lungkärlen, vilket leder till att patienterna kort efter födelsen ofta utvecklar akut respiratorisk svikt [9-11].
Orsaken till kongenitalt diafragmabråck är okänd. Det finns många teorier som försöker förklara etiopatogenesen [12-15]. Tidigare har man trott att det primära var defekten i diafragma som tillät tarm och övrigt bukinnehåll att herniera in i torax under fosterlivet och att trycket på lungorna sedan ledde till hypoplasin [16]. Men djurexperimentell forskning har indikerat att det finns en primär påverkan på lungutvecklingen redan innan hernieringen har skett [14, 17, 18].
Från kirurgisk till fysiologisk akutbehandling
Kongenitalt diafragmabråck beskrevs första gången på 1700-
talet i ett obduktionsmaterial [19]. Den första perioden, med enbart anatomisk beskrivning och klassificering, pågick till slutet av 1800-talet. Under den andra perioden, från slutet av 1800-talet till mitten av 1900-talet, kom de första försöken till kirurgisk åtgärd, som initialt misslyckades. Den första lyckade operationen skedde i början av 1900-talet. Överlevnaden under denna period var låg (under 25 procent). Under den tredje perioden, som pågick fram till 1980 [19-21], opererades patienterna omedelbart efter födelsen för att dekomprimera lungorna. Dessa ingrepp innebar emellertid en retning av lungor och kärl som gjorde syresättningen ännu svårare. Man hade samtidigt kunnat se att patienter som av olika orsaker opererats senare än vanligt hade bättre chans att överleva. Detta låg till grund för den fjärde perioden under 1980-talet, där man utarbetade nya strategier med utökad preoperativ stabilisering och senarelagd kirurgi.
Den femte och nuvarande perioden startade omkring 1990, då begreppen »gentle ventilation« och »permissive hypercapnia« infördes. Man fokuserade på att ventilera patienterna skonsamt för att undvika höga luftvägstryck. Viss hyperkapni accepterades, och vid behov stabiliserades patienterna preoperativt med ECMO (extrakorporeal membranoxygenering). Kvävemonoxid (NO) användes vid tecken till pulmonell hypertension. Behandlingssättet förändrades runt om i världen under 1990-talet i takt med tillgången till teknik och kompetens [1, 11, 22]. De nya behandlingsstrategierna hade varierande resultat men var oftast framgångsrika [22-28]. Tyvärr var långtidsresultaten fortfarande en besvikelse [24, 29, 30], vilket under det senaste decenniet ledde till utvecklingen av en ny terapeutisk period, med implementering av fosterkirurgi, som har testats i olika former och med varierande resultat [31, 32].
1990 infördes i Stockholm en ny behandlingsstrategi för patienter med kongenitalt diafragmabråck baserad på de nya principerna, som inbegrep atraumatisk ventilation och preoperativ stabilisering samt preoperativ ECMO vid behov. Resultaten var initialt lovande med en överlevnad till utskrivning kring 90 procent och har tidigare rapporterats [11].
Syftet med det aktuella arbetet var att utvärdera överlevnaden på både kort och lång sikt för 20-årskohorten 1990–2009.
Metod
Under den preoperativa stabiliseringen ventilerades patienterna med konventionell respirator, och man försökte undvika inspiratoriska tryck överstigande 25 cm H2O. Högre tryck användes korta perioder under förberedelserna för ECMO. Man eftersträvade ett pco2 <8 kPa och en preduktal saturation överstigande 85 procent. NO administrerades vid behov i doser om 10–80 ppm. Högfrekvensoscillerande ventilation (HFOV) användes i ett fåtal fall. Blodtrycket reglerades vid behov med transfusion av kolloider och inotropa läkemedel.
ECMO användes på konventionella indikationer [33, 34] om adekvata blodgaser inte kunde uppnås med ovan beskrivna strategi. I korthet innebar det att om man under 3–4 timmars tid inte lyckats få den preduktala saturationen att överstiga 85 procent eller hålla pco2 <8 kPa utan att öka ventilationstrycket kanylerades patienten för ECMO. Om patienten försämrades under denna period beslutades omgående om ECMO. Kontraindikationer för ECMO var allvarlig kromosomrubbning, födelsevikt <2,0 kg och bilateralt bråck i kombination med hjärtmissbildning. Något krav på en period av kortare intervall av acceptabel syresättning, s k honeymoon, förelåg inte.
Patienterna opererades för sitt diafragmabråck efter en stabiliseringsperiod på i allmänhet 24–96 timmar. Den kortare tiden tillämpades dels tidigt i perioden, dels när inga riskfaktorer förelåg. Längre tid än 96 timmar tillämpades för patienter med mycket instabil hemodynamik. Subkostal incision utfördes i samtliga fall. Defekten slöts primärt där detta var möjligt utan stramning och i övriga fall med hjälp av Gortex-lapp (Figur 2).
Enstaka patienter som ECMO-behandlades förbättrades relativt snabbt och kunde dekanyleras före operation, som i dessa fall gjorts minst fyra dygn efter dekanyleringen. De flesta ECMO-patienterna opererades dock under pågående ECMO-behandling och dekanylerades när lungfunktionen så tillät. Patienter som efter dekanylering fick försämrad lungfunktion och åter uppfyllde konventionella ECMO-kriterier rekanylerades för en andra ECMO-behandling.
Enstaka patienter blev inte handlagda i Stockholm initialt. De hämtades från andra centra i Norden av det mobila ECMOteamet [35]. De kanylerades för ECMO på det inremitterande sjukhuset och transporterades sedan till Stockholm. Behandlingen följde därefter klinikens gängse principer.
Kliniken har skapat ett kvalitetsregister (Access, Microsoft) för patienter med kongenitalt diafragmabråck som togs i bruk i januari 2008. Data avseende tidigare patienter har retrospektivt matats in i detta register. Uppgifter hämtades från sjukvårdsjournaler. I enstaka fall och framför allt avseende patienter som inte primärt handlagts på vår klinik saknas data.
Långtidsöverlevnad studerades under 2010 och minst ett år efter patientens födelse med uppgifter från folkbokföringen. Data anges som medelvärde ± standarddeviation. Students t-test och χ2-test har använts vid signifikansprövningar.
Material
Studien omfattar samtliga patienter som handlagts vid vår klinik (S:t Görans barnkliniker initialt och efter 1998 Astrid Lindgrens barnsjukhus) under 20-årsperioden 1990–2009. Totalt var det 194 patienter. Av dem saknade tio svenskt personnummer (två flyktingar och åtta utländska patienter) och ingår inte i långtidsuppföljningen. En patient med svenskt personnummer emigrerade utomlands vid 11 års ålder och har i redovisningen räknats som långtidsöverlevande.
Prenatal diagnos ställdes med ultraljud på 66 patienter under hela perioden, medan man i 112 fall inte kände till diagnosen vid partus (i sex fall kunde man inte avgöra om diagnosen var känd eller inte vid partus) (Tabell I). Under periodens andra hälft var 50 procent av fallen kända prenatalt.
Av de 184 patienterna behövde 120 intuberas inom sex timmar efter födelsen (Tabell II). Födelsevikt (3,3 ± 0,70 kg) och gestationsålder (38 ± 2,4 veckor) för dessa var desamma som i hela materialet på 184 patienter (3,3 ± 0,66 kg respektive 38 ± 2,4 veckor). Majoriteten av patienterna var pojkar (118 pojkar, 66 flickor), och fördelningen mellan könen var densamma som i riskgruppen som intuberades inom sex timmar. 141 av patienterna hade vänstersidigt bråck, 22 högersidigt och en bilateralt bråck.
I riskgruppen som intuberades inom sex timmar behövde 57 patienter en lapp för att täcka defekten vid operationen, medan 51 patienter kunde opereras med primärsutur. I hela materialet var förhållandet det omvända, och 93 av de 184 patienterna opererades med primärsutur, medan endast 65 krävde lapp. Sex patienter opererades aldrig, och för 20 saknas uppgift avseende lapp.
I riskgruppen behandlades 47 av 120 (39 procent) med ECMO. Tolv av de 47 behandlades ytterligare en gång i ECMO. I hela materialet (184 patienter) behandlades 54 (29 procent) i ECMO, varav 13 två gånger (Tabell II).
Resultat
Av samtliga 194 patienter behandlade under 20-årsperioden överlevde 164 (85 procent) till utskrivning från vårt sjukhus. Tio patienter saknade svenskt personnummer, och framställningen fokuserar därför på de resterande 184 som vi kunnat följa upp. Av dessa skrevs 156 (85 procent) ut levande från vår klinik. Under slutet av år 2010 levde 146 av patienterna. Således förelåg en sen dödlighet på 5 procent (Tabell III).
120 patienter behövde intuberas inom sex timmar. Av dessa levde 99 (83 procent) till utskrivning och 92 (77 procent) vid uppföljningen 1–20 år efter partus. Samtliga patienter som intuberades senare än vid sex timmars ålder överlevde. Av 65 patienter som behövde lapp i diafragmadefekten levde 50 (77 procent) till utskrivning och 45 (69 procent) vid uppföljningen. Två av de 93 patienterna som opererades med primärsutur avled före utskrivning från sjukhuset. 37 (69 procent) av de 54 som behövde behandlas med ECMO levde vid utskrivningen, och 30 (56 procent) var långtidsöverlevande. Av de 13 patienterna som behövde behandlas i ECMO en andra gång levde åtta (62 procent) till utskrivning och sju (54 procent) vid långtidsuppföljningen.
Födelsevikten var signifikant lägre hos dem som avled under sjukhusvistelsen (3,0 ± 0,89 kg) än hos dem som skrevs ut levande (3,4 ± 0,62 kg) (P < 0,05). De som krävde lapp vid operationen hade signifikant lägre överlevnad än de hos vilka man kunde primärsuturera defekten (P < 0,0001). Patienter som behövde intuberas inom sex timmar efter födelsen hade likaledes signifikant lägre överlevnad än övriga (P < 0,01).
Diskussion
Congenital Diaphragmatic Hernia Study Group (CDHSG) är en sammanslutning av ca 50 centra som behandlar kongenitalt diafragmabråck hos nyfödda. De flesta centra är nordamerikanska, men det finns även ett flertal europeiska och asiatiska. Bland annat rapporterar deltagande centra avidentifierade behandlingsresultat till en gemensam databas. Varje centrum får tillgång till gruppens gemensamma resultat. CDHSG bildades 1995 [36], och Stockholm har rapporterat sedan 1998. År 2010 fanns data från 5 577 patienter som diagnostiserades prenatalt eller som fått symtom under första levnadsdygnet.
Den totala överlevnaden i CDHSG:s databas fram till utskrivning från sjukhuset var 69 procent – att jämföra med överlevnaden i Stockholmsmaterialet på 85 procent. Det är dock svårt att jämföra överlevnad mellan olika material eftersom missbildningens allvarlighet kan variera. Ju tidigare symtomen uppstår, desto allvarligare är lunghypoplasin, varför patienter som behöver intuberas inom sex timmar räknas som en riskgrupp. I det befintliga materialet var överlevnaden till utskrivning i denna riskgrupp 83 procent (99/120) och långtidsöverlevnaden 77 procent (92/120). Även i ett skandinaviskt perspektiv ligger överlevnaden högt.
Skari och medarbetare [37] har sammanställt data om patienter från 12 av 13 skandinaviska centra (vår klinik var en av de 12) under fyraårsperioden 1995–1998. Av 195 barn (varav 27 med symtomdebut efter 24 timmar) överlevde 70 procent till utskrivning. Sett över hela 20-årsperioden har överlevnaden i vårt material inte förändrats nämnvärt. I början av perioden var den marginellt högre, vilket rapporterats tidigare [14]. Däremot är den väsentligt högre än under föregående 20-årsperiod vid vår klinik, då endast 60 procent överlevde trots att andelen riskgruppspatienter var väsentligt lägre i det materialet [38].Överlevnad, defektstorlek och ECMO
Överlevnaden vid kongenitalt diafragmabråck korrelerar starkt med defektens storlek [39, 40]. Mortaliteten hos patienter som behöver lapp vid operationen är därför högre än hos dem som kan opereras med primärsutur. Många kliniker avstår till och med från att behandla patienter som bedöms ha en mycket dålig prognos baserad på bl a blodgaser de närmaste timmarna efter partus under maximal respiratorbehandling. Kliniker som avstår från att operera patienter med mycket dålig prognos får då lägre operationsmortalitet. Vid jämförelser kan det därför vara lämpligt att se på dels resultaten för dem som opererats med primärsutur, dels det sammanlagda resultatet för patienter som antingen opererats med lapp eller där man avstått från operation på grund av dålig prognos. Tabell II och III visar att 50 av våra 65 patienter som opererats med lapp överlevde. I sex fall avstod vi från operation, varför överlevnaden i den senare gruppen var 50/71, dvs 70 procent, vilket är signifikant högre (P < 0,001) än motsvarande överlevnad i CDHSG-materialet, där den är 49 procent. Överlevnaden bland våra patienter som opererats med primärsutur var 98 procent (93/95), dvs ungefär densamma som i CDHSG-materialet (95 procent).
ECMO användes på 29 procent av patienterna i hela materialet och på 39 procent av dem som behövde intuberas inom sex timmar. Frekvensen av ECMO-behandlingar var ungefär densamma som vid många utländska centra [41, 42]. Extracorporeal Life Support Organization (ELSO)
Fördelen med prenatal diagnos
En tredjedel av patienterna i det aktuella materialet hade prenatal diagnos. Under periodens senare hälft var hälften kända prenatalt. Prenatal diagnos ger möjlighet till avbrytande av graviditeten (om diagnosen ställts tidigt), till prenatal behandling och till planering av förlossningen. Utförlig information till föräldrarna av experter är naturligtvis av utomordentligt stor betydelse. Det finns ett flertal prognostiska faktorer som kan studeras prenatalt. Bland annat kan man med ultraljud jämföra den kontralaterala lungans storlek med huvudets storlek och beräkna en kvot (lung-to-head ratio) [49]. Lungornas storlek kan även uppskattas med MR-undersökning av fostret [50, 51]. God korrelation med överlevnad har publicerats, men resultaten har varit svåra att reproducera på andra centra. Vid vänstersidiga bråck är förekomst av vänster leverlob i torax en riskfaktor, som däremot är lättare att jämföra mellan centra. I en metaanalys studerades 710 foster med kongenitalt diafragmabråck. Om levern identifierades i torax var överlevnaden 45,4 procent, signifikant lägre än om levern helt låg i buken (73,9 procent) [52]. Vid mycket dålig prognos kan intrauterin behandling av fostret bli aktuellt.
Intrauterin behandling rekommenderas inte
Öppen kirurgisk rekonstruktion av diafragmabråcket har i djurförsök varit lovande men visat sig inte vara genomförbar på människa eftersom navelvenen obstrueras vid bråckrepositionen [53]. Däremot kan fostrets trakea stängas under slutet av graviditeten, vilket kraftigt stimulerar lungtillväxten. Trakeal obstruktion förutsätter dock att denna tas bort senare under graviditeten eller att fostret föds med s k EXIT-procedur (ex utero intrapartrum treatment), där luftvägen säkras under pågående placentacirkulation vid kejsarsnitt. Initialt var resultaten lovande, men en randomiserad studie kunde inte påvisa någon minskning i mortalitet jämfört med kontroller behandlade på konventionellt postnatalt sätt [54].
Deprest et al har därefter utvecklat en helt perkutan endoskopisk metod där trakea obstrueras med en ballong, vilken senare under graviditeten kan punkteras perkutant så att obstruktionen avlägsnas. Jämfört med historiska kontroller har minskad mortalitet påvisats [32]. För närvarande pågår en randomiserad studie med denna metod, men några resultat har inte publicerats. I avsaknad av evidens har författarna hittills inte rekommenderat intrauterin behandling till några föräldrar.
Centeralisering av vården
Vid prenatal diagnos bör förlossningen planeras. Det torde inte råda något tvivel om att den blivande mamman ska förlösas vid ett centrum med tillgång till neonatal intensivvård och barnkirurgisk expertis. Centra med fler fall har i en kanadensisk studie visat signifikant högre överlevnad än centra med färre fall [55], vilket även indikerats i en skandinavisk studie [56]. Enligt The CDH EURO Consortium Consensus bör ECMO finnas i den terapeutiska arsenalen [1]. Om överlevnaden på nationell nivå i Sverige ska förbättras bör således vården av prenatalt kända fall centraliseras till ett eller möjligen två centra. Patienter som diagnostiseras postnatalt bör, liksom tidigare, snarast remitteras till centra med neonatal intensivvård och barnkirurgi. Geografiska hänsyn kan då behöva tas även om patienten i idealfallet bör remitteras direkt till ett centrum med tillgång till ECMO. Om patienten är i för dåligt skick för konventionell transport kan transport med mobilt ECMO-team bli aktuell [35].
Konklusion
Sammanfattningsvis kan konstateras att patientkohorten med kongenitalt diafragmabråck som behandlats vid Astrid Lindgrens barnsjukhus (och tidigare S:t Görans sjukhus) 1990–2009 enligt riktlinjer som rekommenderas internationellt uppvisar en utomordentligt hög överlevnad på såväl kort som lång sikt i ett globalt perspektiv. Ska överlevnaden på nationell bas i Sverige förbättras bör vården centraliseras.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.