Kronisk hjärtsvikt beskrivs ofta som en diagnos med högre mortalitet än flertalet tumörsjukdomar. Mycket kan dock i dag göras för att förbättra överlevnad och livskvalitet och minska behovet av sjukhusvård för många hjärtsviktspatienter. Liksom för många tumörsjukdomar har överlevnaden vid hjärtsvikt förbättrats under de senaste decennierna [1-4] parallellt med utveckling av effektiva behandlingsmetoder för hjärtsvikt med systolisk vänsterkammardysfunktion [5-24]. Däremot har inga behandlingar visat övertygande effekt på överlevnad vid hjärtsvikt med bevarad ejektionsfraktion (HFPEF [heart failure with preserved ejection fraction]) eller högerkammardysfunktion [24].
Registerstudier visar att många hjärtsviktspatienter inte får optimal behandling [25]. Även om en betydande andel av dessa patienter (särskilt de äldre) kan ha kontraindikationer, bör en risk–nyttabedömning göras i varje enskilt fall.
Denna ABC-artikel syftar till att ge en uppdaterad bild av moderna behandlingsprinciper för hjärtsvikt.
Behandlingsprinciper
Vid hjärtsvikt med systolisk vänsterkammardysfunktion [26] syftar behandlingen till att motverka hjärtsviktens progress genom att bryta negativ neurohormonell aktivering (ACE-hämmare, ARB [angiotensinreceptorantagonister], betablockerare, aldosteronantagonister), förebygga sekundär arytmi (betablockerare), avvärja allvarliga konsekvenser av arytmi (ICD [implanterbar defibrillator]), synkronisera kammarkontraktioner (CRT [cardiac resynchronization therapy]) och att förebygga tromboembolism vid samtidigt förmaksflimmer (warfarin).
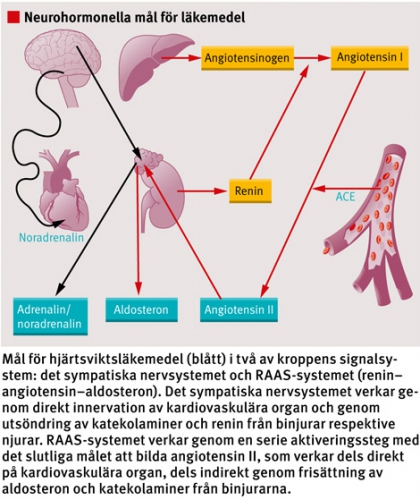
Vid hjärtsvikt aktiveras ett flertal neurohormonella system, av vilka renin–angiotensin–aldosteronsystemet (RAAS) och det sympatiska nervsystemet har klinisk betydelse, eftersom antagonister har visat minskad mortalitet i kliniska studier. Dessa system interagerar och förstärker effekten av varandra.
Behandlingen vid alla former av kronisk hjärtsvikt syftar i övrigt till att behandla underliggande etiologi (hypertoni, alkoholmissbruk, kranskärlssjukdom och ibland klaffsjukdom) och lindra symtom (med diuretika, digoxin och nitrater). Flera medicinska behandlingsalternativ finns. Som sista utpost vid hjärtsvikt tillkommer hjärttransplantation för därtill lämpade patienter. Mekaniskt pumpstöd vid hjärtsvikt (främst LVAD [left ventricular assist device]) används i dag i Sverige i stort sett uteslutande i väntan på hjärttransplantation men har även börjat erbjudas selekterade patientgrupper med kontraindikationer för hjärttransplantation.
Flertalet patienter handläggs och kontrolleras i primärvården, ibland efter initial kontakt med specialistklinik. Patienter som sjukhusvårdats för hjärtsvikt remitteras vid många sjukhus till särskild sjuksköterskeledd hjärtsviktsmottagning för strukturerad information, råd om egenvård, coachning och upptitrering av sviktmedicinering, vilket har visats minska behovet av sjukhusvård [27].
Patientrådgivning är av stor betydelse för att öka livskvalitet och minska behovet av sjukhusvård vid hjärtsvikt. Patienten bör också undervisas om värdet av fysisk träning för att öka livskvalitet och minska behov av sjukhusvård [28]. Behovet av kliniska kontroller är individuellt och varierar från täta kontroller vid svår hjärtsvikt med komplicerad behandling till årliga kontroller vid välbehandlad, lindrig hjärtsvikt.
Plötslig försämring är den vanligaste anledningen till sjukhusvård vid kronisk hjärtsvikt. Hjärtsviktspatienter har ofta små marginaler, och försämring kan orsakas av ett flertal faktorer, t ex överdrivet vätskeintag, intorkning/överbehandling med diuretika, infektion, arytmi (såväl ventrikulär som supraventrikulär; ett förmaksflimmer kan orsaka påtaglig försämring), stort alkoholintag, sviktande behandlingsföljsamhet, akut koronart syndrom, hypertensiv kris, anemi eller akut mitralisinsufficiens på grund av kordaruptur. Plötslig försämring handläggs (som all akut hjärtsvikt) utifrån om den kliniska bilden domineras av lungödem, chock eller högerkammarsvikt och med behandling riktad mot utlösande faktorer (antibiotika, elkonvertering, revaskularisering osv).
systolisk vänsterkammardysfunktion
När diagnosen hjärtsvikt med systolisk vänsterkammardysfunktion ställts klassificeras patientens funktionsgrad enligt New York Heart Associations (NYHA) system [29], vilket sedan vägleder behandlingen. Vid klassificering ska hänsyn tas till samtidiga sjukdomstillstånd som bidrar till sviktsymtom.
ACE-hämmare
Vid minskad njurgenomblödning frisätts renin, som metaboliserar angiotensinogen till angiotensin I. Angiotensin I metaboliseras vidare till angiotensin II av angiotensinkonvertas (ACE) i kärlväggen. Angiotensin II binder till angiotensinreceptorer, vilket resulterar i vasokonstriktion och salt- och vätskeretention samt frisättning av aldosteron och katekolaminer från binjuren.
Behandling med hämmare av ACE resulterar i minskad bildning av angiotensin II och är indicerad hos samtliga patienter med systolisk vänsterkammardysfunktion (LVEF ≤40 procent). Behandlingen har visats förbättra kammarfunktionen, förlänga överlevnaden, minska behovet av sjukhusvård och förbättra livskvaliteten [5-7]. Kontraindikationer utgörs av bilateral njurartärstenos, hyperkalemi, uttalad kreatininstegring utan behandling (>220 µmol/l), hemodynamiskt signifikant aortastenos och idiopatiskt/ärftligt angioödem.
Den vanligaste biverkningen av behandlingen är hosta, varvid byte till ARB rekommenderas. En viss kreatininstegring ses ofta efter behandlingsinitiering och accepteras så länge den understiger 30–50 procent av ursprungsvärdet och ett absolut värde <265 µmol/l. Om något av dessa värden uppmäts, bör dosen halveras och kreatinin monitoreras tätt. Detta är dock endast en tumregel – hänsyn måste tas till den enskilde patienten. Exempelvis torde en kreatininstegring från 120 till 170 µmol/l hos en äldre patient med liten muskelmassa innebära en kraftig försämring av njurfunktionen, och dosen bör justeras tidigt i behandlingsförloppet. Vid stigande kreatinin till >310 µmol/l bör behandingen avbrytas. Andra orsaker till försämrad njurfunktion bör i detta sammanhang eftersökas, inklusive överdrivet diuretikabruk eller samtidigt NSAID-bruk (t ex vid smärtlindring vid hjärtsvikt).
Viss kaliumstegring kan ses vid behandlingsinitiering; nivåer upp till 5,5 mmol/l accepteras, men vid högre värden ska dosen halveras, och vid värden >6,0 mmol/l ska läkemedlet sättas ut omgående. Andra orsaker till hyperkalemi ska uteslutas.
Symtomgivande ortostatisk hypotoni är en vanlig biverkning, och patientinformation är viktig för att förebygga allvarliga konsekvenser (cerebral hypoxi med fallskador). Vid kvarstående symtomatisk hypotoni bör i första hand andra läkemedel som påverkar blodtrycket än ACE-hämmare, betablockerare och aldosteronantagonister reduceras (lämpligen diuretika). Om denna åtgärd inte har effekt, får dossänkning och eventuell seponering av ACE-hämmare, betablockerare eller aldosteronantagonist tillgripas. Hänsyn bör här tas till biverkningsprofilen; om bilden domineras av ACE-hämmarbiverkningar som kreatininstegring, kan ACE-hämmarbehandlingen minskas. Vid angioödem sätts preparatet ut omgående.
Betablockerare
Det sympatiska nervsystemets mediatorer, katekolaminerna, insöndras från binjuren men också från nervceller när tryckreceptorer i centrala artärer aktiveras av sjunkande tryck. Vid långvarig aktivering orsakar de, genom bindning till betareceptorer, minskad inotropi, ökad arytmibenägenhet, minskad njurgenomblödning och ökad reninfrisättning. Behandling med någon av betareceptorblockerarna metoprololsuccinat i slow release-beredning, bisoprolol eller karvedilol är indicerad hos samtliga patienter med hjärtsvikt och systolisk vänsterkammardysfunktion (LVEF ≤40 procent). Behandling med dessa preparat har visats förbättra kammarfunktionen, förlänga överlevnaden, minska behovet av sjukhusvård och förbättra livskvaliteten [8-12]. Andra preparat i betablockerargruppen har inte visat effekt vid hjärtsvikt.
Kontraindikationer är bradykardi (<50 slag per minut), AV-block grad II–III, dekompenserad hjärtsvikt och svår perifer kärlsjukdom med hotande gangrän. Astmaanamnes bör föranleda försiktighet, men vid KOL (kroniskt obstruktiv lungsjukdom) tolereras betablockad oftast väl.
Vid kvarstående symtomgivande hypotoni gäller resonemang som för ACE-hämmare ovan: när biverkningsprofilen utöver hypotoni domineras av betablockerarbiverkningar som kalla fingrar, mardrömmar etc kan i första hand betablockaden minskas. Generellt känner patienter ofta en tidig positiv effekt av ACE-hämmare till skillnad från av betablockad, som upplevs neutralt eller rentav negativt under de första månaderna.
Pulssänkning med ivabradin, som specifikt hämmar sinusknutan, har visats minska hjärtsviktsrelaterad sjukhusvård och död hos hjärtsviktspatienter med vilopuls >70 och sinusrytm [30, 31] som tillägg till standardbehandling. Preparatet bör dock förskrivas endast av hjärtsviktsspecialist.
Aldosteronantagonister
Aldosteron bidrar till salt- och vätskeretention och stimulerar till fibrosbildning och remodellering av myokardiet. Hos patienter med LVEF ≤35 procent och symtom (NYHA-klass II–IV) trots optimal dosering av ACE-hämmare/ARB och betablockerare bör tillägg av en aldosteronreceptorantagonist (spironolakton eller eplerenon) övervägas. Behandling med dessa preparat har visats förlänga överlevnaden och minska behovet av sjukhusvård [13-15]. Spironolakton är till skillnad från eplerenon studerat endast vid NYHA-klass III–IV.
Någon direkt jämförelse mellan preparaten är inte gjord. Prisskillnaden är stor, varför spironolakton oftast används som förstahandspreparat. Det finns dock skäl att varna för de könshormonella bieffekterna (bröstömhet, gynekomasti), som inte alltid spontanrapporteras men som inte desto mindre kan försämra livskvaliteten avsevärt. I dessa fall rekommenderas byte till eplerenon.
Kontraindikationer är hyperkalemi (kalium >5 mmol/l vid behandlingsstart) och uttalat högt kreatininvärde (>220 µmol/l). En viss kreatininstegring ses ofta efter behandlingsinitiering. Större kreatininstegring bör föranleda dosreduktion och tät monitorering eller seponering. Liksom för ACE-hämmare bör hänsyn tas till den enskilde patienten (ålder, samsjuklighet, muskelmassa etc) och till andra orsaker till försämrad njurfunktion, t ex överdrivet diuretikabruk eller samtidigt NSAID-bruk. Viss kaliumstegring kan också ses vid behandlingsinitiering; nivåer upp till 5,5 mmol/l accepteras, men vid högre värden ska dosen halveras, och vid >6,0 mmol/l ska läkemedlet sättas ut omgående. Andra orsaker till hyperkalemi ska uteslutas.
Vikten av elektrolytkontroll exemplifieras av en observationell studie, som visade markant ökad förekomst av hyperkalemi och hyperkalemiassocierad död efter introduktionen av spironolakton år 1994, huvudsakligen på grund av inadekvat elektrolytkontroll [32].
Angiotensinreceptorantagonister (ARB)
Antagonister av angiotensinreceptorn (ARB) minskar effekten av angiotensin II och kan användas som alternativ till ACE-hämmare vid intolerans mot det senare, på samma indikation. Liksom ACE-hämmare förbättrar dessa preparat kammarfunktionen, förlänger överlevnaden, minskar behovet av sjukhusvård och förbättrar livskvaliteten [16-18]. Kontraindikationerna är desamma som för ACE-hämmare men inkluderar inte angioödem; dock finns enstaka fall av angioödem beskrivna även för ARB. Biverkningarna liknar också dem för ACE-hämmare, men hosta förekommer sällan.
Behandlingskombinationer
Patienter med LVEF ≤40 procent och symtom bör enligt ovan behandlas med både ACE-hämmare (eller ARB vid intolerans mot ACE-hämmare) och betablockad. Dubbel RAAS-antagonism i kombination med betablockad är förbehållet patienter i NYHA-klass II–IV och bör handläggas med regelbundna kontroller hos hjärtsviktssjuksköterska under upptitrering av läkemedel. Evidensbaserade läkemedelskombinationer för dubbel RAAS-antagonism utgörs av antingen ACE-hämmare och aldosteronantagonist [13-15] eller ACE-hämmare och ARB (där kandesartan har bäst dokumentation) [19].
Vilken av dessa två kombinationer som bör väljas i första hand är ännu inte studerat, men av kostnadsskäl väljs oftast den förstnämnda kombinationen. Patientens biverkningsprofil och terapisvar kan dock föranleda byte av kombinationsbehandling. Tredubbel RAAS-antagonism (ACE-hämmare och ARB och aldosteronantagonist) i kombination med betablockad har studerats endast i begränsad omfattning i subgruppsanalyser. Även om dessa analyser antytt en möjlig behandlingsvinst, rekommenderas denna behandling för närvarande inte av den europeiska kardiologföreningen (ESC [European Society of Cardiology]).
Vanligen initieras först diuretika för symtomlindring i kombination med ACE-hämmare. Betablockad initieras först när ACE-hämmare titrerats till halv eller full dos, men ordningen kan möjligen också vara den omvända [33] beroende på individuella faktorer hos patienten, t ex etiologi, förekomst av arytmi och annan samsjuklighet. Såväl ACE-hämmare och ARB som betablockerare påbörjas i låg dos och upptitreras gradvis. Kombinationspreparat med ACE-hämmare/ARB och diuretika (som används vid hypertoni) bör undvikas vid hjärtsviktsbehandling för att möjliggöra individualiserad preparatdosering.
Symtomlindrande behandling
Läkemedel som kan ha god symtomlindrande effekt och minska behovet av sjukhusvård är diuretika, digitalis och nitrater. Lägsta effektiva dos ska eftersträvas, eftersom högre doser leder till biverkningar som kan försvåra behandling med preparat med prognostisk effekt, som ACE-hämmare och betablockerare.
Diuretika (andra än aldosteronantagonister, som diskuterats ovan) har god och snabb effekt på hjärtsviktssymtom som beror på vätskeretention, till skillnad från neurohormonell blockad där effekten tar längre tid. Det finns inga entydiga data för effekt på mortalitet, men långsiktiga studier saknas. Ofta föredras loopdiuretika vid hjärtsvikt, men vid behandlingsresistenta ödem kan tillägg av ett tiaziddiuretikum eller liknande prövas. Detta medför dock hög risk för elektrolytrubbning och metabol störning; insättning och uppföljning ska därför ske under noggrann kontroll [34]. Vid behov av diuretika men tendens till hypokalemi kan spironolakton läggas till som kaliumsparande diuretikum.
Digitalis har i en stor randomiserad studie befunnits minska behovet av sjukhusvård men utan effekt på överlevnaden hos patienter med sinusrytm [35]. Digitalis rekommenderas i dag för frekvensreglering till patienter med hjärtsvikt med systolisk vänsterkammardyfunktion (LVEF ≤40 procent) och förmaksflimmer, där behandling med enbart betablockerare inte ger adekvat frekvensreglering [36].
Digitalis kan även övervägas till patienter med symtomgivande hjärtsvikt trots optimal dosering av ACE-hämmare/ARB, betablockerare och aldosteronantagonist [24]. Kontraindikationer är AV-block grad II och III och preexcitation. Särskild försiktighet bör iakttas vid samtidig elektrolytrubbning (då risken för arytmi ökar kraftigt) och vid nedsatt njurfunktion (då risken för digoxinackumulation med påföljande intoxikation ökar).
Kirurgisk behandling
Värdet av revaskularisering är studerat endast i begränsad omfattning hos patienter med hjärtsvikt. I den enda moderna randomiserade studien (STITCH) utvärderades nyligen värdet av revaskularisering jämfört med enbart medicinsk behandling hos hjärtsviktspatienter med ischemisk hjärtsjukdom [39, 40]. Studien visade inte någon statistiskt säkerställd effekt på total överlevnad, men förbättrad överlevnad från kardiovaskulär död och minskat behov av sjukhusvård. Enligt de senaste riktlinjerna från europeiska kardiologföreningen ska revaskularisering därför övervägas hos hjärtsviktspatienter med utbredd kranskärlssjukdom [24].
Vid hjärtsvikt orsakad av klaffsjukdom, särskilt aortastenos, kan kirurgisk [41] eller kateterburen [42, 43] behandling i utvalda fall ha god effekt. Vid hypertrof kardiomyopati med obstruktion av aortautflödet kan kirurgisk myektomi eller kateterburen alkoholinfusion ha god effekt [44, 45].
Överlevnaden efter hjärttransplantation är i dag god; 10-årsöverlevnaden är >60 procent [46, 47]. Med anledning av organbristen kan hjärttransplantation bli aktuell endast för en selekterad grupp patienter med uttalad hjärtsvikt och begränsad samsjuklighet, endast ca 45–55 transplantationer utförs per år i Sverige. I avvaktan på transplantation kan dessa patienter behandlas med mekaniskt pumpstöd. Behandling med permanent mekaniskt pumpstöd [48] har i Sverige utförts i begränsad omfattning men kan, liksom behandling med totalt konstgjort hjärta, bli möjligt för större patientgrupper i framtiden.
HFPEF eller isolerad högerkammardysfunktion
Inga randomiserade, kontrollerade studier har övertygande visat effekt på överlevnad vid hjärtsvikt med bevarad ejektionsfraktion (HFPEF) eller isolerad högerkammardysfunktion, annat än vid behandling av pulmonell arteriell hypertension (PAH). Europeiska kardiologföreningen rekommenderar vid dessa tillstånd försiktigt bruk av diuretika för symtomlindring. Det är dock viktigt att inte driva ut stora mängder vätska för snabbt, vilket kan medföra stor sänkning av minutvolym, svår hypotoni och njurpåverkan. Associerad samsjuklighet vid diastolisk dysfunktion (t ex hypertoni, förmaksflimmer, diabetes och ischemi) ska behandlas.
Vid pulmonell arteriell hypertension kan pulmonell resistens sänkas och symtom lindras med särskilda antihypertensiva preparat: endotelinantagonister, fosfodiesterashämmare och prostacyklinanaloger [49]. För PAH-patienter är centraliserad utredning och behandling viktig, eftersom läkemedlen är associerade med risker, kräver noggrann uppföljning med hjärtkateterisering och är kostsamma [50].
Palliativ behandling
För patienter med svår hjärtsvikt som inte förbättras med kausal behandling, neurohormonell antagonism och CRT och som inte är aktuella för hjärttransplantation eller mekaniskt pumpstöd återstår palliativ behandling, som syftar till symtomlindring och förbättrad livskvalitet. Vid behandlingsrefraktära ödem kan då utökade, noggrannt monitorerade diuretikaregimer prövas, t ex kontinuerlig furosemidinfusion (10–40 mg/h). Tillägg av tiazid- eller tiazidliknande diuretikum kan också övervägas (exempelvis metolazon 0,5–1 tablett à 5 mg 2 gånger/vecka) [34].
Diuretikabehandling kan medföra alkalos, med försämrad diuretikaeffekt som följd. Vid ödem med förhöjt basöverskott kan därför tillägg av kolsyraanhydrashämmaren acetazolamid (förslagsvis 250 mg × 2) vara av värde, men risken för acidos och hypokalemi bör beaktas [51]. Vid behov av diuretika men tendens till hypokalemi kan spironolakton läggas till som kaliumsparande diuretikum.
Vid fortsatt terapirefraktära underbensödem kan pumpstövelbehandling prövas. Som sista utväg kan ultrafiltration övervägas i selekterade fall [52].
Vid återkommande försämringsepisoder relaterade till låg minutvolym kan, utöver digitalis, även intermittent infusion av andra inotropa läkemedel vara ett alternativ, exempelvis levosimendan (0,05–0,2 µg/kg/min). Bruk av inotropa preparat bör dock noga övervägas, eftersom flertalet preparat ökar myokardiets energibehov (ökar arytmirisken) och har visat antydan till ökad mortalitet i vissa studier [53]. Vid hjärtsvikt med kronisk hypoxi kan syrgasbehandling i hemmet vara av värde. Vid vård i livets slutskede kan även sederande medel användas för att dämpa negativa vegetativa symtom.
Vid palliativ behandling av hjärtsvikt uppstår etiska dilemman avseende beslut om att inte utföra hjärt–lungräddning och om deaktivering av ICD. Dessa beslut bör i största möjliga mån ske i samråd med patient och anhöriga [54].
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.