Perimyokardit beskriver samtidig perikardit (hjärtsäcksinflammation) och myokardit (hjärtmuskelinflammation). Mer specifikt syftar perimyokardit på myokardit med inslag av perikardit, medan myoperikardit syftar på perikardit med inslag av myokardit. Sjukdomarna kan vara okomplicerade, självläkande och ofta asymtomatiska. Ibland krävs dock avancerat omhändertagande och intensivvård. Perikardit recidiverar ofta och kan i svåra fall kräva operation där hjärtsäcken avlägsnas. Myokardit kan leda till hjärtsvikt eller i sällsynta fall till plötslig hjärtdöd.
Epidemiologi och etiologi
Prevalens och incidens av både perikardit och myokardit är svåra att uppskatta. Myokardit anses utgöra orsaken till uppemot 4 procent av hjärtsvikt hos yngre och ca 0,5–1 procent av hjärtsvikt hos äldre [1]. Perikardit och myokardit kan utlösas av virus, bakterier, svamp eller parasiter. I västvärlden är virus den dominerande orsaken. Vid perikardit är ca 80 procent av fallen virusorsakade eller idiopatiska. Det finns ett överlapp mellan agens som orsakar perikardit respektive myokardit, t ex coxsackievirus, parvovirus B19 och humant herpesvirus 6.
Utöver virus utgörs de vanligaste specifika etiologierna till perikardit av neoplasi, autoimmunitet och tuberkulos; övriga bakteriella infektioner utgör mindre än 1 procent. Exempel på bakterier som kan orsaka både perikardit och myokardit är mykoplasma, pneumokocker och Borrelia burgdorferi; Borrelia orsakar ofta atrioventrikulärt block. I tuberkulosendemiska områden är tuberkulos den dominerande orsaken till perikardit, framför allt hos hivsmittade, där tuberkulos är förklaringen till betydande perikardutgjutning i mer än 90 procent av fallen [2]. Den globalt vanligaste orsaken till myokardit är Chagas sjukdom, orsakad av parasiten Trypanosoma cruzi [3].
Immunmedierade orsaker förekommer vid både perikardit och myokardit, och det finns en koppling till primärt autoimmuna och systemiska sjukdomar såsom systemisk lupus erythematosus (SLE), sarkoidos, vaskulit och reumatoid artrit. Andra typer av cellskador, joniserande strålning, elektrisk chock, trauma, uremi och toxiner kan också orsaka perimyokardit. Genomgången infektion eller annan orsak till myocytskada kan orsaka försämring eller återfall genom att exponera antigener för immunförsvaret och därmed orsaka en sekundär autoimmun reaktion [3].
Dresslers syndrom (postkardiotomisyndrom eller postinfarktsyndrom) är en typ av perimyokardit till följd av cellnekros vid hjärtinfarkt. Postkardiotomisyndrom kan uppstå efter öppen hjärtkirurgi. Postinfarktsyndrom ses alltmer sällan, eftersom behandlingen (inklusive tidig kranskärlsintervention) förbättrats.
Symtom och initial utredning
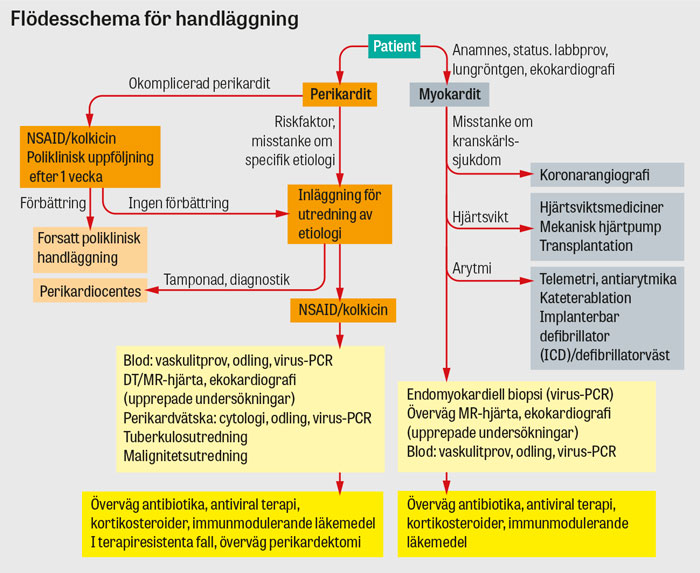
Många patienter med perikardit/myokardit söker aldrig vård, eftersom symtomen kan vara lindriga. I anamnesen framkommer ofta en virusinfektion veckorna före insjuknandet. I utredningen ingår C-reaktivt protein (CRP), troponin och ekokardiografi. Förhöjda troponinvärden innebär myocytskada och därmed åtminstone myoperikardit; vid samtidigt sänkt vänstersidig ventrikulär ejektionsfraktion bör snarast perimyokardit misstänkas.
Perikardit
Karakteristiskt vid perikardit är skarp och pleuritliknande bröstsmärta, som kan variera med andningscykeln och lindras i uppesittande och framåtlutat kroppsläge. Ibland är den dock svår att skilja från ischemiskt orsakad smärta. Perikardiella gnidningsljud kan uppkomma då inflammerat visceralt och parietalt perikardium gnids mot varandra; detta upphör redan vid mindre mängd perikardvätska. Gnidningsljud auskulteras med fördel med stetoskopets membran direkt till vänster om sternum.
På 12-avlednings-EKG ses typiskt generella ST-höjningar och sänkt PQ-sträcka. ST-höjningarna är konkava till skillnad från dem som ses vid ST-höjningsinfarkt, och det saknas reciproka sänkningar.
Det är också värdefullt att ta prov för analys av NT-proBNP (N-terminalen av förstadiet till natriuretisk peptid av B-typ [BNP]) för att värdera förekomst av hjärtsvikt. Den europeiska kardiologföreningen (ESC; European Society of Cardiology) rekommenderar att patienter med misstänkt perikardit genomgår transtorakal ekokardiografi och lungröntgen [2]. Det krävs ofta mer än 300 ml perikardvätska för att den ska kunna ses med lungröntgen.
Myokardit
Symtom vid myokardit utgörs ofta av bröstsmärta, andfåddhet, hjärtklappning och infektionssymtom. Svimning kan ske till följd av långsam hjärtrytm (sjuk sinusknuta eller höggradigt atrioventrikulärt block) eller ventrikelarytmi.
EKG-förändringarna är ofta ospecifika men kan likna dem som ses vid perikardit. Ekokardiografi kan påvisa perikardvätska eller intrakardiell tromb men behöver ibland kompletteras med datortomografi (DT), eftersom förekomst av kompartmentalisering kan vara värdefull information inför perikardiocentes. Ekokardiografi är dessutom en hörnsten i monitorering av patient med myokardit och nedsatt kammarfunktion, men också för att utesluta/påvisa annan samtidig hjärtmuskelsjukdom eller klaffvitium.
Koronarangiografi för att utesluta ischemi bör övervägas hos patienter med myokardit, utifrån kardiovaskulär riskfaktorprofil och klinisk bild [3]. Enligt ESC:s riktlinjer är endomyokardiell biopsi indicerad hos alla med misstänkt myokardit [3]. Myokardit definieras som histologisk bild av inflammatoriska infiltrat samt nekros.
Kliniskt misstänkt myokardit definieras som ≥1 kliniskt symtom och ≥1 diagnostiskt kriterium eller ≥2 diagnostiska kriterier. Rekommendationen bygger på expertkonsensus och tillämpas inte fullt ut i svensk klinisk praxis. Tidig biopsi är viktig för att möjliggöra specifik behandling mot infektion eller med immunsuppression. I Sverige biopseras generellt få patienter, och då oftast bara de svårast sjuka sent i förloppet.
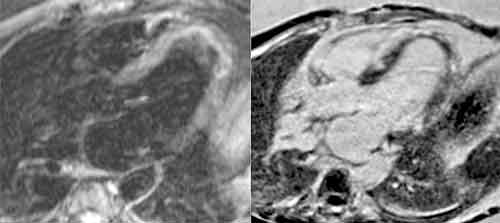
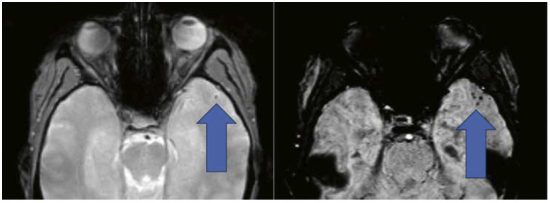
Ett icke-invasivt sätt att stödja diagnosen myokardit är magnetkameraundersökning av hjärtat (MR-hjärta), och Lake Louise-kriterierna kan användas [3]. Enligt ESC är bilden vid MR-hjärta överstämmande med myokardit om den hos patient med kliniskt misstänkt myokardit uppfyller minst 2 av 3 Lake Louise-kriterier:
- högsignalering på T2-viktade bilder (tyder på ödem)
- tidig uppladdning av gadoliniumkontrast (tyder på ökad blodgenomströmning)
- sen uppladdning av gadoliniumkontrast (tyder på ärrvävnad).
MR-hjärta kan också visualisera inflammation och svullnad i perikardiet. Positronemissionstomografi (PET) rekommenderas inte rutinmässigt i utredning av myokardit, men fluorodeoxiglukos-PET kan vara värdefull vid misstänkt hjärtsarkoidos.
Behandling och uppföljning
Perikardit
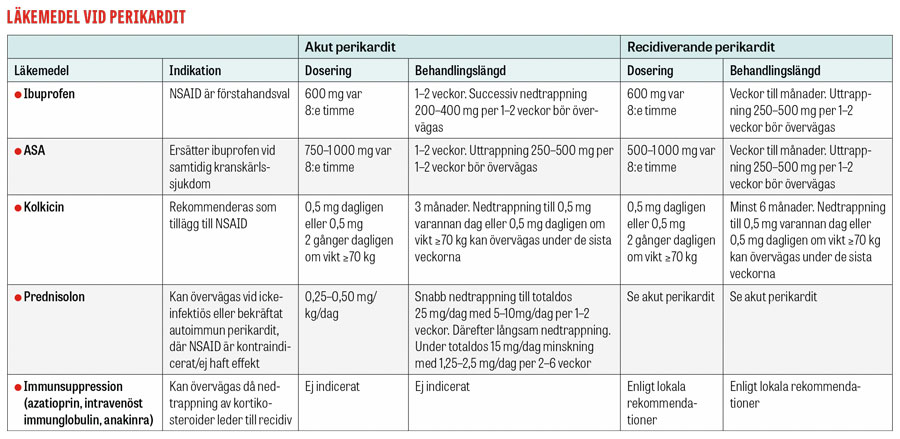
Perikardit har i regel god prognos, och vid okomplicerade fall utan riskfaktorer kan patienten handläggas polikliniskt med acetylsalicylsyra (ASA) eller andra icke-steroida antiinflammatoriska läkemedel (NSAID), med tillägg av kolkicin [2]. Uppföljning bör ske efter 1 vecka med utvärdering av symtom och CRP. [2]. Vid perikardit är det angeläget att värdera förekomst av perikardvätska som kan leda till tamponad och att förebygga utveckling av konstriktiv perikardit.
Vid idiopatisk/viral etiologi inträffar kliniskt betydande konstriktiv perikardit hos mindre än 1 procent. Om en eller flera riskfaktorer föreligger ökar risken för komplikationer, och inläggning och utredning av specifik etiologi rekommenderas i dessa fall [2, 4]. Hos individer från tuberkulosendemiska områden måste tuberkulos uteslutas som orsak till perikardit. Utredning krävs också hos patienter där man har misstanke om annan specifik etiologi, t ex vid autoimmun sjukdom.
ASA/NSAID utgör basen för behandling vid perikardit och är symtomlindrande, men det är osäkert om det påverkar sjukdomsprocessen [5]. De patienter som inte förbättras efter 1 vecka bör läggas in för utredning. Utebliven förbättring efter 1 vecka med ASA/NSAID talar emot godartad idiopatisk/virusutlöst perikardit och indikerar sämre prognos [2, 4].
Vid samtidig kranskärlssjuka rekommenderas i första hand ASA, i övriga fall rekommenderas NSAID (t ex ibuprofen) [2, 5]. De doser som är rekommenderade vid perikardit är höga och bör sättas in tillsammans med gastroprotektion i form av protonpumpshämmare. Kolkicin minskar risken för recidiv och har en fördelaktig risk–nyttaprofil vid perikardit [6]. Kolkicin bör övervägas som tillägg till ASA/NSAID, särskilt vid recidiv.
Kortikosteroider har länge använts vid behandling av perikardit. De ger snabb symtomregress och minskad mängd perikardvätska, men ökar risken för recidiv och anses numera kontraindicerade. I svåra fall, utan effekt av annan behandling och där infektiös etiologi har uteslutits kvarstår dock kortikosteroider som ett alternativ. Immunmodulerande terapier som intravenöst immunglobulin, azatioprin eller anakinra kan övervägas om nedtrappning av kortikosterioder leder till recidiv [2].
Perikardektomi kan övervägas som en sista behandlingsmöjlighet.
Patienter med perikardit bör avstå från fysisk ansträngning till dess att symtom, CRP, EKG och ekokardiografifynd normaliserats. Elitidrottare rekommenderas att avstå från fysisk ansträngning i minst 3 månader [2]. Vid myoperikardit bör de striktare restriktionerna som rekommenderas vid myokardit (minst 6 månader) följas [2, 3]. Dessa rekommendationer baseras på expertkonsensus och den allmänna principen om att avstå från fysisk ansträngning i samband med infektion samt kopplingen mellan fysisk ansträngning och plötslig hjärtdöd [2, 3, 7].
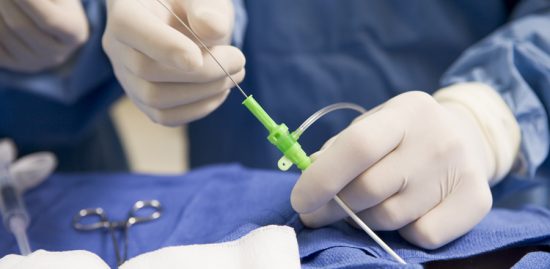
Tamponad är en livshotande komplikation som ofta förekommer tidigt i sjukdomsförloppet, och symtomen är därför viktiga att känna igen [2]. Stor mängd perikardvätska kan tolereras om den utvecklas över längre tid, medan redan mindre mängd snabbt tilltagande perikardvätska kan ge cirkulatorisk påverkan [2]. Perikardvätskan påverkar höger kammares fyllnad. Perikardiocentes kan vara livräddande vid tamponad. Perikardiocentes rekommenderas även vid symtomgivande måttlig (≥10 mm) eller uttalad (≥20 mm) mängd perikardvätska.
Perikardiocentes ska övervägas i diagnostiskt syfte om misstanke finns om tuberkulos, annan bakteriell infektion eller neoplasi.
Konstriktiv perikardit utvecklas över tid, är vanligare vid icke-viral/icke-idiopatisk genes och manifesterar sig som subakut kronisk perikardit [2]. Kliniskt ses tecken på högersidig hjärtsvikt. En differentialdiagnos är restriktiv kardiomyopati. DT- och MR-hjärta kan skärpa diagnostiken genom att påvisa förändringar som förtjockat och förkalkat perikardium. Vid konstriktiv perikardit som inte svarar på farmakologisk behandling kan perikardektomi övervägas.
Myokardit
Alla patienter med myokardit bör utredas och vårdas inneliggande på sjukhus. Vid idiopatisk myokardit saknas specifik behandling för grundsjukdomen. NSAID och kortikosteroider misstänks öka mortaliteten och är kontraindicerade [3]. Om den histologiska bilden vid endomyokardiell biopsi talar för jättecellsmyokardit eller sarkoidos kan kortikosteroider övervägas [3]. Polymeraskedjereaktion (PCR) av virus-RNA från myokardiet och blod används för att upptäcka eller utesluta viral etiologi, och utifrån detta kan specifik antiviral terapi eller immunsuppression väljas/sättas in.
Initialt omhändertagande inriktas på behandling av komplikationer som arytmi eller hjärtsvikt. Återkommande ventrikeltakykardi kan förebyggas med betablockerare och amiodaron [8]. Vid ihållande monomorf ventrikeltakykardi eller elektrisk storm (återkommande episoder av ventrikeltakykardi), där substratet misstänks vara ärrvävnad, bör akut kateterablation övervägas [8]. Vid elektrisk storm kan ibland sövning tillgripas för att hantera arytmisituationen.
Myokarditorsakad hjärtsvikt behandlas enligt allmänna principer, inklusive betablockerare, angiotensinkonverterande enzymhämmare/angiotensinreceptorblockerare och aldosteronreceptorblockerare [3, 9]. Impeller eller extrakorporeal membranoxygenering (ECMO) kan övervägas vid livshotande hjärtsvikt och hemodynamisk instabilitet för att överbrygga tiden till återhämtning, till mekanisk hjärtpump (HeartMate 3) eller hjärttransplantation. I efterförloppet måste risken för plötslig hjärtdöd värderas.
Det kan finnas skäl för implanterbar defibrillator (ICD) [8]. Då myokarditen förväntas läka ut och patienten behöver temporärt skydd mot plötslig död kan en väst med bärbar defibrillator (wearable cardioverter-defibrillator, WCD) vara ett alternativ i utvalda fall [8, 10].
Rekommendationerna för restriktioner och uppföljning avseende fysisk aktivitet efter myokardit liknar dem vid perikardit, men elitidrottare och även icke-elitidrottare rekommenderas avstå från träning i minst 6 månader [3].
Prognos
Prognosen vid både perikardit och myokardit är generellt god, men varierar med etiologi. Vid myokardit finns risk för att utveckla nedsatt kammarfunktion, och prognosen är då sämre liksom vid hjärtsvikt av andra orsaker. I sällsynta fall förekommer akut kardiogen chock eller arytmiorsakad plötslig hjärtdöd.
Av patienter med biopsiverifierad myokardit utvecklar 30 procent dilaterad kardiomyopati [3]. Vid perikardit är recidivrisken betydande, 15–30 procent för idiopatisk perikardit utan kolkicinbehandling [2]. Recidiv kan påverka livsföringen men har inte kopplats till ökad risk för konstriktiv perikardit eller andra allvarliga komplikationer.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.








![Histologisk bild av akut lymfocytär myokardit (hematoxylin–eosin-färgning, förstoring 100 gånger). Från González J, et al [11].](https://lakartidningen.se/wp-content/uploads/EditorialFiles/7I/%5bET7I%5d/2017-115_2_webb.jpg)