Ärftliga trombocytopenier kan feldiagnostiseras som immunologisk trombocytopeni (ITP).
Fel diagnos kan leda till onödig och overksam terapi.
En enkel undersökning (blodfilm) kan inleda utredningen och leda till rätt diagnos för patienter med misstänkt MYH9-relaterad trombocytopeni.
Immunologisk trombocytopeni (ITP) är en hematologisk sjukdom som kännetecknas av trombocytopeni baserad på autoimmunitet. Sjukdomen har oftast ett kroniskt förlopp hos vuxna och ger blödningsmanifestationer i varierande grad. Pålitliga sjukdomsspecifika markörer saknas, och diagnosen baseras fortfarande på att utesluta andra orsaker till trombocytopenin. Mer sällsynta orsaker till trombocytopeni såsom ärftliga trombocytopenier brukar inte ingå i differentialdiagnostiken hos vuxna patienter, och trombocytopenin kan därför misstolkas som ITP [1].
Under de senaste åren har kunskapen om ärftliga trombocytopenier ökat avsevärt. Tidigare kände man bara till de två mest symtomgivande ärftliga trombocytopenierna (Bernard–Souliers syndrom och Wiskott–Aldrichs syndrom) vilka diagnostiserades tidigt under barndomen. Med den förbättrade genetiska kartläggning som finns i dag kan man identifiera fler än 20 enskilda ärftliga trombocytopenier [2]. Dessa ärftliga syndrom ger kronisk medfödd trombocytopeni i olika nivåer med extremt varierande grad av blödningssymtom – från svåra blödningar till helt symtomfria tillstånd. Trombocytopenin kan vara en isolerad sjukdomsmanifestation eller en del av ett syndrom med andra somatiska manifestationer såsom defekter i inre organ.
Vi beskriver här ett fall där en patient med ärftlig trombocytopeni feldiagnostiserades och behandlades för ITP under knappt 50 år. Patientens skriftliga godkännande för publikation föreligger.
Fallbeskrivning
Den kvinnliga patienten remitterades till hematologimottagningen för bedömning av en känd kronisk trombocytopeni inför planerad njurtransplantation. Anamnesen gav följande: 51-årig kvinna utan ärftlighet till blodsjukdom. Inga barn, fem friska syskon.
Vid 3 års ålder utreddes patienten för blåmärken, näsblödningar och trombocytopeni (TPK-värden 10–30 × 109/l) och fick diagnosen ITP. Behandling med kortison i varierande doser inleddes utan någon påverkan på trombocytvärden eller blödningssymtom. Diagnosen ITP bekräftades efter en ny grundligare utredning på universitetssjukhus, och patienten genomgick splenektomi vid 5 års ålder. Vid 14 års ålder upptäcktes progredierande proteinuri och njursvikt, vilket tolkades som kronisk glomerulonefrit. På grund av blödningsrisken togs ingen biopsi. Patienten fick ett första njurtransplantat vid 23 års ålder och ett andra vid 33 års ålder. Ännu en transplantatrejektion och njursvikt vid 49 års ålder ledde till hemodialys, och planeringen för en tredje njurtransplantation påbörjades. Inför denna transplantation förbereddes patienten med rituximab-infusioner.
Patienten hade sedan barndomen en långsamt progredierande bilateral hörselnedsättning som föranledde hörapparat vid 39 års ålder och fullständig dövhet vid 48 års ålder.
Patienten har även haft varierande sjukdomsmanifestationer med hud- och slemhinneblödningar. En spontan abort och kroniskt rikliga menstruationer föranledde hysterektomi vid 28 års ålder.
I samband med olika operationer har profylaktisk behandling mot blödning med trombocyttransfusioner och tranexamsyra haft bra effekt. Även trombocytvärdena har förbättrats efter transfusion. Kortisonbehandlingarna har genom åren gett biverkningar med bland annat osteoporos, upprepade infektioner och bilateral kaputnekros i höftlederna. Under åren har behandlingsförsök i olika omgångar genomförts med bland annat plasmaferes, intravenöst immunglobulin, danazol, azatioprin, kortikosteroider och rituximab.
Vid den kliniska undersökningen under det aktuella vårdtillfället inför njurtransplantationen mådde patienten bra och hade inga pågående blödningsmanifestationer. Laboratorieprovet visade TPK på 30–50 × 109/l. Inför den planerade operationen gjorde man ett behandlingsförsök med TPO-R (trombopoetinreceptor)-agonisten eltrombopag (50 mg dagligen) med bra effekt. TPK-värdena steg upp till 150 × 109/l som högst. Inför operationen fick patienten en mycket svår legionellapneumoni som resulterade i två månaders sjukhusvistelse och en terminal utgång.
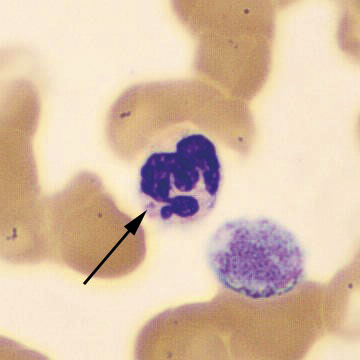
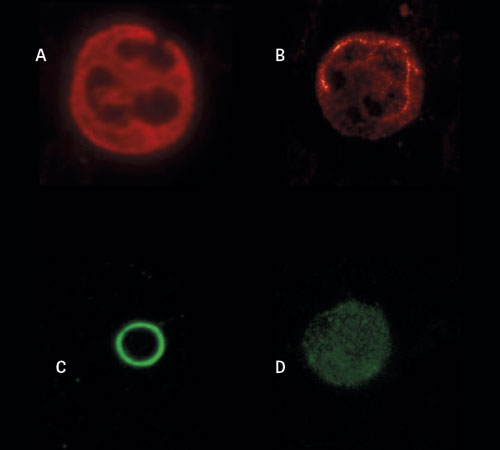
Patientens sjukdomshistoria, frånvaron av terapeutiskt svar på givna immunhämmande/immunmodulerande behandlingar och förekomsten av andra organmanifestationer (njurar och hörsel) gav misstanke om ärftliga trombocytopenier av typen MYH9-relaterad sjukdom (MYH9-RD). Blodfilm påvisade stora trombocyter, Figur 1. Immunfluorescens med anti-NMMIIa (icke-muskulär myosin IIa)-antikroppar påvisade inklusionspartiklar och en patologisk anordning av beta-tubulin i neutrofila celler vilka båda är typiska för MYH9-RD, Figur 2.
Genetisk analys identifierade en patogen heterozygot mutation i MYH9-genen (c.2104C>T[p.Arg702Cys]). Mutationen ligger i området som kodar för NMMIIa-strukturens huvud och har beskrivits tidigare vid MYH9-RD [3].
Inga laboratorieundersökningar av släktingar kunde utföras. Med tanke på symtomfrihet hos föräldrar och alla syskon verkar patientens sjukdom bero på en de novo-mutation.
Diskussion
Denna patient hade en klassisk manifestation av en MYH9-RD. Olika syndromkombinationer inom sjukdomsgruppen har tidigare delats in i May–Hegglin-anomali, Epsteins syndrom, Fechtners syndrom och Sebastians trombocytsyndrom.
Systematiska genanalyser i familjer med flera drabbade personer har lett till att man kunnat identifiera området för den genetiska defekten som ger upphov till denna grupp av autosomalt dominant ärvda syndrom. Ett flertal olika syndromframkallande mutationer i MYH9-genen är kända, samtliga i heterozygot form. MYH9 kodar för motorproteinet NMMHC-IIA (icke-muskulärt myosin, tunga kedjor IIa), ett protein som förekommer i en mängd olika vävnader, vilket förklarar förekomsten av de olika organpåverkande symtomen. Gendefekten påverkar bildning av trombocyter och leder till makrotrombocytopeni. Syndromen är i varierande grad associerad med sensorineural hörselnedsättning, njurfunktionsnedsättning och presenil katarakt. Patienternas fenotyp, inkluderande graden av trombocytopeni och blödningsmanifestationer, varierar beroende på vilken mutation som föreligger och var i genen[4].
MYH9-RD är en av de vanligaste orsakerna till ärftliga trombocytopenier [2]. Incidensen är inte kartlagd. Sjukdomen har ingen specifik behandling. Patienter med MYH9-RD svarar bra på trombocyttransfusioner som kan ges vid blödningskomplikationer och inför kirurgiska ingrepp. Tranexamsyra och desmopressin har beskrivits som effektiva blodstillande medel vid blödning, men några bra referensstudier finns inte. På grund av återkommande blödningar kan järnsubstitution vara indicerad. Patienter med MYH9-RD kan svara långsiktigt på behandling med TPO-R-agonister (eltrombopag eller romiplostim) [5, 6], men några kliniska studier med risk–nytta-analys finns inte. Behandling med ACE-hämmare respektive angiotensinreceptorantagonister kan eventuellt fördröja njurskadan. Splenektomi ger ingen nytta.
Liksom andra patienter med ärftliga trombocytopenier riskerar patienter med MYH9-RD att bli feldiagnostiserade med ITP, med efterföljande ineffektiv och potentiellt skadlig behandling. Vidare förlorar sjukvården möjligheten att förbereda patienten på de organmanifestationer som kan uppstå samt möjligheten till genetisk rådgivning. Sjukdomsmanifestationerna kan komma i vuxen ålder, blödningssymtomen är oftast lindriga och oproportionella till trombocytantalet och eftersom utredning för ärftliga trombocytopenier inte ingår vid rutindiagnostiken vid trombocytopeni hos vuxna patienter kan det feltolkas som ITP.
Patienten i det presenterade fallet gick odiagnostiserad/feldiagnostiserad i nästan 50 år och undergick hela arsenalen av ITP-behandlingar, och de därmed relaterade svåra biverkningarna, till ingen nytta. Det beskrivna fallet är ett lärorikt exempel på vilka risker dessa patienter kan utsättas för.
Lärdomar från patientfallet
Ärftliga trombocytopenier bör misstänkas och utredas hos patienter som har kronisk trombocytopeni och dessutom:
- har känd ärftlighet till trombocytopeni
- har blödningsmanifestationer oproportionella (för mycket eller för lite) till trombocytopenigraden
- har associerade inre organmanifestationer (t ex njursvikt)
- har för stora trombocyter
- är oförväntat refraktära till immunhämmande/immunmodulerande ITP-behandling och/eller splenektomi.
En enkel mikroskopisk undersökning av blodfilm (påvisar makrotrombocyter) samt efterföljande immunhistologi (påvisar inklusionskroppar i granulocyter) och riktad genotypning kan säkra diagnosen [7].
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.