Hypertrofisk kardiomyopati är den vanligaste kardiogenetiska hjärtmuskelsjukdomen. Symtom är främst andfåddhet, bröstsmärta, yrsel och svimning.
Ekokardiografi visar väggtjocklek på minst 15 mm, som inte förklaras av hemodynamiska förhållanden.
Genetisk undersökning rekommenderas och används i släktutredning.
Betablockad ges vid symtom (alternativt verapamil eller disopyramid).
Förmaksflimmer är vanligt, och antikoagulation och rytm-/frekvensreglering behövs.
Intern defibrillator förebygger död i arytmi hos personer med riskfaktorer.
Sjukdomen har ofta ett godartat förlopp, men den är heterogen, och individualiserad bedömning krävs. Sjukdom med nedsatt ejektionsfraktion innebär dyster prognos.
Sjuklig förtjockning av hjärtmuskeln som huvudsakligen orsakas av primära förändringar i muskelns byggstenar benämns hypertrofisk kardiomyopati. Med en förekomst av 1/500–1/1 000 är hypertrofisk kardiomyopati den vanligaste ärftliga hjärtsjukdomen [1]. Sedan 1990 har man påvisat fler än 1 400 mutationer i minst 11 gener som är associerade med hypertrofisk kardiomyopati [2]. Närmare 70 procent av de personer där en sjukdomsorsakande gen anses förklara sjukdomen har mutationer i MYH7- eller MYBPC3-generna, som reglerar uttrycket av kontraktila muskelfilament [3, 4]. Varje släkt med hypertrofisk kardiomyopati har sin specifika mutation, vilket kan användas vid klinisk utredning av medlemmarna [5].
Förutom variationer i genuttrycken bidrar också andra orsaker till den heterogena kliniska bilden hos personer med sjukdomen. I en familj med samma mutation kan många olika kliniska uttryck ses. Penetransen är variabel och beror på bl a ålder och sjukdomsgen, men merparten av dem som bär på ett sjukdomsanlag får symtom under livet [6].
Beskrevs redan för 150 år sedan
För mer än 50 år sedan beskrevs patologin [7], men redan 100 år tidigare hade sjukdomen beskrivits för första gången [8, 9]. Fallrapporter 1964 beskrev utredning och behandling med myektomi vid »idiopatisk hypertrofisk subaortal stenos« [10]. Därefter följde mer än 70 olika benämningar på sjukdomen, som numera bör kallas enbart hypertrofisk kardiomyopati [11, 12].
Trots att detta är den vanligaste genetiska kardiovaskulära sjukdomen kan de skiftande begreppen ha bidragit till att en systematisk kunskapsöversikt försvårades, men det kan också vara ett uttryck för sjukdomens mångsidiga uttryck och komplexitet, vilket kräver särskild eftertanke i utredning och behandling.
Majoriteten har endast lindriga symtom – eller inga alls
Andfåddhet, bröstsmärta, yrsel och svimning förekommer, men majoriteten saknar eller har endast lindriga symtom [2, 6]. Beroende på funktionsnivå påverkas tillvaron i olika grad. De allra flesta kan dock leva ett tämligen normalt liv och begränsas enbart i speciella situationer.
Fysisk ansträngning, intag av större måltid, alkoholintag eller vätskebrist kan utlösa symtom. Även läkemedel som har kärlvidgande eller vätskedrivande effekt kan bidra till symtom. Patienter med betydande tryckskillnad över utflödestrakten i vänsterkammaren (utflödesobstruktion) kan uppleva svår andfåddhet, yrsel eller till och med svimma.
Andfåddhet utan samtidig utflödesobstruktion tillskrivs framför allt relaxationsstörningen av vänsterkammaren och kan föregå en påvisbar systolisk nedsättning under lång tid. Vid hastigt påkommen dyspné bör tillkomst av förmaksarytmi misstänkas.
Bröstsmärtan är ofta av diffus karaktär, och avgränsningen mot kranskärlssjukdom är ibland svår. Histopatologiskt ses ofta småkärlssjukdom, och denna kan vara symtomgivande även i fall där kranskärlsröntgen inte kan påvisa signifikanta förändringar.
Yrsel kan förekomma i vila eller vid fysisk ansträngning. Hemodynamiska förändringar men också arytmi kan ge besvär som patienten beskriver som yrsel eller svimningskänsla.
Svimning, särskilt vid ansträngning, kan bero på förändrad hemodynamik, särskilt hos personer med utflödesobstruktion [13]. Antingen långsam eller snabb hjärtrytm måste dock alltid övervägas.
Upptäcks ibland vid hälsoundersökning
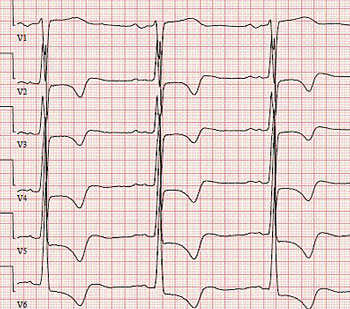
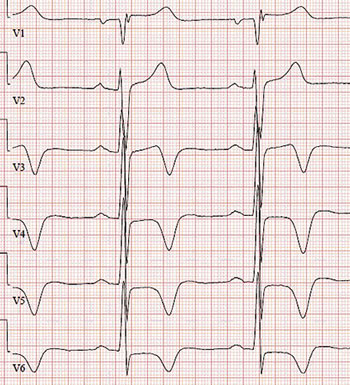
Förutom nämnda symtom kan utredning i annat sammanhang leda till upptäckt av sjukdomen. Hjärtauskultation görs ofta rutinmässigt, och blåsljud kan ibland höras. EKG-förändringar i form av hypertrofitecken och patologiska T-vågor kan ibland inge misstanke om sjukdomen och leda till ultraljudsundersökning (Figur 1 och 2).
Hälsoundersökningar liksom riktad släktutredning kan ibland identifiera individer utan symtom. Socialstyrelsen rekommenderar kaskadtestning, vilket innebär att man gör en släktutredning utgående från indexfall med diagnos.
Riksidrottsförbundet rekommenderar screening av elitidrottare i flera grenar. Screening kan innefatta anamnes, EKG och ibland ekokardiografi [14]. Frågan om generell screening av idrottsutövare har utretts av Socialstyrelsen i Sverige år 2006, och då föreslogs i stället riktade undersökningar av riskgrupper. Europeiska kardiologföreningen däremot rekommenderar screening av bredare grupper av idrottare [15].
Bilddiagnostik med bland annat ultraljud och doppler
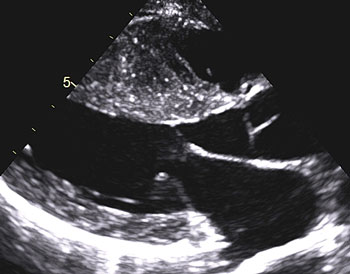
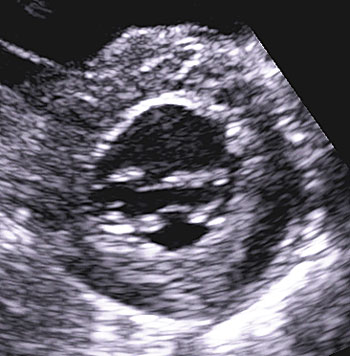
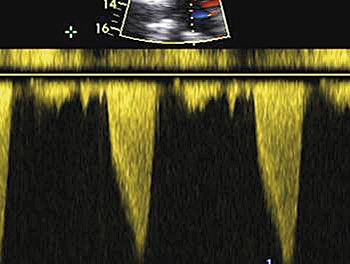
Ultraljudsundersökning av hjärtat påvisar hypertrofi – oftast i kammarseptum, men alla delar av hjärtat kan påverkas (Figur 3, 4 och 5). Det förekommer en variant med enbart apikal hypertrofi. Med dopplerundersökning kan förhöjda hastigheter över vänsterkammarens utflödesregion påvisas i vila hos ungefär en tredjedel, medan hos ytterligare cirka en tredjedel förhöjd gradient (tryckskillnad) kan provoceras fram genom fysiologisk belastning, Valsalvas manöver eller läkemedel. Den metod som numera rekommenderas är fysiologisk belastning på cykelergometer eller gångmatta, vilket är av värde om ingen gradient ses vid vila då anamnesen indikerar en dynamisk gradient.
Inte sällan ses läckage i mitralisklaffen och en framåtgående rörelse av vanligtvis det främre klaffseglet under systole. Vänster förmak kan vara förstorat sekundärt till höga fyllnadstryck.
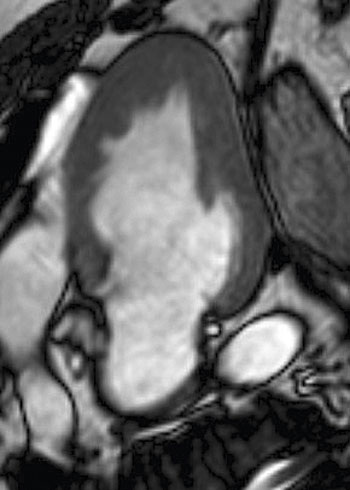
Med magnetkamera kan svårundersökta delar, t ex apex (Figur 6 och 7), och mitralisklaffens funktion ibland bättre bedömas [16]. I riskvärdering för död i arytmi används ibland variablerna sent gadoliniumupptag och förekomst av aneurysm, men kunskapsläget är inte helt klarlagt [17]. Magnetkameran kan bidra till att påvisa inlagringssjukdomar som hjärtamyloidos [18] och Fabrys sjukdom [19].
Positronemissionstomografi (PET) kan påvisa förändringar i blodflöde och metabolism. Hos patienter med hypertrofisk kardiomyopati verkar minskad blodflödesreserv vara associerad med ökad dödlighet [20]. I rutinsjukvård har dock PET i nuläget ingen plats.
Histologisk diagnostik stärker sällan terapeutiska beslut
I mikroskop ses en fläckvis störd ordning av muskelcellerna; cellstorleken varierar påtagligt, och större områden av fibros kan ses [2]. Historiskt har biopsi ibland utförts, men negativt utfall utesluter inte sjukdomen. I skenet av övrig modern diagnostik tillför biopsi sällan något för terapeutiska beslut, men kan vara av betydelse vid obduktion för att fastställa dödsorsak.
Genetisk utredning bör erbjudas
Patienter med hypertrofisk kardiomyopati bör erbjudas genetisk utredning vid kardiogenetisk mottagning på universitetssjukhus med multidisciplinär kompetens i kardiologi, klinisk genetik och barnkardiologi [6]. I ungefär hälften av fallen hittas en genetisk avvikelse (mutation) som förklarar sjukdomen. Indexpatientens mutation kan sedan sökas hos föräldrar, syskon och barn (förstagradssläktingar). Påvisande av genetisk avvikelse kan sedan leda till utredning av ytterligare släktingar. Om samma mutation påvisas hos släktingen bör komplett utredning och riskvärdering göras och återkommande uppföljning ske. Om mutationen däremot saknas, kan misstanken avskrivas och utredningen avslutas.
Om indexpatienten däremot saknar genetisk avvikelse vid primärutredningen måste släktingarna i stället genomgå återkommande kliniska undersökningar, eftersom negativt gentest inte utesluter ärftlig sjukdom och penetransen varierar påtagligt.
Själva provtagningen är enkel, ett venöst blodprov tas, men det kan ta flera månader innan den genetiska analysen är fullständig. När en sjukdomsgen väl är känd går det betydligt snabbare att få svar på efterföljande anlagsbärartest.
Uppföljning av vuxna släktingar med 2–5 års intervall
Hos vuxna mutationsbärare (eller förstagradssläkting till sjuk individ i familjer utan känd mutation) som ännu inte utvecklat symtom rekommenderas kontroller med EKG och ekokardiografi med ett intervall på 2–5 år [6]. Eftersom sjukdomen kan ha ett variabelt förlopp bör utredning göras frikostigt även vid tillkomst av misstänkta symtom. För ungdomar mellan 10 och 20 år bör screening göras med 1–2 års intervall. För barn yngre än 10 år görs mera individualiserad bedömning av barnkardiolog. Vid vissa mottagningar förordas kontroller från 6 års ålder.
Faktorer som motiverar tidigare utredning är misstänkta symtom, intensiv träning eller släkthistoria med allvarlig händelse till följd av hypertrofisk kardiomyopati [6].
Uppföljning av patient med 1–2 års intervall
Standard-EKG med 12 avledningar, 48-timmars-EKG och ekokardiografi bör göras med 1–2 års intervall hos person med fastställd sjukdom där undersökningsresultaten kan ha betydelse för behandling eller riskvärdering. Arbets-EKG ska övervägas med 2–3 års intervall [6].
Läkemedelsbehandling – hos vuxna med symtom
Större randomiserade humanstudier på läkemedel för att minska sjukdomsprogressen saknas [21]. Hos patienter helt utan symtom bör därför behandlingen riktas mot annan samsjuklighet snarare än rutinmässig förskrivning av betablockad eller kalciumantagonister. Hos vuxna patienter med symtom rekommenderas betablockad, medan behandling hos asymtomatiska patienter får anses kontroversiell.
Om betablockad ger biverkan eller inte har tillräcklig effekt kan kalciumantagonisten verapamil prövas. Försiktighet vid hög utflödesgradient bör iakttas, och vid nedsatt systolisk kammarfunktion eller bradykardi bör verapamil seponeras. Disopyramid i kombination med antingen betablockad eller verapamil kan vara ett alternativ vid obstruktiv bild om symtombördan är svår. Antikolinerg biverkan begränsar preparatets användning.
Septal reduktion med myektomi eller alkoholablation
Hos patienter med svår symtombörda (till följd av utflödesobstruktion) som påverkar livskvaliteten kan invasiv strategi övervägas, även om randomiserade studier saknas [22]. Det förutsätter dock att läkemedel i optimal och tolerabel dos först prövats. Vid traditionell myektomi (Morrow-procedur) görs sternotomi och en ca 3 cm lång resektion av kammarseptum [23]. I vissa fall utförs en utvidgad resektion på 7 cm [24]. Ibland behövs samtidig plastik av mitralisklaffen.
Vid alkoholablation ges 1–3 ml etanol lokalt i en septalgren av kranskärlet som försörjer septum. Detta görs under samtidig undersökning med ultraljud för att säkerställa korrekt utbredning. Etanolen leder till att myokardiet som försörjs av kärlet går i nekros och skrumpnar. Först efter 3 månader kan effekten av septumreduktionen vara fullbordad.
Generellt lämpar sig myektomi för den yngre patienten och alkoholablation för den äldre, men det förutsätter att det finns lämplig kranskärlsanatomi [25]. Vid framför allt alkoholablation kan AV-noden skadas, vilket medför behov av permanent pacemaker [26].
Bägge metoderna ska användas endast vid centrum med god erfarenhet av dessa behandlingar.
I Sverige har de senaste 10 åren totalt drygt 100 myektomier respektive 300 alkoholablationer genomförts [27].
Nedsatt ejektionsfraktion ger hjärtsvikt
Hos en del patienter sker efter lång sjukdomsduration en försämring av den systoliska kammarfunktionen med påtaglig dyspné och dyster prognos som följd. Måttet ejektionsfraktion (mätt som den andel av slagvolymen som pumpas ut från vänsterkammaren vid varje hjärtslag) är ofta hög, men när den sjunker till värden under 50 procent är det förenligt med hjärtsvikt. Bilden förändras med ofta minskande hypertrofi och dilatation av hjärtrummen. Sedvanlig läkemedelsbehandling med betablockad, ACE-hämmare/angiotensinreceptorblockerare och aldosteronreceptorblockerare ges då. Ofta kompliceras bilden av samtidigt förmaksflimmer, vilket kräver särskilda överväganden.
Hos biologiskt yngre patienter kan utredning och behandling avseende mekaniskt vänsterkammarstöd och hjärttransplantation bli aktuell. Biventrikulär pacemakerbehandling vid samtidigt vänstersidigt grenblock kan prövas, och det förefaller som om behandlingssvaret kan vara gott – men med individuella skillnader [28].
Förmaksflimmer drabbar ofta särskilt svårt
Förmaksflimmer kan genom embolisering orsaka stroke eller annan systemisk infarkt, vilket motiverar antikoagulation hos patienter med hypertrofisk kardiomyopati oavsett CHA2DS2-VASc-poäng; warfarin är väl empiriskt prövat i patientgruppen. Direktverkande antikoagulantia (NOAK) har inte specifikt prövats i randomiserade studier men kan ändå anses möjliga mot bakgrund av studier på andra patientgrupper; en observationell studie stödjer detta [29].
Patienter med hypertrofisk kardiomyopati drabbas ofta särskilt svårt av förmaksflimmer. Det uteblivna förmaksbidraget till slagvolymen och ytterligare störd diastole till följd av oregelbunden kammarrytm och initialt hög frekvens är särskilt deletär. Ofta eftersträvas rytmkontrollerande strategi, vilken dessvärre begränsas av kontraindikationer för vissa antiarytmika. Emellanåt prövas antiarytmika, särskilt om patienten har en implanterbar defibrillator. Amiodaron har recidivprofylaktiska effekter, men långtidsanvändning begränsas av toxicitet på framför allt sköldkörtel men också lever, lungor och hud. Dronedaron har inte specifikt prövats på denna indikation, och vid hjärtsvikt och/eller permanent förmaksflimmer ska det undvikas.
Kateterburen lungvensisolering kan fungera, men långtidsresultaten är okända och recidivrisken påtaglig.
En definitiv åtgärd för frekvenskontroll är kateterburen destruktion av övergången mellan förmak och kammare, s k His-ablation. Proceduren är relativt säker men irreversibel och kräver därför en fungerande kammarstimulerande pacemaker.
Pacemaker används alltmer sällan
Vid stimulering från höger kammares apex fås ofta en mätbart minskad utflödesgradient. Tidigare implanterades därför pacemaker för att minska symtom. Motstridiga resultat från randomiserade studier gjorde metoden mindre använd [30-34]. Möjligen kan pacemaker övervägas hos en äldre patient med uttalad utflödesgradient trots läkemedelsoptimering och där septumreduktion inte är möjlig [6].
Hos patienter med pacemaker eller intern defibrillator av annat skäl kan dock försök med kammarstimulering göras. Pacemakerns överledningstider bör då programmeras utifrån mätning av utflödesgradient med ultraljud och klinisk värdering.
Graviditet säker vid god symtomkontroll
Vid god symtomkontroll anses graviditet och förlossning säker. Hos kvinnor med symtomatisk hypertrofisk kardiomyopati ska samråd ske mellan obstetriker, anestesiolog och kardiolog vid specialiserat centrum. Läkemedelsbehandling med betablockad bör fortgå men kan ge långsam puls hos barnet. Vid hög utflödesgradient (mer än 50 mm Hg) eller symtom anses risken högre för modern, men graviditet är fortfarande möjlig. Om patienten har systolisk svikt avråds från graviditet [35].
Det är viktigt att kvinnan får information om sjukdomens ärftlighet.
Idrott och träning – måttlig fysisk aktivitet är värdefull
I en ofta citerad studie från USA där man obducerat idrottare som avlidit plötsligt sågs hypertrofi hos närmare hälften [36, 37]. Även ett stort antal fallrapporter visar på samband mellan kraftig ansträngning och död. Mot denna bakgrund avråds patienter från högintensiv idrott med tempoväxlingar, men också idrotter med uttalad statisk belastning, t ex tyngdlyftning [6, 38]. Risken för svimning måste beaktas, t ex vid dykning och höghöjdsaktiviteter. Rådgivningen bör ske mot bakgrund av individuell klinisk profil och aktivitet.
Måttlig fysisk aktivitet får däremot anses värdefull mot bakgrund av den sammantagna hälsobefrämjande effekten.
Risken för arytmiorsakad död välkänd
Dödligheten hos patienter med hypertrofisk kardiomyopati är hos flertalet jämförbar med den hos normalbefolkningen [39, 40]. Sjukdomen är dock heterogen. Det finns ökad risk för stroke och hjärtsvikt, vilket är förknippat med ökad dödlighet. Risken för arytmiorsakad död är välkänd och kräver särskild riskvärdering. Plötslig död förekommer utan tidigare sjukvårdskontakt, och det understryker betydelsen av utredning även av mera subtila symtom och spridning av kunskap kring sjukdomen.
Intern defibrillator kan förhindra plötslig död
En intern defibrillator utgör ett effektivt sätt att bryta livshotande ventrikulära rytmrubbningar. Det är därför angeläget att riskvärdera patienter med hypertrofisk kardiomyopati och erbjuda en implanterbar defibrillator i selekterade fall [2, 6, 41].
Efter överlevt ventrikelflimmer eller ihållande ventrikeltakykardi bör patienten självklart erbjudas en implanterbar defibrillator efter grundlig information. Sannolikheten för adekvat chockbehandling av ventrikelarytmi uppgår i sekundärpreventiva fall till drygt 10 procent årligen [42].
Hos övriga patienter bör individualiserad riskvärdering göras, där samsjuklighet och förväntad överlevnadstid skattas. Det finns två modeller för detta, en amerikansk från 2011 och en europeisk från 2014 [6, 41]. I de amerikanska riktlinjerna från American College of Cardiology Foundation/American Heart Association [41] ges stöd för behandling med intern defibrillator vid uttalad hypertrofi [43], plötslig död hos förstagradssläkting [44] eller svimning utan förklaring, särskilt om den skett det senaste halvåret [45].
Vid utredning med bandspelar-EKG kan icke-ihållande ventrikeltakykardi motivera behandling med intern defibrillator hos yngre patienter, medan ytterligare riskvärdering kan behövas hos äldre [46]. Hos patienter med patologisk blodtrycksreaktion vid fysiologiskt arbetsprov anses också förhöjd risk föreligga [6].
Sedan 2014 finns en ny riskvärderingsmetod som är framtagen för att värdera 5-årsrisken för plötslig arytmidöd vid hypertrofisk kardiomyopati [6]. Metoden utgörs av en algoritm där ålder, icke-ihållande ventrikeltakykardi, maximal kammartjocklek, plötslig död hos förstagradssläkting, oförklarad svimning, vänster förmaksdiameter och grad av utflödesobstruktion från vänster kammare läggs in i en formel som estimerar 5-årsrisk (http://www.doc2do.com/hcm/webHCM.html). Vid 5-årsrisk över 6 procent anses indikation för intern defibrillator föreligga, medan 4–6 procents risk innebär att denna behandling kan övervägas [6].
Vid nedsatt systolisk vänsterkammarfunktion med ejektionsfraktion ≤35 procent bör behandling övervägas i enlighet med sedvanlig riskvärdering vid hjärtsvikt [6].
Vid primärprevention är incidensen av chockterapi av ventrikelarytmi lägre, enligt en nyligen publicerad översiktsartikel 4,8 procent årligen, och komplikationsriskerna bör då särskilt beaktas [47]. Förutom perioperativa komplikationer måste risken för felaktiga chocker minimeras. Oftast beror en sådan onödig chock på förmaksflimmer, skadad elektrod, dubbelräkning av T-våg eller extern störningskälla.
Samlad kompetens behövs för handläggningen
Även om hypertrofisk kardiomyopati är den vanligaste ärftliga hjärtsjukdomen är patientgruppen inte stor på våra mottagningar. Symtomen är ospecifika, och observans krävs för upptäckt. I amerikanska riktlinjer föreslår man bildande av speciella centrum för att optimera omhändertagandet av dessa patienter, men någon motsvarande rekommendation finns inte i europeiska riktlinjer [6, 42].
Rimligen handläggs varje patient med misstänkt eller säkerställd diagnos av kardiolog med intresse för sjukdomen. För en optimal handläggning krävs samarbete med klinisk fysiologi, klinisk genetik, invasiv kardiologi och i förekommande fall med toraxkirurgi. Det kan därför vara värdefullt att utredning och behandling sker i samråd med eller vid sjukhus med sådan samlad kompetens.
Effektiv kausal behandling en framtidsvision
Förbättrat kunskapsläge och tillämpning av genetisk vägledning kan medföra att fler fall av hypertrofisk kardiomyopati upptäcks. Utveckling och användning av läkemedel och invasiva metoder, men också strukturerat omhändertagande, är en ständig process. En vision är att kunna ge effektiv kausal behandling mot bakgrund av ökad kunskap om de molekylärgenetiska uttrycken för sjukdomen.
Potentiella bindningar eller jävsförhållanden: Peter Magnusson har fått föreläsararvode från Abbott, Boehringer Ingelheim och Medtronic; Fredrik Gadler har fått föreläsararvoden från Medtronic och Abbott.