Efter förra årets ovanligt kliniskt inriktade Nobelpris i fysiologi eller medicin prisas i år en riktigt grundvetenskaplig upptäckt.
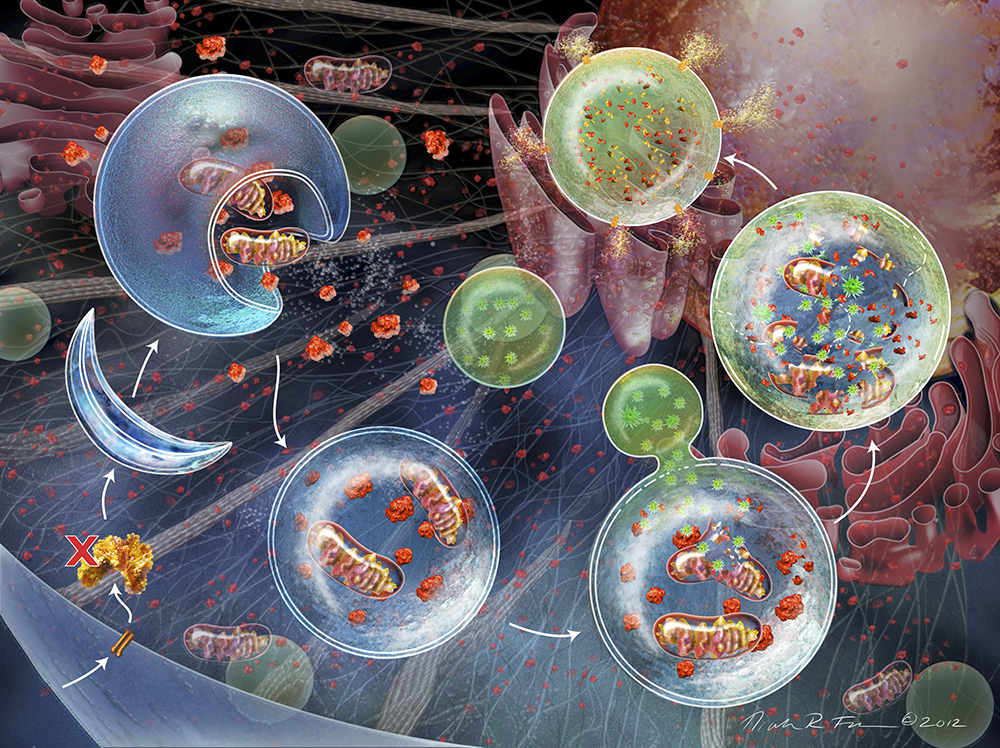
Autofagi är ett begrepp som använts sedan 1960-talet när man i mikroskop såg hur en del av cellens beståndsdelar togs upp av särskilda membranomslutna blåsor, autofagosomer. Dessa sammansmälte i sin tur med lysosomen, som innehåller enzymer som sönderdelar biologiskt material, till exempel skadade proteiner, till tillräckligt små delar för att kunna återvinnas.
Yoshinori Ohsumi, professor vid Tokyo Institute of Technology, får årets medicinpris för att ha klarlagt mekanismerna bakom autofagi.
Yoshinori Ohsumis väg mot Nobelpriset började i tidigt 1990-tal när han lyckades ta fram ett modellsystem som sedan skulle göra det möjligt att studera vilka gener som var inblandade i autofagi. Han ville använda jästceller, som har många fördelar och ofta används för att studera cellprocesser. Ett problem var dock att man då inte ens visste säkert om autofagi förekom i jästceller, eftersom de är små och svårstuderade i mikroskop. Yoshinori Ohsumi löste detta genom att använda muterade jästceller som saknade några av nedbrytningsenzymerna i vakuolen (jästcellens motsvarighet till lysosomen) och odla dessa i ett näringsfattigt medium för att aktivera autofagi. Resultatet blev att autofagosomer ansamlades i vakuolen och därmed blev synliga i mikroskopet. Nu var det alltså klart att jästceller använder autofagi, och ett modellsystem fanns på plats [Takeshige K, et al. J Cell Biol. 1992;119:301-11].
Nästa anhalt för Yoshinori Ohsumi blev att identifiera 15 gener viktiga för autofagi. Dit nådde han bara ett år efter den första iakttagelsen av autofagi i jästcellerna. Metoden var att utsätta samma jästceller med näringsbrist, där autofagosomer ansamlades i vakuolen, för mutationsframkallande kemikalier. Om ansamlingen av autofagosomer i vakuolen uteblev innebar det att en gen med betydelse för autofagi hade inaktiverats [Tsukada M. FEBS Lett. 1993;333:169-74].
Nu var man framme vid att förstå funktionen hos de proteiner som de 15 generna kodade för. Yoshinori Ohsumi och hans medarbetare lyckades de kommande åren beskriva hur dessa proteiner och proteinkomplex, steg för steg, bildar och förlänger autofagosommembranet tills det slutligen försluts till en färdig autofagosom. I samma veva kunde de också visa att det hos människa finns autofagigener som är homologa till dem i jäst [Mizushima N, et al. Nature 1998;395:395-8] samt [Ichimura Y, et al. Nature. 2000;408:488-92].
Yoshinori Ohsumis upptäckter har skapat stort intresse för autofagi, särskilt som det visat sig att mekanismerna för autofagi i våra egna celler är närmast identiska med dem i jästceller. Sedan millennieskiftet är autofagi, enligt Nobelförsamlingen, ett av de mest beforskade områdena inom biomedicin.
Nu vet vi att autofagi är livsviktig vid olika typer av stress, till exempel näringsbrist, när cellen snabbt behöver tillgång till energi eller byggstenar. Men vi vet också att autofagi inte bara är ett svar på stress utan pågår på basal nivå i cellen hela tiden.
Vi har också fått kunskap om att nedsatt autofagifunktion är kopplad till sjukdomar som parkinson och typ 2-diabetes och att autofagi är inblandad när cancer utvecklas. Flera sällsynta diagnoser, ofta autosomalt recessivt nedärvda, beror på försämrad autofagi, till exempel vici-syndromet och SENDA (static encephalopathy of childhood with neurodegeneration in adulthood).
Forskning har vidare visat att en subtyp av autofagi, kallad xenofagi, används för att bryta ned och oskadliggöra bakterier och virus. Och att virus och intercellulära bakterier utvecklat strategier för att kringå detta.
Läs även: »Yoshinori Ohsumis forskning har stor medicinsk betydelse«