En enkätundersökning som Smittskyddsinstitutet nyligen genomfört i samarbete med landets mikrobiologiska laboratorier visar på en markant ökning av antalet diagnostiserade fall av Clostridium difficile-infektion.
Bakterien har inte bara ökat med 60 procent de senaste tio åren. Enligt en gemensam studie, utförd av Smittskyddsinstitutet och Socialstyrelsen, påvisas att antalet dödsfall där Clostridium difficile nämns som huvudorsak eller bidragande dödsorsak i dödsbevisen, också har ökat från 90 till 136 mellan 1997 och 2004.
– Ökningen beror framför allt på ökad antibiotikaanvändning och bristande hygien i vården, säger Torbjörn Norén, överläkare vid infektionskliniken på Universitetssjukhuset i Örebro.
– Som sjukvården ser ut i dag kan vi inte isolera de drabbade patienterna, och vi ger ibland antibiotika i onödan därför att vi tvingas skicka hem patienterna snabbt.
Nästan alla antibiotika har associerats med CDI (Clostridium difficile-infektion), men det gäller framför allt klindamycin, cefalosporiner och kinoloner.
– Vi måste nu verka för en rationell antibiotikaanvändning, där vi undviker bredspektrumantibiotika och där vi måste vara mer restriktiva med att sätta in antibiotika profylaktiskt. På sjukhusen bör man i större utsträckning använda aminoglykosider vid allvarligare buk- och urinvägsinfektioner, säger Torbjörn Norén.
– Det handlar om en mycket utbredd komplikation som innebär stort lidande för patienterna, kostar mycket pengar men som går att förebygga.
Redan 1995 var CDI den vanligaste bakteriella tarminfektionen i Sverige, med 5000 fall, och har sedan ökat till över 8000 fall under 2007, enligt Smittskyddsinstitutets enkätundersökning.
Detta kan jämföras med de vårdrelaterade infektioner som orsakas av meticillinresistenta stafylokocker (MRSA), vankomycinresistenta enterokocker (VRE) och ESBL-bildande bakterier, som sammantaget uppgår till cirka 5000 fall 2008, enligt statistik från Smittskyddsinstitutet.
Är resistens överhuvudtaget en fråga vad gäller CDI?
Både ja och nej, svarar Torbjörn Norén.
– När det gäller behandling av CDI med metronidazol eller vankomycin blir svaret tills vidare nej.
– Resistens har däremot betydelse för deponering av infektiösa sporer i sjukhusmiljön. De flesta studier visar att minst femtio procent av CDI-fallen på sjukhus infekteras av sporer i miljön. Det innebär att om en avdelning frekvent använder breda antibiotika och får många fall av Clostridium difficile-diarré, kombinerat med svårigheter att upprätthålla isolering och handhygien, kommer »tagytor« som textil, sänggrindar, handtag och så vidare att bli nedsmutsade av just de mest resistenta Clostridium difficile-bakterierna.
– Denna selektion i miljön underlättar kolonisering i en antibiotikastörd tarm av just dessa resistenta typer, fortsätter Torbjörn Norén.
– Med tiden är ju risken att vi ändrar den naturliga smittpopulationens resistensförhållanden och detta är ju i analogi med MRSA.
Trenden som nu ses i Sverige är väl känd internationellt och är i många länder kopplad till framför allt vissa stammar av bakterien.
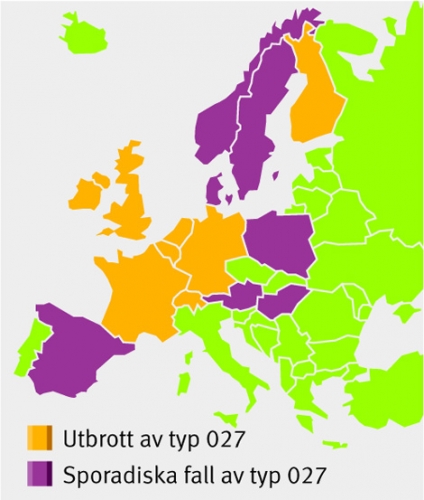
En av stammarna, en hypervirulent typ kallad Clostridium difficile PCR-ribotyp 027, upptäcktes 2003 i Kanada och har nu spritt sig från den nordamerikanska kontinenten ut över världen och till Europa.
Stammen visar en betydligt svårare sjukdomsbild med förhöjd dödlighet, ökad smittsamhet och ökad återfallsfrekvens.
I en rapport från 2008 konstaterar EU-organet ECDC (European Centre for Disease Prevention and Control) att Clostridium difficile typ 027 nu etablerat sig i 16 europeiska länder. Nio av dem har haft epidemier, däribland England, Irland, Frankrike, Holland, Belgien, Tyskland och Finland. Bakterien finns även i Danmark och Norge. I Sverige har det hittills konstaterats ett fall i Uppsala.
Riskgrupperna anses vara äldre och kroniskt sjuka, men i södra Finland, där 49 procent av CDI-proven utgörs av den här stammen, finns ett fall där en 44-årig man utan riskfaktorer dog i en akut förlöpande infektion.
– Det är mycket oroande när en ung människa utan riskfaktorer dör i den här diarrén. Vi vet att den här stammen är mycket virulent och kan leda till kolit och sekundär blodförgiftning när tarmen brister, säger Torbjörn Norén.
Karaktäristiskt för de olika stammar som orsakar CDI är att de var för sig är dominerande på olika orter, vilket är onaturligt och tyder på att det florerar en lokal spridning inom respektive sjukhus.
Det betyder också att man sannolikt har en lokal problematik som går att åtgärda.
Universitetssjukhuset i Örebro ligger långt fram, både vad gäller forskningen och hanteringen av CDI.
– Tre avdelningar här har väldigt hög frekvens och är nu under övervakning. Vi planerar bland annat att införa begränsningar av antibiotikaval och att intensifiera städ- och handhygienåtgärder samt att kunna isolera patienterna på eget rum, säger Torbjörn Norén.
Man har också t ex lokala hygienombud som kallar till riktade workshopar på avdelningarna.
På en konferens om CDI som Smittskyddsinstitutet nyligen anordnade i Örebro tog Olle Aspevall, överläkare inom vårdhygien på Karolinska Universitetssjukhuset, upp vårdhygieniska interventioner.
Han menade att nuvarande vårdhygieniska riktlinjer för infektiös gastroenterit respektive CDI gäller om de kompletteras med kohortvård kring en isolerad patient.
Rum där patienter med CDI vårdas ska desinficeras regelbundet, och efter att en patient med CDI skrivits ut ska slutstädning och desinfektion ske med medel som har sporicid effekt (klorinnehållande medel).
Enligt Torbjörn Norén är tidsfaktorn också enormt viktig. Epidemisk Clostridium difficile, till exempel typ 027, måste snabbt kunna upptäckas så att spridning kan stoppas.
– Vi har en bra och snabb diagnostik, men inte på alla laboratorier. Man upptäcker exempelvis inte 027 om man inte lägger en diskdiffusion mot moxifloxacin på odlingsplattan och sedan typar resi-stenta isolat. PCR-ribotypning görs i dag endast på Smittskyddsinstitutet och på Universitetssjukhuset i Örebro.
Trots den ökande spridningen av allvarliga typer av CDI finns det inte i Sverige någon standardiserad och landsomfattande statistik över inträffade fall.
Våren 2008 kontaktade därför Smittskyddsinstitutet Socialstyrelsen för en diskussion kring frågan om att få Clostridium difficile anmälningspliktig enligt smittskyddslagen.
Förslaget var att laboratoriediagnosen skulle bli anmälningspliktig i analogi med vad som gäller för ESBL.
– Med en anmälningsplikt för laboratorierna får vi en uppfattning, om problemets omfattning och det skapas en basincidens som möjliggör upptäckt av såväl utbrott som förändringar över tiden, säger Karin Tegmark Wisell, medicinskt ansvarig läkare för Clostridium difficile vid bakteriologiska avdelningen på Smittskyddsinstitutet.
– Genom att tidigt upptäcka utbrott eller en långsam ökning av antalet Clostridium difficile-fall får vi möjlighet att föreslå riktade interventioner. Detta är extra aktuellt i dag med vår åldrande befolkning, liksom att flera landsting arbetar med förändrade antibiotikastrategier där effekten på Clostridium difficile måste bevakas. Man bör generellt vara restriktiv med antibiotika, oavsett ålder, men personer över 65 år utgör den huvudsakliga riskgruppen för CDI.
Smittskyddsinstitutet har ännu inte fått något officiellt svar från Socialstyrelsen, men diskussion pågår, enligt Karin Tegmark Wisell.
I väntan på besked från Socialstyrelsen kommer nu Smittskyddsinstitutet – från och med september 2009 – att införa ett frivilligt anmälningssystem för de mikrobiologiska laboratorierna.
Anmälan kommer att ske elektroniskt via SmiNet2, det system som redan används för anmälan enligt smittskyddslagen.
I Uppsala län, där man haft Sveriges enda fall av Clostridium difficile typ 027, har man redan i dag – som enda område i landet – en lokal anmälningsplikt.
Anders Tegnell, enhetschef på Socialstyrelsens smittskyddsenhet, kommenterar att det ännu inte finns tillräckliga data för att göra CDI anmälningspliktig.
– Man måste ha väldigt bra skäl för att vidta en sådan åtgärd, säger han. Anmälningsplikten är ett ganska tungt system som måste leda till direkt nytta i samhället och direkt vara kopplad till åtgärder som ger en nytta för den enskilde patienten. Den är inte en metod som kan användas till att få en uppfattning om problemets omfattning.
– Jag tror inte man löser Clostridium difficile-problemet enbart genom att föra in det i smittskyddslagen, men förfrågan ligger som en del i arbetet med att gå igenom hela anmälningssystemet.