Denna artikel publiceras här i en längre version än den i pappersutgåvan av Läkartidningen 32–33/2009 sidorna 1992-4.
Behandling med simvastatin är den dominerande terapin för kardiovaskulär prevention hos högriskpatienter med ordinära till måttligt förhöjda lipidhalter. Statinbehandling är klart indicerad för sekundär prevention, medan ställningstagande till behandling av patienter för primär prevention bör baseras på en individuell riskskattning [1, 2]. Vår rekommendation för Stockholms läns landsting i Kloka listan [3] är att det stora flertalet högriskpatienter med ordinära till måttligt förhöjda lipidnivåer med fördel kan behandlas med simvastatin [4]. Det finns ett antal stora studier som dokumenterar effekter av behandling med olika statiner i olika doseringar på sjuklighet och död, samt säkerheten med statinbehandling [5-19]. Flertalet av studierna har inkluderats i metaanalyser [20, 21]. Resultaten stämmer väl överens, och vi bedömer att skyddet mot allvarliga hjärt–kärlhändelser huvudsakligen betingas av »klasseffekter«, men vi kan inte utesluta att skillnader i t ex HDL-höjande effekter och så kallade pleiotropa effekter av de olika statinerna kan ha viss betydelse [22]. Vi rekommenderar simvastatin för det stora flertalet patienter, men alternativ behövs ibland på grund av biverkningar eller risker för interaktioner [4]. För patienter med särskilt hög risk och/eller familjära lipidrubbningar kan en intensivare lipidsänkande behandling med högdoserad statin och/eller andra lipidsänkande läkemedel givetvis bli aktuell.
Vår rekommendation av simvastatin i doseringen (20)–40 mg/dag har ifrågasatts [23], och nyligen har Tandvårds- och läkemedelsförmånsverket (TLV) beslutat om subvention av lipidsänkande läkemedel [24]. Dessa händelser föranleder oss att utveckla våra tankar kring preparatval och hur lipidsänkande behandling bör styras. De viktigaste frågorna är hur väl underbyggt det är att behandla patienter till målvärden för LDL-kolesterol, samt i vilken utsträckning man bör beakta kostnadseffektivitet i preparatval och rekommendationer.
Landets samtliga läkemedelskommittéer rekommenderar simvastatin som förstahandsval för lipidsänkande behandling. Vi har utförligt motiverat vår rekommendation av simvastatin och doseringen (20–)40 mg/dag för kardiovaskulär profylax hos högriskindivider med ordinära till måttligt förhöjda lipidvärden [4]. Simvastatin är en utomordentligt väl dokumenterad statin, som dessutom är mycket billig. Ett års behandling med simvastatin 20–40 mg kostar mindre än 200 kr, medan behandling med atorvastatin eller rosuvastatin kostar mer än 3 000 kr i doseringen 10 mg/dag och mer än 6 000 kr i de högsta doseringarna (80 respektive 40 mg/dag). Kostnadsskillnaderna är således avsevärda! Vilken ytterligare patientnytta ger behandling med de dyrare alternativen när det inte finns speciella skäl att ge dessa?
Hur ser statinanvändningen i Sverige ut?
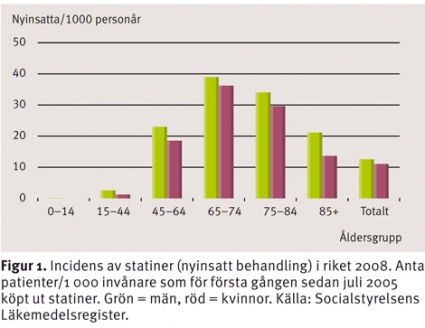
Vi har analyserat utköpen av lipidsänkande läkemedel (ATC-kod C10A) i landet med individbaserade data från Socialstyrelsens läkemedelsregister [25] under 2008. Analyser gjordes per ålder, kön och landsting av prevalens, incidens, val av läkemedel, genomsnittligt uthämtad dygnsdos samt tidigare användning av lipidsänkande läkemedel vid nyinsättning av atorvastatin eller rosuvastatin. Under 2008 hämtade drygt 760 000 svenskar (8 procent av befolkningen) ut recept med lipidsänkande medel, som därmed är de vanligast använda läkemedlen för kroniskt bruk, efter betablockerare och acetylsalicylsyra. Prevalensen var högre bland män än bland kvinnor (9,0 vs 7,6 procent) och högst i åldersgruppen 75–84 år, där var tredje svensk behandlades med dessa läkemedel. Användningen dominerades av statiner (97 procent av alla individer med lipidsänkande medel). Drygt 24 000 personer köpte ut ezetimib, ensamt eller i kombination med statin, vardera drygt 10 000 behandlades med fibrater eller resiner och drygt 300 personer med nikotinsyrapreparat. Totalkostnaden för lipidsänkande läkemedel var 740 miljoner kronor, varav landstingen stod för tre fjärdedelar. Under året fick drygt 110 000 svenskar nyinsatt lipidsänkande behandling, varav 108 000 erhöll en statin. Det motsvarar en incidens på 12,6 respektive 11,1 patienter per 1 000 personår (Figur 1). Nyinsättningarna var relativt sett vanligast i åldersgruppen 67–74 år, men även bland äldre sattes läkemedlen in i stor utsträckning.
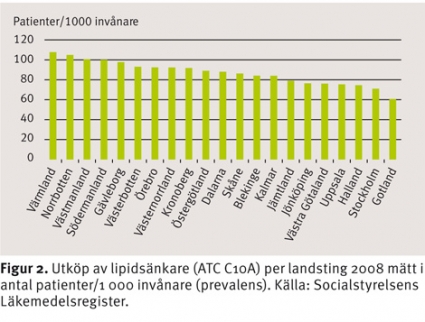
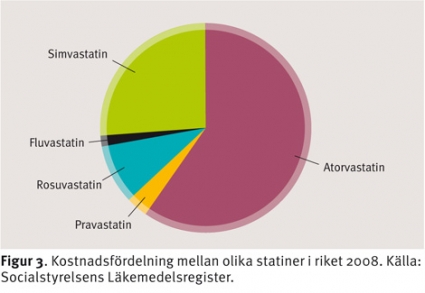
Användningen av lipidsänkande medel varierade avsevärt mellan olika landsting. Under 2008 var den högst i Värmland och lägst på Gotland (108 respektive 61 patienter/1 000 invånare) (Figur 2). Skillnaderna förklaras endast till en liten del av skillnader i åldersstruktur. Det enskilt vanligaste lipidsänkande läkemedlet var simvastatin, som 611 000 svenskar (83 procent av alla statinbehandlade) köpte ut under året. Näst vanligaste statin var atorvastatin med drygt 100 000 (14 procent), medan 23 000 behandlades med pravastatin och 20 000 med rosuvastatin. Den stora prisskillnaden medförde att atorvastatin betingade 60 procent och simvastatin endast 26 procent av den totala kostnaden för statiner (Figur 3). Andelen simvastatinbehandlade var lägst i Stockholm, Dalarna och Norrbotten (79 procent) och högst på Gotland (91 procent).
Under 2008 nyinsattes i genomsnitt 10 000 personer varje månad på simvastatin, 1 600 på atorvastatin, 770 på rosuvastatin, 190 på pravastatin och ett 30-tal på fluvastatin. Nästan en tredjedel (29 procent) av dem som nyinsattes på atorvastatin, och 44 procent av dem som fick rosuvastatin, hade inte behandlats med simvastatin under de närmast föregående 18 månaderna.
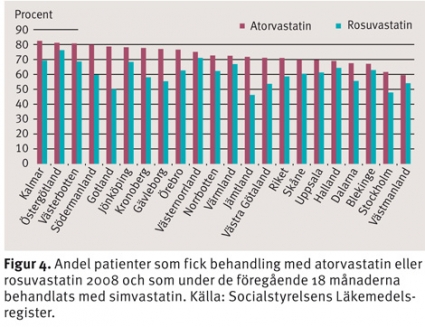
Praxis vid nyinsättningar varierade mellan landstingen (Figur 4). I Kalmar hade mer än 80 procent av patienterna provat simvastatin innan atorvastatin. Motsvarande siffra var inte mer än cirka 60 procent i Västernorrland och Stockholm. De som fick nyinsatt behandling med rosuvastatin hade i lägre grad tidigare behandlats med simvastatin i samtliga landsting (Figur 4). Under 2008 var 20 mg den vanligaste dosen (40 procent) för simvastatin, följt av 10 mg (35 procent); färre än 1 procent av patienterna fick 80 mg simvastatin. För atorvastatin var 10 mg den vanligaste doseringen (55 procent) följt av 20 mg (24 procent); endast 3 procent fick 80 mg. För rosuvastatin var 10 mg vanligast (41 procent), följt av 5 mg (39 procent) och 20 mg (15 procent); endast 2 procent hade 40 mg som genomsnittlig dos under 2008. Atorvastatin och rosuvastatin i hög dos utnyttjas mycket litet, men den bäst dokumenterade doseringen av simvastatin (40 mg/dag) förefaller underutnyttjas.
Ska vi behandla till ett »kolesterolmål« eller med en terapi som är dokumenterad i studier?
Nationella och internationella riktlinjer anger att olika patientkategorier ska behandlas till olika kolesterolhalter i blodet [1, 2, 26-29]. Fokus är främst på LDL-kolesterol, och målvärdena har successivt krupit nedåt [30]. Vilka principiella och praktiska problem medför detta?
Statinernas dos–responseffekt för LDL-sänkning är sådan att man får relativt små ytterligare sänkningar när doseringarna höjs från ordinära till de högsta rekommenderade. I den jämförande STELLAR-studien [31] sänktes LDL-kolesterol med i genomsnitt 35, 39 och 46 procent med simvastatin i doseringarna 20, 40 och 80 mg/dag. Motsvarande sänkningar var 37, 43, 48 och 51 procent med atorvastatin 10, 20, 40 och 80 mg/dag, och 46, 52 och 55 procent med rosuvastatin 10, 20 och 40 mg/dag. Skillnaderna i LDL-sänkning mellan simvastatin 40–80 mg/dag och maximala doseringar av alternativen är således måttlig. Vilken ytterligare patientnytta ger ytterligare sänkning av LDL-kolesterol med 5–10 procentenheter (från ca 40–45 procent till 50–55 procent)? Kan man bortse från att biverkningarna ökar vid hög dosering?
Metaanalyser av statinstudierna har funnit att en lägre LDL-nivå är associerad med en lägre risk att drabbas av en allvarlig hjärt–kärlhändelse [20, 21]. Cholesterol Treatment Trialists’ Collaborators (CTT) har beräknat att 1 mmol/l sänkning av LDL-kolesterol leder till drygt 20 procents relativ minskning av risken [20]. Den figur som illustrerar sambandet (Figur 3 i [20]) visar emellertid en tämligen dålig anpassning av studiernas resultat till regressionslinjen. Studiernas duration har varierat och regressionslinjen har dessutom »tvingats« gå genom origo. Ingen studie har testat teorin om dos–respons för LDL-sänkning avseende hjärt–kärlrisk med statiner eller med annan behandling. I den största statinstudien, Heart Protection Study (HPS), var den relativa riskminskningen oberoende av initial LDL-kolesterolnivå och av storleken på LDL-sänkningen med simvastatin 40 mg/dag hos enskilda patienter (<38 procent, 38–47 procent, eller mer än 47 procent) [10]. Evidensen för behandling till ett visst kolesterolmål är indirekt och bygger på analogiresonemang som ännu inte testats vetenskapligt [4, 30].Rekommenderade målvärden för LDL-kolesterol är t ex ≤2,0 mmol/l vid prevention hos högriskpatienter [27] eller ≤1,8 mmol/l för diabetespatienter med kranskärlssjukdom [28] eller patienter med akuta koronara syndrom [29]. Av intresse i sammanhanget är att färre än hälften av patienterna i IDEAL- och TNT-studierna nådde LDL-halter ≤2,0 mmol/l med atorvastatin 80 mg/dag [16, 17]. Hur ska alla de patienter som inte når målen med 80 mg atorvastatin eller 40 mg rosuvastatin behandlas? Vad vet vi om effekter och biverkningar av sådan (kombinations)-behandling? Vad får det kosta?En studie som testar hypotesen att behandling till ett visst målkolesterolvärde är det bästa för patienten är angelägen. Den borde dokumentera om lipidsänkande behandling till ett visst kolesterolmål (helst med en tydlig, förspecificerad behandlingsalgoritm) medför större patientnytta än ordinär behandling med förslagsvis simvastatin. Utan en sådan studie är – enligt vår mening – beslutsunderlaget för målstyrd behandling alltför bräckligt. Däremot kan man på basen av tillgänglig dokumentation rekommendera statinbehandling i hög dosering till vissa patientkategorier i situationer där ordinär simvastatinbehandling inte anses räcka.En viktig aspekt som vi saknar svenska data på är i vilken utsträckning patienterna kvarstår på behandling (persistens) under lång tid, med tanke på att den i allmänhet avses vara livslång. I en översikt av studier fann man en genomsnittlig persistens av endast 66 procent, och att 51 procent av patienterna hade en »medication possession ratio« (ett mått på behandlingsföljsamhet) ≥80 procent efter 12 månaders behandling med lipidsänkande läkemedel [32]. Motivationen hos patienten och tolerabiliteten torde ha stor betydelse för patientens vilja att fortsätta med behandlingen. Dosberoende biverkningar kan vara viktiga för följsamheten och behandlingsresultaten.Riskreduktion i förhållande till kostnader med olika lipidsänkande alternativ I en utvidgad analys inspirerad av Hayward och medarbetare [30] kunde vi bekräfta att den ytterligare patientnytta som erhålls med statinbehandling jämfört med placebo eller med intensiv jämfört med ordinär statinbehandling avtar ju lägre kontrollgruppens risknivå och LDL-kolesterolhalter är [4]. Primärpreventiva studier kan visa goda effekter i relativa termer, medan den absoluta behandlingsvinsten är sådan att man inte kan rekommendera primärpreventiv behandling utan en individuell riskskattning som identifierar individer med hög risk [1, 2]. JUPITER-studien [19] är ett bra exempel på detta [4]. För patienter med hög hjärt–kärlrisk är statinbehandling indicerad, och då måste analysen av alternativa behandlingar baseras på patienternas risk (och LDL-kolesterol) med ordinär statinbehandling, inte på patienternas obehandlade risknivå (eller kolesterolhalter). I det perspektivet kan nyttan med intensifierad statinbehandling vara begränsad även om patienten har en hög hjärt–kärlrisk [4].Utan avancerad hälsoekonomisk metodik kan man lätt konstatera att högdosbehandling med atorvastatin kan generera stora kostnader jämfört med ordinär behandling med simvastatin trots liten ytterligare effekt [4]. I IDEAL-studien resulterade 4,8 års behandling med atorvastatin 80 mg/dag jämfört med simvastatin i medeldoseringen 24 mg/dag i en icke signifikant (P=0,07) absolut minskning av risken för en primär kombinerad hjärt–kärlhändelse med 1,1 procent [16]. Läkemedelskostnaden för att förhindra en primär hjärt–kärlhändelse med högdos atorvastatin i stället för ordinär dos simvastatin är drygt 2,5 Mkr (5 900 kr x 4,8 år x 91 patienter) i IDEAL-studien. Hur mycket mer hade det kostat om man hade jämfört med simvastatin 40 mg/dag (eller 80 mg/dag), som kunde ha gett ytterligare effekt i den gruppen?
I studier har dessutom fler än dubbelt så många avbrutit behandling med atorvastatin 80 mg/dag jämfört med simvastatin 24 mg/dag [16], atorvastatin 10 mg/dag [17] eller simvastatin 80 mg/dag [33]. Högdosbehandling bör förbehållas patienter med den högsta kardiovaskulära risken.Vad anser Socialstyrelsen om statinbehandling?
Socialstyrelsen har fått en anmälan mot våra rekommendationer och har yttrat att statinbehandling bör individualiseras [23]. Man hänvisar till den Nationella riktlinjegruppen för hjärtsjukdomar som anför att »En sänkning av LDL-kolesterolet till 2,5 mmol/l ger en signifikant reduktion av kranskärlshändelser (gott vetenskapligt underlag). En sänkning till 1,6 mmol/l kan ge ytterligare effekt (visst vetenskapligt underlag).« I beslutsstödsraden A137 ges »blodfettssänkning med adekvat behandling« hög prioritet för patienter med aterosklerotisk kärlsjukdom och kolesterol > 4,5 alternativt LDL-kolesterol > 2,5 mmol/l som inte nått målnivå med förstahandsbehandlingen (generisk statin). Man öppnar således för en intensiv LDL-sänkande behandling till målnivåer ner mot 1,6 mmol/l, vilket måste innebära en ökad användning av lipidsänkande terapier (med tillägg av t ex ezetimib?) som saknar dokumentation avseende hjärt–kärlhändelser. Kolesterolmålen bygger på subgruppsanalyser och analogiresonemang, inte på studier som testar effekter av måluppfyllelse. Kan vi, i avsaknad av dokumentation av en eller flera strategier för att nå kolesterolmålen, lita på att effekterna och säkerheten blir så goda som man hoppas? Kostnadseffektiviteten av rekommendationen i beslutsstödet A137 anges vara »ej bedömbar«.
Vad anser Tandvårds- och läkemedelsförmånsverket (TLV)?
TLV:s utredning om lipidsänkande läkemedel har ett fylligt bakgrundsdokument [24]. TLV har ambitionen att främja en kostnadseffektiv statinanvändning och förordar – i likhet med läkemedelskommittéerna – i första hand behandling med simvastatin, som ju är mycket billigt och väldokumenterat. Man fäster dock stor vikt vid små skillnader i de olika statinernas relativa förmåga att sänka LDL-kolesterol i olika doseringar. Några exempel i TLV:s hantering av problematiken som kan diskuteras är:
1. TLV tar bort subventionen för atorvastatin 10 mg och rosuvastatin 5 mg, med motiveringen att deras effekt inte skiljer sig från simvastatins, men subventionerar tämligen låga doser av medlen (20 respektive 10 mg) baserat på resonemang kring procentuell LDL-sänkning (Tabell 2, Figur 9 i [24]). Simvastatin sänker enligt TLV:s utredning LDL-kolesterol med 37 procent i doseringen 40 mg/dag och 42 procent i doseringen 80 mg/dag.
Atorvastatin 20 mg/dag och rosuvastatin 10 mg/dag sänker båda LDL-kolesterol med 43 procent. Skillnaderna i LDL-sänkning som motiverar en 15 gånger högre kostnad är således endast 6 procentenheter jämfört med simvastatin 40 mg, och 1 procentenhet jämfört med 80 mg simvastatin. Vad kan dessa små skillnader i LDL-sänkning ge för ytterligare patientnytta? Vad blir de hälsoekonomiska konsekvenserna?
Små skillnader i LDL-sänkning med olika statiner och doseringar ska också ses mot bakgrunden av hur exakt bestämningen av LDL-kolesterol är. LDL är en beräknad variabel (Friedewalds formel), och resultaten påverkas av både preanalytisk (fysiologisk) och analytisk variabilitet. NICE (National Institute for Health and Clinical Excellence) har noterat att mätfelen är i storleksordningen 15 procent och därmed större än skillnaderna i LDL-sänkning med olika statindoseringar som diskuteras ovan [34]. Hur blir »träffsäkerheten« för den individuelle patienten?
2. TLV:s hälsoekonomiska värdering av den ytterligare nyttan av behandling med högdos atorvastatin (80 mg/dag) jämfört med simvastatin är inte grundlig. En hälsoekonomisk subgruppsanalys i IDEAL-studien accepteras (med vissa reservationer), men man gör inga egna beräkningar utifrån primära effektresultat i publicerade studier. Våra enkla beräkningar ovan visar att kostnaden kan bli mycket hög. Hur hög risk ska patienterna ha för att en intensiv statinbehandling ska bli kostnadseffektiv i jämförelse med simvastatin (20)–40 mg/dag?
3. Simvastatin i doseringen 80 mg/dag anses av TLV inte vara något alternativ att allvarligt överväga på grund av biverkningsproblem. Den doseringen rekommenderas emellertid av NICE när ytterligare effekt av behandlingen eftersträvas [34]. Den enda direkt jämförande kliniska prövning som vi har funnit och som ger en god bild av effekter och biverkningar visade något lägre LDL-kolesterol, men också lägre HDL-kolesterol och dubbelt så många behandlingsavbrott på grund av biverkningar med 80 mg atorvastatin jämfört med 80 mg simvastatin (6,0 vs 2,6 procent) [33]. Är simvastatin 80 mg/dag ett dåligt alternativ?
Hur ska vi förhålla oss till rådande situation?
LDL-kolesterolmål för att styra behandlingen har blivit (nästan) allmänt accepterade, men det finns kritiker av detta paradigm [29, 34, 35]. Vad vet vi om patientnytta och patientsäkerhet med de höga statindoseringar och tilläggsbehandlingar som krävs för att nå LDL < 2,0 (eller 1,6) mmol/l? Det finns ingen studie som testar behandling till dessa mål, men vi vet att biverkningarna kommer att bli fler och att kostnaden blir mycket högre! Socialstyrelsen borde fästa större vikt vid kostnadseffektivitet i sina prioriteringsunderlag för sjukvården. Vi ifrågasätter hälsoekonomiska analyser som baseras på antaganden om patientnytta med olika LDL-mål i ett behandlingsområde som har många stora och välgjorda studier av verkliga händelser med olika statinbehandlingar. Vi är förvånade över TLV:s enkla gränsdragning för subvention av icke-generiska statiner – över eller under 38 procent relativ sänkning av LDL-kolesterol – och hur man hanterat simvastatin i doseringen 80 mg/dag.Vissa patienter har behov av annan statinbehandling i ordinära doseringar på grund av biverkningar eller interaktioner [4], och TLV skulle ha kunnat besluta om förbehållet att simvastatin ska prövas innan dyrare statin används (med subvention) oavsett dosering. Vår åsikt är att behandling med atorvastatin eller rosuvastatin i hög dosering inte bör bli utbredd av ovan angivna skäl. Vi vill framför allt inte få en utbredd användning av icke dokumenterade (kombinations)terapier för att nå allt lägre kolesterolmål på de lösa grunder som vi anser föreligger. Beträffande preparatval och dosering skrev Läkemedelsverket i sin behandlingsrekommendation för lipidreglerande läkemedel: »Faktorer som dokumenterad dos och dokumenterad effekt vid olika tillstånd, tolerans samt pris bör styra läkemedelsvalet hos den enskilde patienten« [1]. Det stora flertalet patienter med hög kardiovaskulär risk och ordinära till måttligt förhöjda lipidnivåer erhåller en god och mycket kostnadseffektiv profylax med simvastatin, och det kan enligt vår mening inte vara fel att eftersträva den bäst dokumenterade doseringen av medlet, 40 mg/dygn, om patienten tolererar denna.För patienter med familjära lipidrubbningar är kunskapsläget mycket sämre, och ställningstagande till högdosbehandling med statin och/eller andra lipidsänkande läkemedel får baseras på patofysiologiska resonemang och ett begränsat underlag av observationsstudier. Vi har även publicerat ett dokument om denna problematik på http://www.janusinfo.se [36].Slutligen har vi anmodat Statens beredning för medicinsk utvärdering (SBU) att utreda frågan om evidensbaserad och kostnadseffektiv kardiovaskulär prevention med lipidsänkande behandling. Vi anser att man behöver skärskåda vad som faktiskt är evidensbaserat, samt även ta ett bredare grepp på hälsoekonomin kring lipidsänkande behandling för kardiovaskulär prevention.• Potentiella bindningar eller jävsförhållanden: Inga uppgivna.