Sammanfattat
Panton–Valentine-leukocidin (PVL) är ett exotoxin som produceras av vissa stammar av Staphylococcus aureus. PVL-positiva Staph aureus-orsakade nekrotiserande pneumonier beskrivs i ökande omfattning. Dessa kan vara primära eller sekundära till en annan djup Staph aureus-infektion (exempelvis osteomyelit, artrit eller djup mjukdelsinfektion).
Nekrotiserande pneumoni/abscess, empyem eller dåligt terapisvar på antibiotika ger misstanke. Hemoptys, lunginsufficiens och septikemi är typiska symtom i svåra fall. Leukopeni är vanligt i det akuta skedet.
Diagnostik med PCR bör definitivt utföras vid alla Staph aureus-pneumonier och kan övervägas även vid andra invasiva Staph aureus-infektioner, i synnerhet med MRSA.
Kirurgiskt dränage är viktigt. Antibiotika med inhibitoriska effekter på bakteriernas toxinsyntes (tex klindamycin eller linezolid) bör övervägas tidigt i förloppet. I svåra fall kan även intravenöst immunglobulin övervägas.
De vanligaste orsakerna till samhällsförvärvad pneumoni hos i övrigt friska barn är olika luftvägsvirus, Mycoplasma pneumoniae och Streptococcus pneumoniae. Haemophilus influenzae har minskat i betydelse sedan allmän vaccination infördes. Pneumoni orsakad av Staphylococcus aureus (Staph aureus) är mera ovanlig och har beskrivits ha en incidenstopp före ett års ålder [1]. Gillet och medarbetare beskrev 2002 sexton fall av nekrotiserande pneumoni orsakade av Panton–Valentine-leukocidin(PVL)-producerande Staph aureus [2]. Medianåldern var 14,8 år och alla var tidigare friska. Kliniska särdrag var ett influensaliknande insjuknande, hemoptys, leukopeni och hastigt progredierande andningsinsufficiens. Histopatologiska studier visade utbredda ulcerationer, nekroser och blödningar i slemhinnan från larynx och distalt, stora mängder grampositiva kocker, men anmärkningsvärt lite inflammatoriska infiltrat av granulocyter. PVL är en sedan länge känd virulensfaktor vid Staph aureus-orsakade hud- och mjukdelsinfektioner och sågs nu även associerat med nekrotiserande pneumonier. Det fagburna PVL-toxinet binder till och avdödar neutrofila granulocyter och monocyter genom att bilda en por i cytoplasmamembranet, vilket kan leda till leukopeni [3, 4]. Den exakta patogenesen bakom Staph aureus-pneumoni är fortfarande oklar, men andra arbeten har bekräftat en höggradig association med PVL [5, 6].
I epidemiologiska studier har man funnit att 5 procent av alla Staph aureus-isolat i öppenvården är PVL-positiva [7]. Dock finns en koppling mellan PVL och meticillinresistens bland Staph aureus-isolat av en ny typ, som fått en kraftig spridning framförallt i USA, men även i Europa [8, 9]. Den vanligaste infektionstypen är dock hud- och mjukdelsinfektion.
Medvetenheten om denna svåra infektion är säkert hög i infektionsläkar- och mikrobiologkretsar, men få rapporter har publicerats från Sverige, och inom andra specialiteter är detta troligen en relativt okänd infektionssjukdom [10, 11]. På barnkliniken i Halmstad har vi under en 6-månadersperiod upplevt tre svåra fall av PVL-positiva Staph aureus-pneumonier hos tidigare friska unga. Inget epidemiologiskt samband har funnits mellan de tre fallen. Syftet med detta arbete är att beskriva den kliniska bilden vid PVL-positiv Staph aureus-pneumoni för att göra fler kliniker uppmärksamma på denna aggressiva och snabbt förlöpande sjukdom.
Fall 1
Under oktober 2005 insjuknade en tidigare frisk 12-åring med ca 40°C feber, torrhosta, hälta och lokal värk mitt i höger lår. Han sökte barnakuten dag 3 i sjukdomsförloppet, och i ankomststatus noterades en lokal palpationsömhet på lårets framsida. C-reaktivt protein, CRP, var 166 mg/l (normalt 5). Ultraljud påvisade en utgjutning i höger höftled, och punktion gav utbyte av 4 ml grumlig ledvätska. Behandling med cefuroxim inleddes. Dag 4 utfördes en artrotomi med renspolning på grund av ökade lokala besvär. Odling från ledvätska och blod visade växt av fullt antibiotikakänsliga Staph aureus, och behandlingen ändrades till kloxacillin dag 5. Patienten var då leukopen med LPK 3,5 x 109/l (5,0–13,0). Dag 7 uppfattades en klar försämring med tillkomst av takypné, hypoxemi och torakala smärtor. Lungröntgen och datortomografi visade utbredda parenkyminfiltrat bilateralt samt pleuravätska. Antibiotikabehandlingen kompletterades med gentamicin. Överflyttning till Barn- och ungdomssjukhuset vid Universitetssjukhuset i Lund skedde för dränering av empyem och fortsatt vård därefter. Odlingar från blod och pleura visade fortfarande växt av Staph aureus trots fyra dygns antibiotikabehandling och polymeraskedjereaktion, PCR, för PVL utföll positivt. Det fortsatta förloppet komplicerades av en djup ventrombos (DVT) i höger vena femoralis, och antikoagulantiabehandling påbörjades. Transesofageal ekokardiografi visade ingen endokardit. På grund av persisterande feber försöktes behandling med rifampicin, som dock fick seponeras på grund av allergisk reaktion. Klindamycin gavs kontinuerligt, med viss förbättring, men feberfrihet uppnåddes inte förrän behandlingen kombinerades med linezolid från och med dag 23. Kirurgiskt dränage av höften utfördes också. Tillståndet stabiliserades, men med röntgen och MR ca 8 veckor efter insjuknandet kunde man påvisa utveckling av kronisk osteomyelit, och pojken har därför fortsatt med mycket långvarig kombinationsbehandling med klindamycin och linezolid. Bred immunologisk utredning och koagulationsutredning har inte givit hållpunkter för någon bakomliggande defekt. Sex veckor efter insjuknandet hade pojken en restriktiv lungfunktionsnedsätttning med vitalkapacitet kring 40 procent av det åldersförväntade, men vid uppföljning sex månader efter insjuknandet hade lungfunktionen förbättrats till ≈ 70 procent av förväntat värde.
Sammanfattningsvis bedömer vi detta som en PVL-positiv Staph aureus-sepsis med hematogen osteomyelit i femur och genombrott till höftleden. Sekundärt uppkom utbredda, bilaterala pneumonier. En djup ventrombos komplicerade också förloppet, och det är möjligt att lunginfektionerna utgjordes av rena septiska embolier.
Fall 2
Under februari 2006 insjuknade en tidigare frisk, knappt 15-årig flicka med hosta, halssmärtor och feber. Dag 3 i sjukdomsförloppet sökte hon vård på grund av ett urtikariellt exantem. Symtomen bedömdes vara virusorsakade, och CRP var 9 mg/l, LPK 7,8 x 109/l. Exantemet bedömdes som en reaktion på NSAID, och hon behandlades med adrenalin och steroider. Före hemgång undersöktes patienten även av ÖNH-specialist, och man såg svullna, såriga slemhinnor i larynxingången.
Hon sökte på nytt dag 5, fortfarande med hög feber, halssmärta, ont i kroppen och hemoptys. Man fann dämpning och sänkta andningsljud över höger lungfält samt lätt leverförstoring. Hon hade en snabb, ytlig andning och SaO2 89 procent. Lungröntgen visade då utbredda infiltrat i högerlungan, och patienten hade en uttalad leukopeni med LPK på 1,2 x 109/l. Åtta timmar efter ankomst var LPK 0,8 x 109/l. varav neutrofila granulocyter 0, och CRP var 380 mg/l.
Efter odlingar från svalg, nasofarynx, urin, blod och feces medicinerades flickan med meropenem men försämrades snabbt. Syra–basstatus i blodet visade normalt pH, adekvat ventilation, hypoxemi samt P-laktat på 7. Hon hade kraftig samtalsdyspné, och nio timmar efter ankomst påbörjades respiratorvård.
Flickan var cirkulatoriskt instabil och krävde inotropt stöd. Efter en intravenös vätskebolus läckte blodtillblandad vätska ur trakealtuben. Förnyad lungröntgen efter cirka 8 timmar visade tydlig progress av lungförändringarna med atelektasbildning. Patienten utvecklade en uttalad disseminerad intravasal koagulation. Behandlingen utökades dag 6 med gentamicin, levofloxacin och initialt även erytromycin. Hon fick även filgrastim (G-CSF) och drotrecogin alfa (Xigris; rekombinant humant aktiverat protein C, koagulationshämmare). Dag 7 gjordes ett behandlingsförsök med intravenöst immunglobulin (IVIG). Ordinationen var 1 g/kg, men infusionen avbröts hastigt på grund av blodtrycksfall. På grund av ytterligare försämrad syresättning påbörjades behandling med extrakorporeal membranoxygenering (ECMO), och flickan överfördes till Stockholm. Vid bronkoskopi fann man en nekrotisk bronkialslemhinna och rikligt med brunaktigt sekret ur lungorna.
Initiala odlingar och serologier var negativa, förutom växt av Staph aureus i nasofarynx (fullt känslig för antibiotika), och grupp C-streptokocker i svalg. Den funna Staph aureus-stammen var PVL-positiv. Behandling med linezolid startades dag 8. Staph aureus växte även i blod dag 9. Linezolid byttes dag 10 mot klindamycin, som senare byttes mot rifampicin, och den totala behandlingstiden blev cirka sju veckor. Staph aureus växte i lungsköljvätska dag 17, trots 9 dagars adekvat behandling. Dag 18 och 19 upprepades IVIG (1 g/kg och dag).
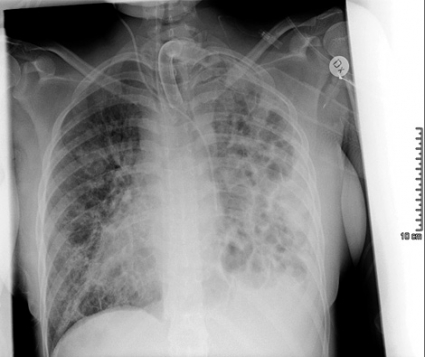
Upprepade lungröntgen- och DT-toraxundersökningar visar att höger lunga är svårt destruerad, och det finns även omfattande parenkymförändringar på vänster sida (Figur 1 och 2). Hon eftervårdades i Halmstad och förbättras långsamt. Vid utskrivning efter 3,5 månader klarade hon att gå några hundra meter men har en kvarstående lungskada med stora emfysemblåsor i höger lunga och kombinerad restriktiv och obstruktiv lungfunktionsinskränkning.
Detta fall av PVL-positiv Staph aureus-sepsis bedöms således som en primär pneumoni, med ett aggressivt och snabbt progredierande förlopp. Behandlingen omfattade förutom antibiotika även IVIG och filgrastim, men ECMO var en förutsättning för att patientens liv kunde räddas.
Fall 3
En nyfödd flicka inkom, efter okomplicerad graviditet och förlossning, i april 2006 till akuten vid 15 dagars ålder med 3–4 dagars anamnes på lätt hosta. Natten före ankomsten hade hon haft stötig andning och inte velat äta. I status fann man att flickan var något blek, lätt muskelhypoton, hade en något insjunken fontanell och stötig andning. Temperaturen var 37,6°C. Lungröntgen var vid ankomsten helt normal, och infektionsprov visade IL-8 80 ng/l (ref 70), samt CRP 36 mg/l. Cefuroximbehandling startades efter odlingar. Natten efter ankomsten försämrades tillståndet betydligt med dålig perifer cirkulation och lågt blodtryck. Tilltagande ytlig andning, ökande syrgasbehov och koldioxidretention föranledde respiratorbehandling. Antibiotikabehandlingen kompletterades med gentamicin. Meningit kunde uteslutas efter lumbalpunktion. Ny lungröntgen efter 20 timmar visade nytillkomna förtätningar apikalt och basalt i vänster lunga samt lätt nedsatt lufthalt apikalt i höger lunga. Patienten utvecklade dag 2 neutropeni med neutrofila granulocyter på 0,2 109/l och fick filgrastim dag 2 till dag 4. Flickans tillstånd stabiliserades. Dag 3 sågs klinisk förbättring, men på grund av fortsatt stigande CRP utbyttes cefuroxim mot meropenem. Lungröntgenbilden försämrades ytterligare. Blod- och svalgodling visade växt av Staph aureus resistenta mot klindamycin och fucidinsyra. Med tanke på det allvarliga sjukdomsförloppet och patientens låga ålder gavs IVIG (2,6 g/kg fördelat på fem dagar). En ultraljudsundersökning av den vänstra lungan dag 5 visade en helt konsoliderad lunga med misstanke om abscessbildning. Samtidigt började pusliknande sekret tömmas via trakealtuben. Samma dag meddelade laboratoriet att stafylokockerna var PVL-positiva, varefter linezolid insattes. Flickan förbättrades kliniskt, men först dag 11 syntes bättre lufthalt i vänster lunga. Hon extuberades dag 12, och från dag 20 kunde hon försörja sig via flaskmatning. Dag 23 hade lunginfiltraten minskat betydligt, och 6 veckor efter insjuknandet är lufthalten helt normal, men en lätt volymsminskning kan ses som ett resttillstånd i vänster lunga. Flickan var vid efterkontroll vid ca 8 veckors ålder välmående och utvecklades normalt.
Sammanfattningsvis är detta ett fall av sannolikt primär PVL-positiv Staph aureus-pneumoni hos ett spädbarn, med mycket snabbt progredierande andningsinsufficiens och leukopeni. Tillståndet var mycket allvarligt under några dygn, men förbättrades betydligt snabbare än för de två andra patienterna. Även i detta fall användes förutom antibiotika, filgrastim och IVIG i behandlingen.
Diskussion
Vi vill fästa uppmärksamheten på PVL-positiva Staph aureus som orsak till samhällsförvärvade, svåra pneumonier hos unga individer. I USA och Europa har man sett en kraftig ökning av PVL-positiva meticillinresistenta Staph aureus (MRSA), som orsak till samhällsförvärvade hud- och mjukdelsinfektioner, pneumonier eller led- och skelettinfektioner [8, 12, 13]. Våra fall gällde meticillinkänsliga Staph aureus, men PVL-positiva MRSA har rapporterats också från Sverige [11]. Inga uppenbara epidemiologiska samband kunde påvisas mellan de tre fallen. Att det var frågan om tre oberoende fall bekräftas av att de tre Staph aureus-isolaten vid spa-typning visade sig tillhöra de tre distinkt olika spa-typerna t186, t1211 respektive t044 [14].
I Gillets material av PVL-positiva nekrotiserande Staph aureus-pneumonier var mortaliteten så hög som 75 procent, men det var selekterat och delvis retrospektivt [2]. Det har senare visats att många pneumonier orsakade av PVL-positiva Staph aureus inte är letala [5]. Föregående influensa A har utpekats som en klar riskfaktor för svår, nekrotiserande pneumoni [5, 13]. Den kliniska bilden kan vara primär pneumoni (som i Fall 2 och 3), eller sekundära, metastatiska pneumonier (som i Fall 1).
Hemoptys är vanligare vid PVL-positiva pneumonier [2]. Detta fann vi indirekt i Fall 2 och 3 genom det blodtillblandade sekret som kom ur trakealtuben, tydande på djupa skador i slemhinnorna. Sårbildningar kunde också anas vid inspektion av larynxingången hos patienten i Fall 2.
Blododlingar och odlingar från infekterade vävnader var positiva i alla tre fallen, även efter flera dagars behandling med antibiotika, och patienterna var septiskt påverkade. En bidragande orsak till denna tröga antibiotikaeffekt kan vara den uttalade leukopeni som uppkommer vid infektion med PVL-positiva Staph aureus. Patienterna i Fall 2 och 3 behandlades med G-CSF för att motverka granulocytopenin, men det skall påpekas att vi inte är medvetna om någon klinisk studie som undersökt effekten av G-CSF vid just denna infektionstyp.
I Fall 1 uppkom en djup ventrombos (DVT) i v femoralis, och detta fall liknade den tidigare beskrivna triaden av osteomyelit, djup ventrombos och septiska lungembolier, som är associerad med PVL-positiva Staph aureus-infektioner [15, 16]. Vid metastatiska pneumonier är det angeläget att undersöka om djup ventrombos föreligger.
Frågan om »rätt antibiotikaval« är öppen. Den traditionella antibiotikabehandlingen av Staph aureus-pneumoni är betalaktamasstabila medel ur betalaktamgruppen. MRSA-problematiken har medfört att vankomycin blivit ett förstahandsalternativ i drabbade områden. En invändning mot vankomycin är att vävnadskoncentrationerna blir låga i lungan [17]. Linezolid är ett nytt alternativ vid komplicerade Staph aureus-infektioner, som ger höga intrapulmonella koncentrationer [18]. Det har också visat sig i randomiserade studier att linezolid är överlägset vankomycin vid nosokomiala MRSA-pneumonier [19]. Staph aureus kan producera flera virulensfaktorer, och därför kan den kliniska effekten av antibiotikabehandling förstärkas av att exotoxinfrisättning inhiberas med antibiotika som hämmar proteinsyntesen (tex klindamycin, linezolid) [20, 21]. Enstaka fallbeskrivningar har indikerat detta [6, 22]. Klindamycin är ett beprövat medel vid svåra mjukdelsinfektioner med toxinproduktion, men viss oro för resistensutveckling, vilket även förelåg i Fall 3, kan tala till linezolids fördel. Till linezolids nackdel måste nämnas risken för allvarlig biverkning (benmärgsdepression och sensorisk neuropati) och den höga kostnaden.
Svår nekrotiserande pneumoni orsakad av PVL-positiva Staph aureus har beskrivits främst bland unga, och den primära formen är vanligast hos barn 5 år [5]. En orsak kan vara att neutraliserande antikroppar mot PVL saknas hos små barn. Antikroppar mot PVL utvecklas sannolikt genom upprepade subkliniska exponeringar för toxinet, i analogi med vad som visats för toxic shock staphylococcal toxin [23]. Kommersiellt IVIG har höga nivåer av anti-PVL-immunglobulin G, och majoriteten av vuxna har höga antikroppsnivåer [4]. PVL-antikroppar kan neutralisera toxinets cytopatiska effekt på granulocyter in vitro [4]. Mot denna bakgrund kan IVIG vara en experimentell behandlingsform. Enstaka fallrapporter har hävdat att även en klinisk effekt finns, men kontrollerade studier saknas [24, 25]. Patienterna i Fall 2 och 3 erhöll ungefär 2 g IVIG/kg på 2 respektive 5 dagar, samma doser som givits i nyssnämnda fallrapporter[24, 25]. Det är svårt att avgöra effekten av en enskild åtgärd i komplicerade fall, men IVIG-behandling förtjänar ytterligare studier.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.