Sammanfattat
Vakuumassisterad sårbehandling (VAC) ger förbättrad sårläkning och används allt oftare vid komplicerade sår.
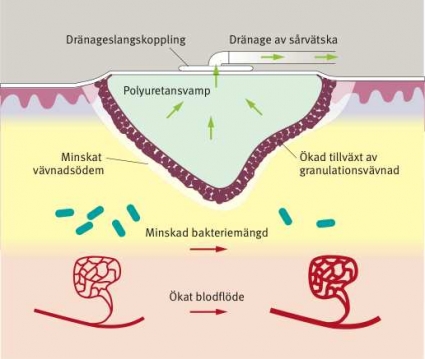
Sårbehandling med undertryck ger ökat lokalt blodflöde och minskat vävnadsödem samt stimulerar tillväxten av granulationsvävnad.
Vakuumassisterad sårläkning är en effektiv behandling vid djupa sternuminfektioner.
I detta nummer av Läkartidningen publiceras två artiklar som på olika sätt beskriver modern behandling av akut kompartmentsyndrom. I behandlingen, som beskrivs av Peter Qvarfordt och medarbetare respektive Magnus Jonsson och medarbetare, ingår såromläggning och ödemreduktion med hjälp av vakuumassisterad sårläkning (vacuum-assisted closure; VAC). Behandlingen av sår med lokalt undertryck, vilken även benämns »negative-pressure wound therapy« alternativt »topical negative pressure« i litteraturen, har under de senaste åren fått stor spridning inom flertalet specialiteter som handlägger komplicerade sår.
Vid akut kompartmentsyndrom i buken är målet, via upprepad såromläggning med VAC-förband, ett icke-ödematöst, icke-inflammerat sår som successivt reduceras i storlek. Detta ökar möjligheten för sekundär slutning samtidigt som man under behandlingstiden har ett effektivt förband som utgör en skonsam temporär bukvägg. Resultaten för 100 amerikanska patienter som genomgått bukväggsrekonstruktioner efter VAC-behandling publicerades nyligen av DeFranzo och medarbetare, och de kunde där påvisa kortare tid till sekundär slutning och minskat behov av avancerad lambåkirurgi [1].
Vi presenterar här en genomgång av de grundläggande mekanismer som anses leda till förbättrad sårläkning vid behandling med lokalt undertryck. Dessutom beskrivs en del av de kliniska resultat som uppnåtts vid VAC-behandling av djupa sternuminfektioner (mediastinit efter sternotomi) efter hjärtkirurgi vid Universitetssjukhuset i Lund.
Bakgrund
Konceptet med lokal undertrycksbehandling utarbetades i början på 1990-talet efter initiala studier av Argenta och Morykwas och lanserades i sin nuvarande form i USA 1995 av KCI Inc [2, 3]. Behandlingen användes initialt på svårläkta kroniska bensår, men efter hand har en mängd olika applikationer för lokal undertrycksbehandling vuxit fram.
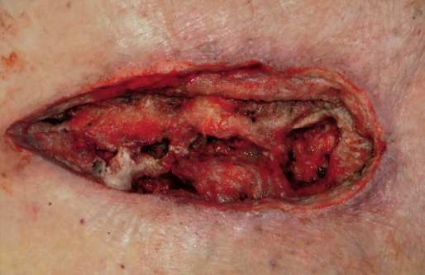
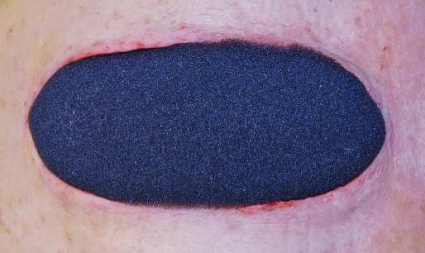
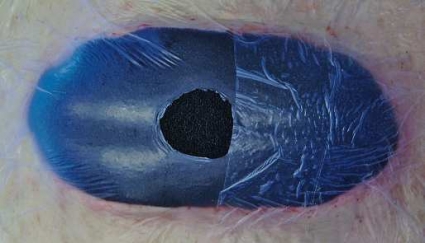
Metoden går i princip ut på att man efter sedvanlig kirurgisk revision av nekrotisk vävnad (Figur 1 a) fyller sårhålan med en storleksanpassad polyuretansvamp (Figur 1 b) med öppen porstruktur (porstorlek 400–600 (my)m). Detta moment ska dock anpassas efter sårtyp och lokalisation. Därefter täcker man över såret och omgivande hud med en självhäftande, transparent plastfilm (Figur 1 c).
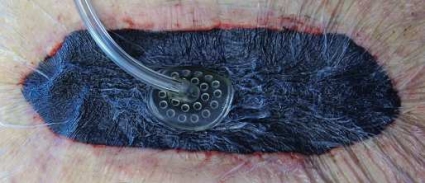
Nästa steg är att göra ett litet hål i plastfilmen (mitt på sår-svampen) där ett kopplingsstycke infogas och en dränageslang ansluts (Figur 1 d). Den andra änden av dränageslangen kopplas till uppsamlingsbehållaren på den mobila undertryckskällan (VAC-pumpen), och önskad nivå på undertryck ställs in, vanligtvis –125 mm Hg. När undertrycket kopplas på evakueras luften i såret, vilket resulterar i en komprimering av polyuretansvampen och en jämn fördelning av undertrycket i sårhålan (Figur 1 e). Medan undertrycksbehandlingen pågår är såret isolerat, och all sårvätska dräneras till den utbytbara behållaren på undertryckskällan via ett slutet slangsystem.
En välkänd förutsättning för god sårläkning är ett väldränerat sår. Vid undertrycksbehandling uppnås ett effektivt dränage i kombination med isolering av såret, vilket erbjuder fördelar från smittspridningssynpunkt och förenklad vårdlogistik, liksom möjlighet till mobilisering under pågående sårbehandling. Patienten kan ta med sig undertryckskällan på tex en rullator eller droppställning under delar av dagen genom ett inbyggt uppladdningsbart batteri.
För patienter med små sårytor finns mindre undertryckskällor, vilka med fördel kan användas i hemmet, och patienten kan då återkomma för kirurgiska revisioner och byten till ny polyuretansvamp i poliklinisk regi. Detta sistnämnda behandlingsalternativ har använts på vår klinik vid svårläkta sårinfektioner efter vengrafttagning på underbenet (vena saphena magna), som utförs i samband med kranskärlsoperationer.
Vakuumassisterad sårläkning bevarar fuktigheten i såret, vilket dels minskar risken för uttorkning och vävnadsnekros, dels stimulerar flera mekanismer som leder till förbättrad sårläkning (Figur 2).
Intervallen för svampbyten vid VAC-behandling varierar beroende på sårtyp, storlek, lokalisation och dränagemängder, men en vanlig rekommendation är 2–3 gånger per vecka. Det är dock viktigt att påpeka att vakuumassisterad sårläkning inte på något sätt ersätter kirurgisk revision eller adekvat antibiotikabehandling. Dessa komponenter måste i stället kombineras under pågående sårbehandling för att uppnå optimalt resultat.
Generella verkningsmekanismer vid VAC-behandling
Ökad bildning av granulationsvävnad. Tidiga experimentella studier av Morykwas och medarbetare visade att man fick en ökad bildning av granulationsvävnad när man behandlade sår med vakuumassisterad läkning vid –125 mm Hg [2]. Dessa fynd har konfirmerats i senare randomiserade studier vid liknande undertrycksnivåer [4].
Man har även kunnat påvisa en ökning av granulationsvävnad vid undertrycksbehandling i studier på sår där man jämfört vakuumassisterad sårläkning med konventionella fuktiga kompresser [5].
Liknande resultat, med ökad reepitelialisering och minskad såryta, har presenterats i senare publikationer [6].
Mekanismen bakom den ökade bildningen av granulationsvävnad är inte helt klarlagd, men man har föreslagit att kontakten mellan polyuretansvampen och sårytan orsakar en mekanisk påverkan på cellväggen och cytoskelettet. Vakuumassisterad sårläkning approximerar vävnadskanterna och utövar därigenom en kraft på omgivande vävnad. Studier har visat att mekanisk påverkan på cytoskelettet kan ha en positiv effekt vid sårläkning genom en stimulerad frisättning av andra budbärare (second messengers), uppreglering av tillväxtfaktorer och ökad cellproliferation [7, 8]. Det är tidigare visat att successiv uttänjning av huden inför lambåkirurgi stimulerar neoangiogenes och ökar den mitotiska aktiviteten i huden [9].
Man har därför framlagt teorin att den positiva effekt man ser vid vakuumassisterad sårläkning utövas som en form av »inverterad« vävnadsexpansion [10].
Ökat mikrovaskulärt blodflöde. Tidigare studier har också visat att man ökar blodflödet i sårets omgivande vävnad genom att applicera lokalt undertryck [2]. Dessa fynd har vår forskargrupp konfirmerat i laser-dopplerstudier, som visade att blodflödet i sårkanterna kan ökas med 50–200 procent vid kontinuerlig undertrycksbehandling [11]. Den optimala nivån för terapeutiskt undertryck är dock inte helt klarlagd och beror till viss del på sårstorlek, lokalisation och vävnadskomposition. Vilka mekanismer som samverkar för att öka det mikrovaskulära blodflödet är inte heller helt fastställt. En hypotes som diskuterats är att undertrycket ger en ökad hydrostatisk gradient över arteriolerna och att man därigenom drar blodet ut till sårkanten längs blodkärlet [12].
Minskat vävnadsödem. Sårinfektioner följs av en inflammatorisk reaktion med en ökad kärlpermeabilitet och ett ökat vätskeutträde extracellulärt. Denna mekanism leder i sin tur till ett lokalt vävnadsödem i omgivande mjukvävnad. Man har beskrivit det som att det i en ödematös sårkant råder ett lokalt kompartmentsyndrom som hindrar det kapillära blodflödet. Försämrat blodflöde påverkar syresättningen och nutritionen av såret negativt samt minskar möjligheterna till effektiv antibiotikaterapi. En verkningsmekanism som föreslagits är att reduktionen av ödemet minskar vävnadsturgor och därigenom sänker kapillärernas afterload, vilket i sin tur förbättrar cirkulationen [2]. Andra studier har visat att lokal undertrycksbehandling också minskar det lokala vävnadsödemet genom att återställa kärlpermeabiliteten och reducera mängden inflammatoriska mediatorer i såret [13, 14].
Minskad bakteriemängd. Man har också föreslagit att vakuumassisterad sårläkning skulle minska bakteriemängderna i såret [2]. Denna mekanism är dock fortfarande mer kontroversiell, eftersom de flesta studier har varit relativt små, och vissa senare publikationer har även visat motstridiga data [5, 15]. Sårläkningen har i vissa fall fortskridit i oförminskad takt trots kvarvarande bakteriemängder. Det har därför diskuterats huruvida man kan använda sig av etablerade nivåer för vävnadsinfektion eller ej vid användning av undertrycksbehandling eller om det kräver andra riktlinjer framöver.
VAC vid djupa sternuminfektioner efter hjärtkirurgi
Djup sternuminfektion är en potentiellt livshotande komplikation som uppträder hos 1–5 procent av patienterna efter hjärtkirurgi. Välkända patientrelaterade riskfaktorer är diabetes mellitus, hjärtsvikt, njursvikt, adipositas, KOL (kroniskt obstruktiv lungsjukdom) och perifer kärlsjukdom [16]. Trots modern antibiotikaregim rapporteras 30-dagarsmortaliteten i litteraturen vanligen till 10–25 procent [17-19]. Denna komplikation är således fruktad av behandlande läkare samtidigt som den orsakar patienten ett stort lidande i form av sårrelaterad smärta samt ökad mortalitet. Samtidigt belastas sjukvårdens resurser i form av upprepade kirurgiska behandlingar, långvariga sjukhusvistelser, isolering på intensivvårdsavdelningar och ökat vårdbehov av närvarande personal.
Studier från USA har visat att en djup sternuminfektion (mediastinit efter sternotomi) kostar 2–3 gånger så mycket som en standardmässig hjärtoperation utan postoperativ sårinfektion [20]. Dessa resultat har verifierats i en nyligen publicerad studie från vår forskningsgrupp, som analyserade kostnader för djupa sternuminfektioner vid svenska förhållanden [21].
Parallellt med utvecklingen av modern hjärtkirurgi har ett flertal konventionella behandlingar mot djup sternuminfektion utvecklats [16]. Traditionella tekniker är bla direkt resutur av sternum efter kirurgisk revision, öppet sternum med multipla byten av koksaltkompresser, antibiotikainnehållande spoldrän av sternumsåret och kirurgi med användande av oment-, pektoral- eller rektuslambåer [22]. Dessa infektionsbehandlingar har använts var för sig eller i olika kombinationer, men begränsas alla av att de ursprungligen har utvecklats för en klinisk situation, som inte motsvarar dagens hjärtkirurgi. Traditionella tekniker är behäftade med osäker effekt, långa vårdtider och procedurassocierade komplikationer [22].
Detta har sammantaget lett till otillfredsställande behandlingsresultat för dagens mer komplicerade patientklientel i kombination med ökande antibiotikaresistensproblematik.
På avdelningen för thoraxkirurgi vid Universitetssjukhuset i Lund inleddes redan 1999 ett pionjärarbete med att utveckla och anpassa VAC-behandlingen från kroniska bensår till djupa sternuminfektioner efter hjärtkirurgi [23]. I vårt koncept används VAC-behandling som primärt behandlingsalternativ fram till sekundär slutning av sternum utan komplettering med avancerad lambåkirurgi. Studier från vår forskningsgrupp har visat mycket goda resultat jämfört med tidigare konventionella behandlingar, och med en successivt ökande erfarenhet har en standardiserad behandlingsalgoritm för VAC-behandling utarbetats i Lund [16, 22, 24].
Liknande resultat med vakuumassisterad sårläkning vid djupa sternuminfektioner har presenterats från andra internationella toraxkirurgiska centrum [25, 26]. Förutom att VAC-behandling erbjuder ett väldränerat och isolerat sår, ger den komprimerade polyuretansvampen en momentan stabilitet av torax med möjlighet till full mobilisering under pågående terapi. Stabiliteten är viktig, eftersom den ger mindre sårsmärta och möjliggör en god respirationsmekanik. Vår forskargrupp har i en tidigare studie visat hur respirationen påverkas vid undertrycksbehandling av sternum och mediastinum [27]. Ett stabilt sternum minskar även risken för att sternumkanterna skaver mot underliggande högerkammare. Kammarrupturer är beskrivet vid konventionell mediastinitbehandling och kan vara en letal komplikation även vid omedelbar tillgång till toraxkirurgisk kompetens [28, 29].
Behandling med vakuumassisterad sårläkning för djup sternuminfektion ska alltid ske i kombination med sedvanlig kirurgisk revision och adekvat antibiotikaterapi. Vid avdelningen för thoraxkirurgi i Lund antibiotikabehandlas patienterna i samråd med infektionsläkare, och vanligtvis initieras en intravenös kombinationsbehandling med vankomycin och imipenem vid misstänkt sternuminfektion. I samband med revision och inläggande av VAC-svampen tas multipla vävnadsodlingar (totalt 5 odlingar), och så fort odlingssvar med resistensmönster finns tillgängliga inriktas antibiotikabehandlingen mot ansvarig patogen. Den vanligast förekommande bakteriestammen är koagulasnegativa stafylokocker, vilken nu har passerat Staphylococcus aureus som huvudansvarig för djupa sternuminfektioner i vår del av världen [17, 30].
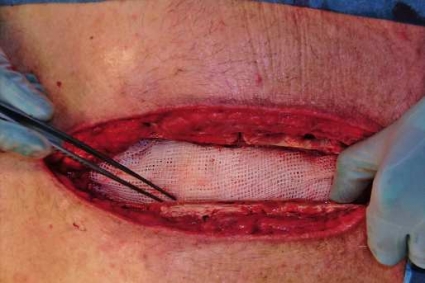
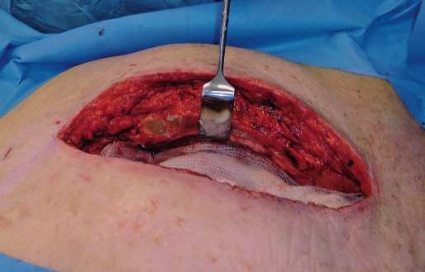
Vid VAC-behandling av djupa sternuminfektioner måste man, precis som vid behandling av andra känsliga organ och strukturer, ta vissa specialhänsyn. Vid VAC-behandling efter hjärtkirurgi måste underliggande vävnad som hjärta, bypassgrafter och i viss mån lungor skyddas mot alltför kraftiga undertryck med multipla lager av vaselinkompresser (Figur 3 a). Dessutom bör man fridissekera hjärtat noggrant från sternum, dels för att möjliggöra en sekundär resutur av sternum, dels för att minska risken för hjärtskador till följd av kraftig hosta eller skav från vassa sternumkanter (Figur 3 b). Högerkammarrupturer har rapporterats även vid vakuumassisterad sårläkning, och en trolig orsak är att dissektionsarbetet har utförts utan adekvat kirurgisk erfarenhet eller att underliggande organ inte har skyddats i tillräcklig utsträckning [31].
Slutligen ska man vid behandling av djupa sternuminfektioner använda sig av två lager polyuretansvamp: den första svampen placeras mellan sternumkanterna (Figur 3 c), medan den andra svampen placeras subkutant och fixeras mot hudkanten (Figur 1 b). Därefter sker inplastning och koppling samt aktivering av undertryck på sedvanligt sätt.
Byten av polyuretansvamparna sker cirka 2–3 gånger per vecka på operationsavdelningen med patienten intuberad, muskelrelaxerad och i generell anestesi, vilket möjliggör adekvat revision. Gamla VAC-svampar och vaselinkompresser avlägsnas försiktigt från såret (gärna med hjälp av ljummen koksaltlösning), och icke-granulerad, nekrotisk vävnad revideras samtidigt som sternumkanterna förbereds för en senare sternumslutning. Med hjälp av VAC-behandling kan man i stor utsträckning undvika ett totalnekrotiskt sternum som kräver lambåkirurgi med mjukdelsslutning och ett så kallat hjärtbråck som följd [32]. Patienten extuberas på operationssalen efter svampbytet och flyttas till vanlig vårdavdelning för fortsatt mobilisering efter några timmars övervakning.
Även om det rent tekniskt inte är speciellt avancerat att initiera VAC-behandling för djup sternuminfektion, bör man inte överlåta detta moment till en oerfaren kollega på jourtid utan möjlighet till snar senior backup. Våra egna erfarenheter tyder på att undertrycksbehandling har en beskedlig inlärningskurva om tekniken introduceras på ett strukturerat sätt och att goda kliniska resultat kan uppnås direkt [33].
Behandlingens progress följs genom
• patientens kliniska bild under VAC-behandlingen
• sårets läkningsprocess i samband med byte av polyuretansvamp
• resultat från vävnadsodlingarna
• dagliga provtagningar av CRP-nivåer.
Avvecklingen av undertrycksbehandlingen sker när följande krav är uppfyllda:
• patienten ter sig kliniskt stabil
• såret är täckt med välvaskulariserad granulationsvävnad
• odlingssvaren är negativa
• CRP-nivån har en sjunkande trend och är stabil runt 50–70 mg/l.
CRP-nivåerna bör sjunka successivt efter det att VAC-behandlingen har initierats under det att adekvat antibiotikabehandling har påbörjats. Man får dock vara beredd på att patientens CRP-nivåer stiger något dagen efter ett svampbyte som en reaktion på den kirurgiska revisionen. CRP-värdet ska dock snabbt återta sin sjunkande trend, och i annat fall bör man vara observant på andra orsaker till CRP-stegringen, tex pneumoni.
Effektivt koncept
Sammanfattningsvis kan man säga att VAC-behandling är ett effektivt koncept för sårläkning, vilket har spridit sig till en mängd specialiteter på grund av sina goda kliniska resultat. Genom vetenskapliga studier har man successivt börjat få klarhet i de bakomliggande mekanismer som leder fram till förbättrad sårläkning. Det är dock viktigt att påpeka att vakuumassisterad sårläkning inte ersätter kirurgisk revision eller adekvat antibiotikabehandling. Dessa komponenter måste i stället kombineras i en strukturerad behandlingsalgoritm för att uppnå ett optimalt kliniskt resultat.
*
Potentiella bindningar eller jävsförhållanden: Johan Sjögren och Ronny Gustafsson har erhållit forskningsanslag från KCI Inc för studier av långtidsresultat vid VAC-behandlade sårinfektioner efter toraxkirurgi. Övriga: Inga uppgivna.