Sammanfattat
Svensk förening för klinisk kemi har genom en tvärvetenskaplig arbetsgrupp tagit fram rekommendationer om njurfunktionsundersökning. Flera förbättringar rekommenderas.
Njurfunktionen bör anges som relativt GFR (glomerulär filtrationshastighet) med enheten ml/min/1,73 m2.
Relativt och absolut GFR ska tydligt särskiljas.
Eliminationsundersökning, tex med iohexol, för att mäta clearance är referensmetoden.
Cystatin C ger resultat som är oberoende av muskelmassa och rekommenderas vid utredning, för barn, inför läkemedelsbehandling och vid låg muskelmassa.
Kreatinin kan användas för att följa upp patienter med känd njurskada.
Kvantifiering av albumin (albumin-/kreatininkvot) i morgonurin kompletterar utredningen av njurskada.
Standardisering och kvalitetssäkring kan förbättras.
Njuren är ett tyst organ. Först vid omfattande skador uppkommer kliniska symtom. Tidig och adekvat diagnostik av njurpåverkan kräver därför biokemiska markörer av god kvalitet, ordinerade vid rätta indikationer och korrekt tolkade.
Det finns i dag en osäkerhet om bästa diagnostiska strategi. Därtill har brister i dagens metodik nyligen lyfts fram [1]. Osäkerheten har inte blivit mindre i och med att en nyare markör, cystatin C, blivit tillgänglig på landets laboratorier. Samtidigt har än en gång njurfunktionens betydelse för rätt läkemedelsbehandling poängterats i Läkartidningen [2-4]. Svensk njurmedicinsk förening har också nyligen lagt fram rekommendationer om utredning och behandling av njursjukdomar [5].
För att söka konsensus om optimal diagnostik av nedsatt njurfunktion initierade Svensk förening för klinisk kemi (SFKK) en arbetsgrupp (Fakta 1) med uppdrag att ge kliniska rekommendationer inom njurdiagnostiken. Denna grupp, med representanter för klinisk kemi, njurmedicin, transplantationskirurgi och allmänmedicin, har nu lagt fram sitt konsensusdokument. Det finns tillgängligt på SFKK:s webbplats http://www.kliniskkemi.org [6].
Dokumentet vänder sig till icke-specialiserad njursjukvård. Målgruppen är främst primärvården, men eftersom njurdiagnostik bedrivs inom alla specialiteter är råden riktade till hela sjukvården. Några huvuddrag ska här presenteras.
Begreppet GFR centralt
Rekommendationens grundläggande punkt är att framhäva begreppet GFR (glomerulär filtationshastighet). Det är denna hastighet som är avgörande i bedömningen av en patients njurfunktion, inte plasmakoncentrationen i sig av biokemiska markörer. Oftast sker en omräkning med någon av de tillgängliga formlerna utifrån plasmahalten av exempelvis kreatinin.
Vi vill nu i stället uppmana till att ange och diskutera patientens njurfunktion i GFR. Denna trend har redan fått sitt fotfäste i USA, där National Kidney Disease Education Program under de senaste åren bedrivit ett aktivt arbete med att förbättra diagnostiken och öka medvetenheten bland läkare och allmänhet om GFR:s betydelse [7].
I Sverige har utvecklingen accentuerats av att mer än 20 laboratorier nu utför analys av cystatin C och då automatiskt gör en beräkning av relativt GFR. Denna beräkning medföljer analysresultatet. Vid behov av absolut filtrationshastighet, som vid ordination av njurtoxiska läkemedel, tillhandahåller svenska laboratorier webbaserade algoritmer.
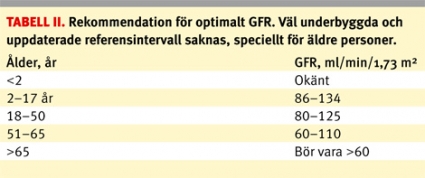
Vi vill i våra rekommendationer betona betydelsen av att kliniskt resonera i GFR, snarare än i koncentration av markör, tex kreatinin och cystatin C. Stadieindelning av njursjukdom grundar sig på GFR (Tabell I). Vi vill därför rekommendera att GFR bestäms vid all diagnostik och uppföljning av njursjukdom och inför dosering av läkemedel som utsöndras via njurarna. På sikt bör endast GFR anges, men säkert behövs en längre övergångsperiod då också plasmakoncentrationen av den biokemiska markören lämnas ut.
En svaghet som vi identifierat är att de referensintervall som i dag finns för GFR måste förbättras (Tabell II). Det gäller framför allt hos den stora gruppen äldre patienter. Dagens referensintervall får därför ses snarast som rekommenderade intervall.
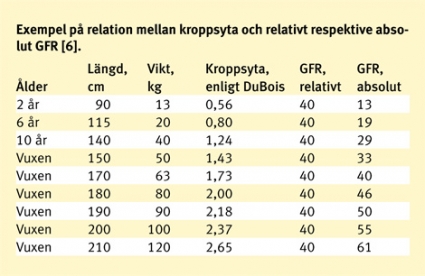
Det är viktigt att skilja på relativt och absolut GFR. Vid diagnostik och uppföljning är det relativt, eller kroppsytenormerat, GFR som är aktuellt. Däremot ska absolut GFR beräknas då läkemedel som elimineras via njurarna ska ges. Det är speciellt viktigt att skilja relativt och absolut GFR åt när det gäller barn eller personer med kraftigt avvikande kroppsvikt (Fakta 2).
Dagens metoder för att bestämma GFR
De finns i dag tre dominerande metoder för att bestämma GFR: eliminationsundersökningar, cystatin C och kreatinin. Samtliga metoder har styrkor och svagheter och kan komplettera varandra. De behöver dock förbättras på flera punkter.
Eliminationsundersökning med iohexol eller krom-EDTA. Elimination (clearance) från plasma via glomerulär filtration av exogent tillförd substans utgör referensmetoden. För optimal mätning ska undersökningsmetodiken uppfylla strikta krav på given dos och provtagningsintervall. Här behöver laboratorierna se över sina rutiner.
Cystatin C. Beräkning av GFR utifrån analys av cystatin C i plasma kan vid nedsatt njurfunktion ge resultat som motsvarar de värden som erhålls med eliminationsundersökning. Analysen bör beställas på barn och initialt i en utredning, speciellt om endast lätt njurpåverkan misstänks.
Analysen bör beställas när det kan förväntas att olika faktorer påverkar nivån av kreatinin så att felaktigt estimerat GFR fås. Detta är fallet hos patienter med hög ålder och reducerad muskelmassa. Metoden bör användas för GFR-estimering inför läkemedelsbehandling som ska anpassas utifrån njurfunktionen. Cystatin C kan användas vid diagnostiktillfället, medan kreatininbaserad beräkning av GFR sedan kan användas för att följa njursjukdomens förlopp.
Estimerat GFR bör anges upp till 90 ml/min/1,73 m2. Över denna nivå bör resultat anges som >90 ml/min/1,73 m2.
Cystatin C har få kända interferenser, men påverkan har rapporterats vid tyreoideasjukdom och behandling med steroider i hög dos.
En internationell standardisering, initierad av Svensk och Nordisk förening för klinisk kemi, väntas vara klar inom ett år och behövs bla för bättre överförbarhet av resultat mellan olika laboratorier nationellt och internationellt.
Kreatinin. I Sverige har vi nu genom gemensamma ansträngningar, koordinerade av EQUALIS (Extern kvalitetssäkring inom laboratoriemedicin i Sverige), uppnått god standardisering av kreatinin med liten analytisk spridning mellan olika laboratorier. Flera olika biologiska tillkortakommanden kvarstår dock, speciellt vid liten muskelmassa och lätt njurskada, vilket gör att njurskada kan undgå upptäckt om endast kreatinin ordineras. Estimering av GFR utifrån analys av kreatinin i plasma är dock en acceptabel metod för vuxna personer med normal muskelmassa för att följa redan känd minskning av GFR. Estimerat GFR bör beräknas upp till 60 ml/min/1,73 m2. Över denna nivå bör resultat anges som >60 ml/min/1,73 m2.
Beräkningen av GFR bygger på att kreatininvärdet värderas i relation till muskelmassan hos en individ. Detta kräver i moderna algoritmer att ålder och kön (men inte längd och vikt) är kända parametrar. Muskelmassan kan variera även utan koppling till ålder och kön, något som ökar metodens osäkerhet.
Övriga analyser. Vid undersökning av njurfunktionen bör GFR kompletteras med andra biokemiska metoder, främst kvantifiering av albumin i urin. Samtidig analys av kreatinin i urin bör då göras (albumin-/kreatininkvot, uttryckt i mg/ mmol). Analys bör göras på morgonprov och normalt behövs inte dygnsurin.
Kreatininclearance ska inte utföras på grund av svårkontrollerade felkällor, främst vid urinsamling.
Hälsoekonomiska effekter
Kostnaderna för njursjukvård, dialys och läkemedelsbiverkningar orsakade av njurfunktionsrubbning är mycket höga. En tidig intervention har en njurskyddande effekt. Korrekt GFR-bestämning inför vissa läkemedelsbehandlingar kan reducera kostnader för biverkningar [3].
Iohexolbelastning är cirka tio gånger dyrare än bestämning av cystatin C. Som för andra belastningsundersökningar är de samhällsekonomiska kostnaderna betydligt högre. De rörliga kostnaderna i form av reagens är i dag cirka tio gånger högre för cystatin C än för kreatinin.
Beaktande att cirka 10 miljoner kreatininanalyser årligen utförs i Sverige skulle en generell övergång från kreatinin till cystatin C med dagens reagenspriser teoretiskt innebära en avsevärd kostnadsökning. En ökad analysvolym kan i framtiden sannolikt reducera reagenskostnad per analys.
Datoriserad estimering av GFR innebär i sig inga ökade kostnader. Däremot minskas personalkostnader och felkällor inom vården om beräkningen av GFR görs automatiskt.
En god ekonomisk analys har inte gjorts, men sannolikt bör en kostnadsökning inom diagnostiken reducera kostnader inom klinisk sjukvård.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Konsensusdokumentet, med ytterligare referenser, finns på webbplatsen för Svensk förening för klinisk kemi: http://www.kliniskkemi.org/Filer/Dokument/31/Konsensus%20om%20GFR%20final%20080318.pdf