Sammanfattat
Idiopatisk spontan kranskärlsdissektion är en ovanlig orsak till akut koronart syndrom. Diagnosen bör övervägas särskilt hos yngre kvinnor utan riskfaktorer för kranskärlssjukdom och som visar symtom som vid akut koronart syndrom.
Ingen enskild mekanism kan helt förklara patogenesen vid spontan kranskärlsdissektion.
Snar koronarangiografi är viktig för korrekt diagnos och behandling. Prognosen avgörs av dissektionens lokalisation och utbredning.
Här beskrivs 4 fall där yngre medelålders och medelålders kvinnor med få eller inga riskfaktorer för hjärt–kärlsjukdom insjuknat i akut koronart syndrom och där koronarangiografi visade dissektion av ett eller flera kranskärl.
Våra patientfall beskriver tillståndets varierande prognos och de olika behandlingsalternativ som rekommenderas i litteraturen.
Kranskärlsdissektion kan uppstå vid aortadissektion, trubbigt toraxtrauma, hjärtkateterisering, koronarangioplastik och aortokoronar bypass-operation men kan också uppkomma spontant, och det senare illustreras i de fallbeskrivningar som presenteras i denna artikel. Spontan kranskärlsdissektion delas ofta in i tre grupper: hos patienter med bakomliggande ateroskleros, hos kvinnor i tredje trimestern av graviditeten eller tidigt post partum samt idiopatisk dissektion [1].
Spontan kranskärlsdissektion är en sällsynt orsak till akut koronart syndrom och plötslig död. Cirka 300 fall finns beskrivna i litteraturen [2]. Tillståndet har beskrivits i Läkartidningen 1990 [3]. Majoriteten av dessa patienter är kvinnor (80 procent), varav cirka 25 procent drabbas peripartalt [4]. I en nyligen publicerad undersökning där man gick igenom 11 605 koronarangiografier fann man 23 fall av spontan kranskärlsdissektion. 74 procent gällde kvinnor, och av dessa var inga gravida eller befann sig i postpartumperioden [5].
Incidensen av spontan kranskärlsdissektion vid konsekutiva koronarangiografier har rapporterats variera mellan 0,1 och 1,1 procent [6]. Incidensen är sannolikt underskattad då spontan kranskärlssjukdom kan leda till plötslig död och diagnosen inte ställs såvitt obduktion inte utförs [7]. Det finns sannolikt även en viss underdiagnostik av detta tillstånd. Man kan misstänka att flera fall missas när kranskärlet är ockluderat på grund av dissektionen och man inte ser någon dubbellumenkontrast under koronarngiografin. De flesta dissektioner involverar endast ett kranskärl. Vänster koronarartärs främre nedåtstigande gren (LAD) är det mest frekvent involverade kärlet hos kvinnor (80 procent), medan det hos män oftare är höger koronarkärl som drabbas (60 procent) [8]. Dissektion av vänster huvudstam och flerkärlsdissektion har sämre prognos med risk för plötslig död eller utbredd hjärtinfarkt [9].
Fallbeskrivningar
Fall 1. Vår första patient var en 38-årig tvåbarnsmor utan riskfaktorer för hjärt–kärlsjukdom som insjuknade akut med tryckande bröstsmärta, illamående och kräkningar med en duration på 20–30 minuter. Hon remitterades till akutmottagningen. I ankomststatus noterades en helt opåverkad kvinna med normalt hjärt–lungstatus, blodtryck 125/90 mm Hg och ett invändningsfritt EKG. En översiktlig ekokardiografisk undersökning på akutmottagningen visade normalstor vänster kammare med ordinära kontraktioner.
Troponin I var förhöjt (0,21 µg/l; referensvärde <0,03, gränsen för hjärtinfarkt >0,10), och patienten lades in på hjärtintensivvårdsavdelningen (HIA). Behandling inleddes med acetylsalisylsyra (ASA), betablockad, klopidogrel och lågmolekylärt heparin. En troponin I-kurva som vid en mindre hjärtinfarkt utvecklades, och koronarangiografi efterföljande dag visade en mindre dissektion distalt i LAD, i övrigt normala kranskärl. Förnyad ekokardiografi visade normala förhållanden. Patienten skrevs ut med ASA, betablockad och tre månaders klopidogrelbehandling. Vid återbesöket åtta veckor senare var patienten helt besvärsfri.
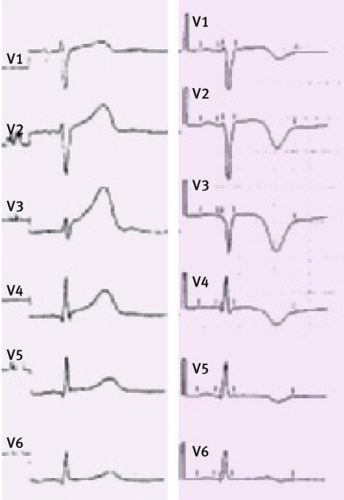
Fall 2. Vårt andra patientfall gällde en 33-årig icke-rökande tvåbarnsmor utan hereditet för ischemisk hjärtsjukdom som under de senaste fem dagarna vid två tillfällen sökt husläkare på grund av kortvarig ansträngningsutlöst obehagskänsla i bröstet. EKG var vid båda dessa tillfällen normalt, varför ingen ytterligare åtgärd vidtogs. Under ankomstdagen debuterade mer intensiva bröstsmärtor i samband med ett träningspass. Vid ankomsten till akutmottagningen var patienten blek och smärtpåverkad. EKG visade ST-höjning över framväggen (Figur 1), och hon fördes till HIA. Patienten fick behandling med ASA, intravenös betablockad och sublinguala nitrater. Akut ekokardiografisk undersökning visade regional anterior hypokinesi, och patienten ordinerades trombolys med tPA (vävnadsplasminogenaktivator) eftersom detta fall är från 1995 när akut koronarangiografi inte var förstahandsåtgärd.
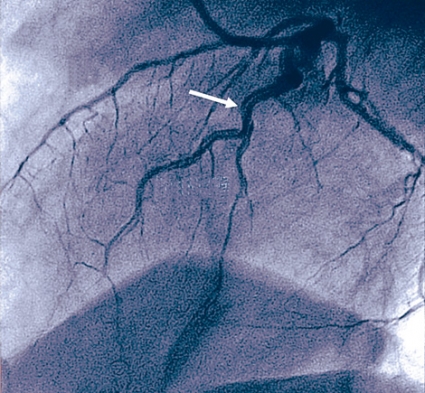
Hon blev efter denna behandling snabbt smärtfri. I laboratorievärden noterades ett CK-MB på maximalt 78 µg/l som vid måttligt stor hjärtinfarkt. Koronar-angiografi visade en flera centimeter långsträckt dissektion av LAD med början strax efter avgången från huvudstammen (Figur 2). Förnyad ekokardiografisk undersökning visade oförändrad anterior hypokinesi med nedsatt ejektionsfraktion (cirka 40 procent). Toraxkirurgi övervägdes men det beslutades om konservativ behandling. Efterförloppet var komplikationsfritt, och patienten skrevs ut till hemmet med ASA, betablockad, långverkande nitrater och warfarin (vilket vid tiden för insjuknandet var en vanlig behandlingsrutin vid större framväggsinfarkter).
Poliklinisk kontrollangiografi efter sex veckor visade att dissektionen var under läkning, dock med kvarstående dubbellumen. Efter sex månader visade förnyad koronarangiografi en oförändrad bild. Drygt 10 år senare avled emellertid patienten plötsligt i ett hjärtstopp i samband med fysisk ansträngning. Obduktionen visade att dödsorsaken var kranskärlsdissektion med blödning i vänster koronarartärs huvudstam och ocklusion av kärllumen.
Patient 3. Vår tredje patient var en 39-årig kvinna, även hon utan riskfaktorer för kranskärlssjukdom. Sedan några månaders tid hade hon i vila besvärats av episoder av timslång tryckkänsla i bröstet som strålade ut i armarna. Under en semester i Sydeuropa fick hon accentuerade symtom med domningar ut i vänster arm, och vid besök på akutmottagningen konstaterades relativt kraftig troponinförhöjning och inferiora EKG-förändringar. Koronarangiografi visade dissektion i ett dominant höger kranskärl, och patienten fick akut behandling med intrakoronar trombolys. Ekokardiografi visade nedsatt ejektionsfraktion (40–50 procent) med hypokinesi inferiort och posteriort. Behandlingen inleddes med ASA, ACE-hämmare och statin. På grund av hypotension avstod man från betablockad. Vid hemgången var patienten välmående och besvärsfri.
Patienten följdes upp på hemsjukhuset med arbetsprov. Vid en belastning på 140 W utvecklade hon tryckkänsla i bröstet med obehag ut i armarna. På EKG noterades ST–T-sänkningar och T-invertering inferiort samt uttalade ST-sänkningar anterolateralt. Patienten lades in för observation. Vårdförloppet var komplikationsfritt, och man beslutade om konservativ behandling med förhoppning om kollateralutveckling. Vid det första återbesöket tre veckor senare besvärades hon emellertid av viss angina. Myokardskintigrafi visade antytt nedsatt upptag apikalt anteriort och basalt inferolateralt, dock utan tecken till reversibilitet, varför ny koronarangiografi inte gjordes. Vid uppföljningen några månader senare mådde patienten väl och besvärades inte av angina.
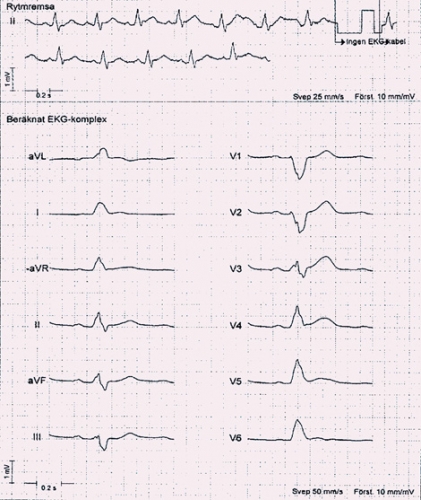
Fall 4. Vårt fjärde patientfall var en 60-årig kvinna, före detta rökare, med hypertoni. Hon vaknade allmänpåverkad och med kraftig central bröstsmärta. EKG som skickades från ambulansen till HIA visade atypiskt vänstersidigt skänkelblock (Figur 3). Tillståndet behandlades som akut ST-höjningsinfarkt, och hon fick ASA, lågmolekylärt heparin, klopidogrel och betablockad.Koronarangiografi genomfördes akut, vilken visade måttliga stenoser i arteria cirkumflexa, i en marginalgren och i en måttligt stor intermediärgren där också trombrester noterades distalt om stenosen (Figur 4). Stenosen i intermediärgrenen bedömdes vara en så kallad nyckelstenos (culprit lesion). Kärlet var dock för litet för intervention, och man beslutade om konservativ behandling. Ekokardiografi ett dygn senare visade antydd hypokinesi apikalt men med bevarad ejektionsfraktion. I samband med ett arbetsprov inför hemgången kollapsade patienten. Akut EKG visade nytillkomna ST-höjningar anterolateralt, och en akut koronarangiografi genomfördes. De tidigare beskrivna stenoserna i arteria circumflexa kunde inte lokaliseras, intermediärgrenen sågs nu vara ett stort kärl med en dissektion proximalt hela vägen distalt ut i kärlet (Figur 3). De beskrivna stenoserna bedömdes vara dissektioner, alternativt kärlspasm.
Efter diskussion beslutades om konservativ behandling, men patienten utvecklade tilltagande sviktsymtom. Det gjordes en ny ekokardiografi, och man fann tillkomst av betydande systolisk nedsättning av vänsterkammarfunktionen, perikardvätska och begynnande apikal aneurysmutveckling. Patienten behandlades konservativt och skrevs sedermera ut med ASA, betablockad och ACE-hämmare.
Drygt en månad senare sökte hon akut på grund av tilltagande hjärtsviktssymtom, och man noterade kraftig pro-BNP-förhöjning (14 500 ng/l). Ekokardiografi visade måttligt dilaterad vänsterkammare, apikalt aneurysm, förhöjda fyllnadstryck, måttlig mitralisinsufficiens och liksom tidigare betydande systolisk funktionsnedsättning.
Vid den tredje koronarangiografin gick det inte att identifiera någon dissektion, och den bedömdes därför vara utläkt. Vänsterkammarangiografi visade som tidigare ett stort vänsterkammaraneurysm. Patienten accepterades för operation med vänsterkammarrekonstruktion och samtidig ventrikeltakykardikirurgi. Operationen utfördes komplikationsfritt. En slagvolymsbedömning med magnetkamera (MRI) visade minskad kammarvolym och förbättrad ejektionsfraktion (från 24 till 32 procent). Patienten har vid uppföljning återfått god funktionsnivå och kan promenera obehindrat utan begränsande symtom.
Diskussion
Våra fall beskriver idiopatisk spontan kranskärldissektion och representerar väl hur patientpopulationen ser ut avseende könsfördelning (övervikt för kvinnor), ålder (vanligen medelålders personer), avsaknad av riskfaktorer för hjärt–kärlsjukdom samt variation i förlopp och prognos. Den senare bestäms av dissektionens lokalisation och dess utbredning.
I det första fallet drabbades patienten av en mindre dissektion distalt i LAD. Hon var hela tiden kliniskt stabil utan angina eller andra kliniska tecken till progress. Prognosen bedömdes god, varför någon förnyad koronarangiografi inte genomfördes. Fall nummer två visar på risken för recidiv och den sämre prognos som föreligger vid större och mer proximal dissektion av LAD. Vår patient drabbades i mitten av 1990-talet, och trombolys bedömdes då vara det mest lämpliga alternativet. Patienten avled plötsligt under fysisk aktivitet flera år senare på grund av förnyad dissektion.
I det tredje fallet har dissektionen en något mindre vanligt förekommande lokalisation (höger koronarkärl) men är typisk avseende kön och ålder. Någon intervention genomfördes inte utan patienten följdes kliniskt och har stabiliserats. Det fjärde fallet illustrerar att även patienter med kända riskfaktorer för aterosklerotisk hjärtsjukdom kan ha dissektion. Fallet visar också hur dramatiskt sjukdomsförloppet i vissa fall kan utvecklas främst beroende på dissektionens lokalisation och utbredning.
Alltjämt oklar etiologi. Etiologin bakom spontan kranskärlsdissektion är alltjämt oklar. Bland kvinnor som drabbas i samband med graviditet eller post partum anges cirka 30 procent ha riskfaktorer för ateroskleros. Multiparitet och hög ålder har rapporterats öka risken, och hos dessa patienter är ofta flera kranskärl involverade. Hypoteser har lagts fram om förändringar i kärlväggen, dels på grund av förändrad hemodynamik med ökad blodvolym och ökad hjärtminutvolym (cardiac output), dels på grund av hormonella faktorer med åtföljande strukturella förändringar i kärlväggen [10]. Skjuvkrafter (»shear stress«) i cirkulationen i samband med fysisk ansträngning och förlossning ökar sannolikt risken för kranskärlsdissektion hos predisponerade individer, vilka sannolikt är individer med försvagad kärlvägg på grund av hormonella faktorer, periadventiell inflammation, bindvävsdefekter eller andra okända faktorer. Dissektionen medför att kärllagren separeras och median skiljs från adventitian, varvid ett falskt lumen uppkommer och komprimerar det äkta kärllumen. Därmed orsakas distal myokardischemi med infarktutveckling [7].
I den idiopatiska gruppen saknas konventionella riskfaktorer för kranskärlssjukdom [11]. En svag men viss ökad risk för kranskärlsdissektion har setts hos rökare och hos hypertoniker. Spontan kranskärlsdissektion har också rapporterats hos patienter med Marfans syndrom, Ehlers–Danlos’ syndrom (EDS), polyarteritis nodosa och vid systemisk lupus erythematosus (SLE). Kranskärlsdissektion har även associerats med medicinering med orala antikonceptiva medel, cyklosporiner och vid kokainintag. Spontan dissektion har också beskrivits i samband med eller efter fysisk ansträngning hos annars friska medelålders individer [6].
Diagnos, behandling och prognos. Diagnosen ställs med koronarangiografi och bör övervägas hos yngre kvinnliga patienter som trots avsaknad av riskfaktorer för kranskärlssjukdom presenterar symtom som vid akut koronart syndrom [4, 12]. Intravaskulärt ultraljud kan i vissa fall användas för att differentiera aterosklerotisk kranskärlssjukdom från dissektion, särskilt vid svårtolkade angiogram, och för att bedöma utbredningen av dissektionen [13].
Det saknas klara behandlingsriktlinjer. Behandlingen avgörs av dissektionens lokalisation, antalet affekterade kärl, blodflödet i kranskärlen och hemodynamiken hos patienten [6, 14]. Antitrombotisk behandling med acetylsalicylsyra, klopidogrel och lågmolekylärt heparin samt antiischemisk behandling med nitrater och betablockad har föreslagits vara medicinsk basbehandling för kliniskt stabila patienter med begränsad dissektion [14].
Vid återkommande ischemi där större kärl är angripna rekommenderas ofta perkutan koronarintervention (PCI), men komplikationer med såväl retrograd som antegrad dissektion kan uppstå [15]. En vanlig rekommendation i den medicinska litteraturen är att genomföra bypass-kirurgi vid flerkärlsdissektion eller dissektion av vänster huvudstam [1, 7]. Även vid kirurgi kan det dock vara svårt att identifiera och begränsa dissektionen.
Trombolysbehandling kan lysera intramurala koagel men kan potentiellt expandera det intramurala hematomet med ytterligare dissektion och därmed mer utbredd ischemi som påföljd [2, 16]. I fallrapporter har framgångsrik aggressiv immunsuppressiv behandling med steroider och cyklofosfamid till patienter med flerkärlsdissektion beskrivits. Detta kan möjligen övervägas om operation inte kan genomföras [17].
Vid genomgång av litteraturen ses varierande mortalitetsdata mellan 48 och 82 procent. Plötslig död har rapporterats i 28–63 procent av fallen, särskilt vid dissektion av vänster huvudstam [15]. Cirka 50 procent återinsjuknar med ytterligare dissektion i samma eller annat kranskärl inom 1–2 månader efter den första händelsen. De patienter som överlever den akuta fasen anges ha en överlevnadsprognos på 80 procent under 30 månader, oavsett behandlingsregim. Män har beskrivits ha en högre överlevnad än kvinnor (93 respektive 74 procent) [7]. Långtidsprognosen är dock god vid begränsad dissektion då kärllumen inte är totalt obstruerat, vid komplikationsfritt infarktförlopp, och vid avsaknad av kvarstående ischemitecken vid efterföljande stresstest [9].
Slutkommentarer
Idiopatisk spontan kranskärlsdissektion är en ovanlig orsak till akut koronart syndrom. Diagnosen bör emellertid övervägas hos yngre medelålders och medelålders kvinnor utan kardiovaskulära riskfaktorer som visar symtom som vid akut koronart syndrom. Vid misstanke om spontan kranskärlsdissektion bör antitrombotisk behandling och antiischemisk behandling påbörjas. Koronarangiografi bör utföras snarast för diagnos och beslut om vidare behandling, därutöver ges medicinsk behandling. Även PCI eller bypass-kirurgi kan bli aktuellt. Dessa beslut baseras på dissektionens lokalisation, antalet drabbade kärl, blodflödet i kranskärlen och patientens hemodynamik. Snabb diagnos och start av behandling är av stor vikt då tillståndet överlag har en god prognos.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.