Sammanfattat
Läkemedelsorsakad levertoxicitet är en viktig differentialdiagnos vid kliniska fynd tydande på leversjukdom.
En patient som utvecklat ikterus efter intag av det till synes ofarliga kosttillskottet Fortodol beskrivs.
Eftersom kosttillskottets innehåll uppfattades som harmlöst ur levertoxisk synvinkel fördröjdes diagnosen.
När det uppdagades att nimesulid, en substans med dokumenterade hepatotoxiska biverkningar, i det dolda tillförts kosttillskottet Fortodol fann man en rimlig förklaring till patientens leverpåverkan.
Ett tätare samarbete mellan Läkemedelsverket och Livsmedelsverket är önskvärt för att tidigare kunna identifiera liknande säkerhetsproblem i framtiden.
Trots den utbredda användningen av komplementära alternativmedicinska produkter, såsom kosttillskott och naturläkemedel, är ofta säkerhetsproblematiken kring dessa medel dåligt kartlagd. Om dessutom en annan farmakologiskt aktiv substans i det dolda tillförs ett sådant medel kan särskilt svåridentifierade säkerhetsproblem uppkomma. Syftet med ett sådant förfarande kan vara att förstärka den farmakologiska effekten av produkten [1]. Beskrivningen av preparatet kan därmed ge en felaktig bild av produktens säkerhet, och denna felaktiga information kan bidra till att biverkningar orsakade av den tillsatta substansen undgår upptäckt eller fördröjs påtagligt. Internationellt finns tyvärr många exempel på denna typ av manipulering [1]. Även i Sverige har denna typ av manipulerade produkter avslöjats [2].
Vi beskriver ett fall där allvarlig leverpåverkan utvecklades hos en patient som intagit det till synes ofarliga kosttillskottet Fortodol och där orsakssambandet förblev oklart under flera månader.
Fallet
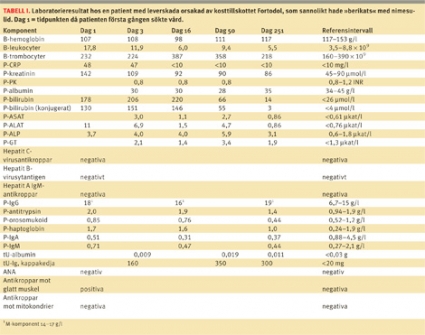
En 91-årig vital kvinna noterade tillkomst av mörkfärgad urin och misstänkte att hon drabbats av urinvägsinfektion. En vecka senare kontaktade hon vårdcentralen eftersom hon dessutom fått aptitlöshet, illamående och svår klåda. Provtagning påvisade fynd som vid urinvägsinfektion och behandling med pivmecillinam (Selexid) påbörjades. Man noterade också att kvinnan var ikterisk. Kompletterande blodprov (Tabell I, dag 1) visade tydlig leverpåverkan, varför patienten remitterades till Universitetssjukhuset i Linköping. Ultraljudsundersökning av buken var utan anmärkning.
Kvinnan behandlades för hypertoni och var tidigare opererad för ett meningeom. Hon besvärades sedan många år av ryggvärk. Alkoholöverkonsumtion och rökning negerades. Hon medicinerade sedan många år tillbaka med hydroklortiazid plus amilorid (Normorix mite) och acetylsalicylsyra (Trombyl). Vid specifik förfrågan uppgav patienten att hon de senaste två månaderna även ätit kosttillskottet Fortodol för att lindra ryggvärken.
Ingen rimlig förklaring till leverskadan
Under vårdtiden var hon mentalt opåverkad och hade normala PK-INR-värden. Man fann inga hållpunkter för aktuell eller genomgången infektion med hepatit A, B eller C. Då inga tecken till akut leversvikt förelåg genomfördes den fortsatta utredningen polikliniskt. Eftersom man inte kunnat påvisa någon rimlig förklaring till sjukdomsbilden övervägdes om intaget av Fortodol kunde vara orsaken. Enligt patientens medhavda förpackning innehöll Fortodol de verksamma substanserna gurkmeja och fenylalanin. Hon uppmanades i avvaktan på utredningens resultat att inte inta Fortodol.
Telefonkontakt togs med Läkemedelsverket för att beskriva reaktionen och efterhöra om liknande fall hade rapporterats tidigare. Eftersom Fortodol är ett kosttillskott hänvisades till Livsmedelsverket, som efter en litteratursökning meddelade att man inte hade funnit rapporter om att gurkmeja eller fenylalanin hade associerats med leverskador.
Differentialdiagnoser övervägdes
Alternativa diagnoser övervägdes. Man påvisade antikroppar mot glatt muskulatur och förhöjt IgG i plasma – fynd som kan vara förenliga med autoimmun hepatit. Emellertid var antikropparna inte riktade mot F-aktin, vilket är det vanligaste vid autoimmun hepatit [3], och IgG-stegringen var monoklonal, något som inte heller talar för autoimmun hepatit. I urinelektrofores kunde man påvisa förekomst av Bence Jones’ proteinuri med utsöndring av monoklonala kappakedjor, varför misstanke om plasmacellssjukdom uppstod.
Obstruktiv ikterus orsakad av myelominfiltration i pankreas har rapporterats [4]. Även infiltration av plasmaceller i levern har beskrivits [5]. Utredningen kompletterades därför med magnetkameraundersökning av buk och rygg, som inte kunde påvisa några avvikelser i pankreas eller tecken till vidgade gallvägar. I ryggraden sågs uttalade spondylosförändringar men inga destruktioner eller lytiska lesioner. Benmärgspunktion visade bild förenlig med »monoclonal gammopathy of undetermined significance« (MGUS). Hematolog bedömde att plasmacellsinfiltration i lever eller pankreas var osannolik.
Orsaken till patientens leverskada var fortfarande oklar. Patientens allmäntillstånd förbättrades, men klådan var fortfarande besvärande och lindrades inte av vare sig anjonbytare eller antihistaminer. Leverbiopsi övervägdes för att kunna differentiera mellan toxisk leverskada, autoimmun leversjukdom och ikterus orsakad av amyloidos [6] eller plasmacellsinfiltration [5]. Patienten ville dock avvakta. Ikterus gick sedermera i regress, och nivåerna av aminotransferaser, ALP och γ-GT i plasma sjönk successivt.
Drygt åtta månader efter insjuknandet hade patienten endast en diskret kvarstående klåda, och biokemiskt sågs en lätt förhöjning av leverproven med företrädesvis kolestatiskt mönster. M-komponenten och Bence Jones-proteinurin har ökat svagt men inte till några kliniskt signifikanta nivåer.
Diskussion
Diagnostiken av levertoxicitet orsakad av läkemedel eller alternativmedicinska substanser är ofta svår eftersom det inte finns några tillförlitliga diagnostiska markörer. Diagnostiken baseras i regel på anamnestiska uppgifter. Ofta rör det sig om en tidigare leverfrisk patient som utvecklat tecken till leverskada efter intag av en potentiellt levertoxisk substans och där utredning inte påvisat någon annan orsak till leverskadan, som exempelvis missbruk av alkohol och/eller illegala droger, leversteatos, cirkulatorisk insufficiens, viral hepatit, autoimmun leversjukdom eller mekanisk obstruktion av gallvägarna. Ytterligare stöd för diagnosen substansorsakad leverskada erhålls om patienten samtidigt med insjuknandet uppvisar allergiska manifestationer, om tillfrisknande sker efter utsättning av den misstänkta substansen, om ny hepatotoxisk reaktion uppkommer vid (ofrivillig) reexponering eller, i de fall leverbiopsi utförs, om leverhistologin är förenlig med leverskada som har associerats med substansen i fråga.
Incidensen av läkemedelsorsakad leverskada
Incidensen av läkemedelsorsakad leverskada är ofullständigt känd eftersom metoderna som används i populationsbaserade undersökningar är behäftade med många nackdelar, såsom underrapportering och retrospektiv design med ofullständig information, i synnerhet angående självmedicinering och intag av hälsokostpreparat [7-9]. I en prospektiv fransk studie, där uppföljningstiden var tre år, rapporterades att incidensen av leverrelaterade biverkningar av läkemedel var 14 fall per 100 000 invånare och år [10]. Sannolikt underskattar denna siffra den verkliga incidensen eftersom endast symtomatiska patienter inkluderades i analysen.
Incidensen av svår läkemedelsorsakad leverskada är avsevärt lägre och har uppskattats till 7,4 fall per miljon invånare och år [11]. I en nyligen publicerad studie kom man fram till att 3,5 procent av 800 ikteriska patienter hade läkemedelsorsakad leverskada [12]. Om den läkemedelsorsakade hepatocellulära skadan har gett upphov till ikterus kan prognosen vara allvarlig. I en svensk studie rapporterades att 12,7 procent av dessa patienter avled eller genomgick levertransplantation [13]. Liknande siffror (11,7 procent) har rapporterats från Spanien [14].
Långdraget förlopp hos vår patient
Vår patient utvecklade, förutom ikterus, initialt en tydlig hepatocellulär skada med övervägande ALAT-stegring. Senare i förloppet dominerades den kliniska och biokemiska bilden av en blandad hepatocellulär och kolestatisk reaktion med dominans av den senare komponenten. I dessa fall är mortaliteten låg men sannolikheten för kronicitet är större inkluderande utveckling av prolongerad kolestas och av en histologisk bild som i anglosaxisk litteratur betecknas med termen »vanishing bile duct syndrome« [15]. Det långdragna förloppet vid kolestatiska reaktioner illustreras också av vår patient, som ännu drygt åtta månader efter leverskadans debut har kvar lättare klåda i kombination med förhöjda leverprov av företrädesvis kolestatisk profil.
Även om leverbiopsi inte genomfördes på den aktuella patienten kunde övrig utredning med rimlig säkerhet utesluta andra orsaker till hennes ikterus. Trombyl och Normorix mite hade hon ätit i flera år. Ett tidssamband mellan intag av Fortodol och hepatotoxicitet fanns, och en tydlig regress av leverskadan sågs när användningen av Fortodol upphörde. Emellertid kvarstod en osäkerhet kring diagnosen eftersom Fortodol, oss veterligt, inte innehöll någon känd hepatotoxisk substans.
Fortodol var orsaken
Misstanken om att Fortodol orsakade den allvarliga leverreaktionen bekräftades dock nio månader efter den inträffade händelsen. Läkemedelsverket rapporterade då att man fått kännedom om fyra fall av leverpåverkan hos svenska patienter som intagit Fortodol. En av patienterna utvecklade akut letal leversvikt. Vår patient var inte inkluderad bland dessa fall. I Norge hade dessutom ytterligare fyra fall av leverpåverkan, varav ett med dödlig utgång, efter intag av Fortodol beskrivits [16].
Läkemedelsverket undersökte innehållet av Fortodol närmare och fann att flera förpackningar innehöll, förutom gurkmeja och fenylalanin, cyklooxygenashämmaren nimesulid. Nimesulid är i vissa länder ett registrerat läkemedel men har aldrig registrerats i Sverige. Substansen har en dokumenterad förmåga att kunna orsaka leverskada [17]. Företaget som tillhandahåller Fortodol i Sverige har polisanmälts för misstanke om brott mot läkemedelslagen.
Vår patient hade således intagit ett till synes tämligen harmlöst kosttillskott, som sannolikt »berikats« med en substans som var känd för att ge hepatotoxiska biverkningar. Få fall av denna typ av manipulation är kända i Sverige. Internationellt är dock fenomenet att blanda konventionella läkemedel med naturläkemedel för att förstärka effekten av de senare ett välkänt problem [1].
Tätare samarbete mellan myndigheter nödvändigt
I det aktuella fallet tog det lång tid att finna förklaringen till patientens sjukdomsbild, och patienten fick genomgå en rad undersökningar. Eftersom kosttillskottets innehåll uppfattades som harmlöst ur levertoxisk synvinkel fördröjdes diagnosen. Fallet illustrerar också att inblandade myndigheter kan ha svårt att upptäcka och kartlägga säkerhetsproblematiken vid denna typ av händelser. Läkemedelsverket ansvarar för läkemedelssäkerheten i Sverige, men eftersom det rörde sig om ett kosttillskott så hanteras säkerhetsfrågor primärt av Livsmedelsverket. I de fall som läkemedel tillsatts kosttillskott övergår ansvaret till Läkemedelsverket.
Vi anser att ett tätt samarbete mellan Livsmedelsverket och Läkemedelsverket är nödvändigt. Gemensamma utredningar vid misstanke om biverkningar av kosttillskott vore värdefulla. Att dessutom i högre grad använda sig av Läkemedelsverkets spontanrapporteringssystem för biverkningar bör vara ett viktigt instrument för att tidigt kunna identifiera och bevaka säkerhetsproblematiken även för kosttillskott. Numera finns också ett separat spontanrapporteringssystem för konsumentrapportering, vilket bör vara extra värdefullt i detta arbete.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.