Någon form av blodtrycksstegring under graviditet ses hos ca 8 procent av alla gravida kvinnor, och 3–4 procent insjuknar i preeklampsi [1, 2]. Trots förbättrad mödrahälsovård och neonatalt omhändertagande orsakas fortfarande en betydande del av maternell och fetal mordbiditet och mortalitet av preeklampsi.
Denna artikel avser att ge en beskrivning av det moderna omhändertagandet av kvinnor med preeklampsi. I den mån sådant material finns tillgängligt baseras texten på meta-analyser och randomiserade, kontrollerade studier.
Etiologi – »teoriernas sjukdom«
Etiologin bakom preeklampsi är långt ifrån klarlagd. Preeklampsi har med fog kallats för »the disease of theories«, och en systematisk genomgång av mekanismerna bakom preeklampsi ligger långt bortom målsättningen med denna artikel. Immunologiska mekanismer, endotelcellsdysfunktion och genetisk predisposition anses ligga bakom sjukdomsutvecklingen.
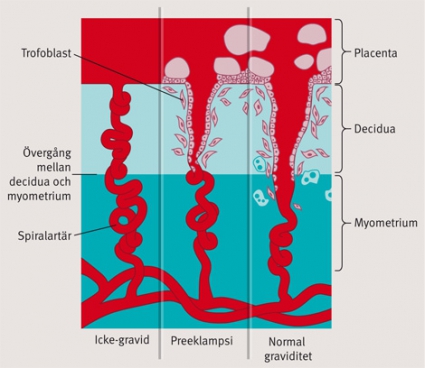
Vid normal graviditet sker en trofoblastinvandring genom deciduan och in i myometriet, en process som är nödvändig för att omvandla spiralartärena till eftergivliga lågresistenta kärl, vilket möjliggör en effektiv gas- och näringstransport till fostret. Vid preeklampsi sker en ofullständig invandring av trofoblaster, och flödesmotståndet i spiralartärena förblir högt. Störd endotelcellsfunktion vid preeklampsi ger upphov till trombocytaktivering och aktivering av koagulationskaskaden. Flera teorier avseende orsaken till endotelcellsdysfunktion vid preeklampsi har framlagts. En attraktiv modell är att den hypoxiska placentan frisätter endoteltoxiska substanser. Placentans produktion av prooxidanter är ökad medan dess bildning av antioxidanter är nedsatt vid preeklampsi, vilket skulle kunna ge upphov till oxidativ stress och därmed kärlskada. sFLt1 (soluble fms-like tyrosine kinase 1) bildas i ökad mängd vid preeklampsi och hämmar angiogenesen, som är en förutsättning för en normal placentation [3].
hypertonitillstånd under graviditet
Hypertoni som uppträder under graviditet kan klassificeras i fyra huvudgrupper baserat på rekommendationer från International Society for the Study of Hypertension in Pregnancy [4].
Graviditetshypertoni definieras som blodtryck ≥140/90 mm Hg som utvecklas efter graviditetsvecka 20 och där inga hållpunkter för preeklampsi finns. Blodtrycksmätning bör utföras vid två tillfällen med 4–6 timmars mellanrum [4]. Blodtrycksstegringen ska gå i remission spontant inom tolv veckor post partum. I frånvaro av blodtryck ≥140/90 mm Hg bör en blodtryckstegring på ≥30/15 mm Hg från inskrivningsblodtrycket inge misstanke om eventuell graviditetsrelaterad hypertoni [5]. Graviditetshypertoni innebär endast måttligt ökad risk för perinatal morbiditet, medan svår graviditetshypertoni är jämförbar med preeklampsi [6].
Preeklampsi definieras som blodtryck ≥140/90 mm Hg som utvecklas efter graviditetsvecka 20 med samtidig signifikant proteinuri ≥0,3 g/dygn. Liksom för graviditetshypertoni ska blodtrycksstegringen gå i remission spontant inom tolv veckor post partum. Svår preeklampsi definieras som blodtryck ≥160/110 mm Hg och/eller proteinuri ≥5 g/dygn. En alternativ indelning som förespråkas av vissa författare är indelningen i tidig (debut <34 veckors graviditet) och sen (debut ≥34 veckors graviditet) eftersom tidig debut oftare är förenad med ett mer dramatiskt förlopp och mer uttalad fosterpåverkan än sen debut [7].Kronisk hypertoni är essentiell eller sekundär hypertoni som diagnostiserats före graviditeten eller före graviditetsvecka 20.Kronisk hypertoni med pålagring av preeklampsi är hypertoni med utveckling av tecken till preeklampsi. För diagnos krävs en blodtrycksstegring på ≥30/15 mm Hg och tillkomst eller förvärring av redan befintlig proteinuri. I detta sammanhang bör nämnas att 10–15 procent av alla patienter med eklampsi och 12–18 procent av alla med HELLP (hemolysis, elevated liver enzymes, low platelet count syndrome) har normalt blodtryck vid ankomst till sjukhuset [8]. Tidigare ansågs ödem vara ett av huvudsymtomen vid preeklampsi, men det innefattas inte längre i diagnoskriterierna. Dock uppvisar ofta patienter med preeklampsi ökad ödembenägenhet på grund av ökad kärlpermeabilitet med påföljande extravasering av vätska från blodbanan [3]. Av den anledningen ses ofta höga hemoglobinvärden hos kvinnor med preeklampsi, inte sällan före sjukdomsdebuten.Proteinuri Rutinmässigt används urinstickor för detektion av proteinuri, där ≥1+ protein ska utgöra grund för vidare diagnostik av proteinuri. Definitionsmässigt anses en proteinutsöndring i urinen på ≥0,3 g/dygn som patologisk under graviditet [4]. Numera använder vissa centra albumin/kreatininkvoten i urinen för bestämning av signifikant proteinuri, där ca ≥30 mg/mmol motsvarar 0,3 g albumin/dygn [9]. Huruvida albumin/kreatininkvoten kan användas för att exakt kvantifiera dygnsutsöndringen av albumin är dock kontroversiellt [10]. Trots massiv proteinuri är njurfunktionen, uppskattad enligt lokala rutiner med kreatinin eller cystatin C [11], i de flesta fall normal. Något klart samband mellan grad av proteinuri och maternell/fetal morbiditet finns inte [12].Multiorganpåverkan Multiorganpåverkan (framför allt CNS, koagulation, lever) ses i synnerhet vid svår preeklampsi. I frånvaro av proteinuri anser vissa författare att preeklampsi föreligger vid hypertoni i kombination med organpåverkan. Tecken till CNS-påverkan i form av huvudvärk och synfenomen (fotopsi och/eller skotom) är vanligt. Hyperreflexi och klonus bör inge misstanke om progress till eklampsi [13]. Stroke kan förekomma vid svår, okontrollerad preeklampsi [14]. Koagulationspåverkan förekommer i synnerhet vid svår preeklampsi, men lindrig trombocytopeni kan ses även vid lättare fall. Hemolys och disseminerad intravasal koagulation (DIC) ses i 10 procent av fallen med svår preeklampsi [15]. Leverpåverkan med stegrade transaminaser och smärta under höger arcus ses i synnerhet vid begynnande HELLP-syndrom [16]. Man bör ha i åtanke att plasmanivåer av γ-glutamyltransferas (γ-GT), aspartataminotransferas (ASAT), alaninaminotransferas (ALAT) och bilirubin ofta är lägre hos friska gravida än hos icke-gravida kvinnor [17]. Eftersom störd placentafunktion är en av de patogenetiska hörnpelarna vid preeklampsi är intrauterin tillväxthämning, för tidig avlossning av placenta (ablatio placentae), fetal hypoxi och intrauterin fosterdöd betydligt vanligare i denna patientgrupp än bland kvinnor utan blodtryckssjukdom. En betydande del av fetal morbiditet och mortalitet beror på iatrogen prematurbörd på maternell indikation [15].Riskfaktorer Preeklampsi drabbar i första hand förstföderskor. Det finns en relativt stor återupprepningsrisk för preeklampsi, och tidigare genomgången preeklampsi är sålunda en betydande riskfaktor hos omföderskor [18]. Hos patienter som vid första graviditeten var normotensiva är risken för utveckling av preeklampsi vid påföljande graviditet reducerad med 90 procent om den blivande barnafadern är densamme. Riskreduktionen elimineras vid partnerbyte och minskar vid lång duration mellan graviditeterna [15]. Hereditet ökar risken för preeklampsi, men även hereditet för preeklampsi hos den blivande barnafadern (dvs svärmor och svägerska) tycks öka risken för insjuknande [19]. Äggdonation [15], flerbörd [20] och mola hydatidosa ökar risken för preeklampsi [21]. Ökad risk för preeklampsi ses vid fetal trisomi 13 [22]. Huruvida trisomi 18 och trisomi 21 ökar risken för preeklampsi är oklart [23]. I övrigt är riskfaktorerna för insjuknande i preeklampsi påfallande lika dem för övrig kardiovaskulär sjukdom och innefattar högt BMI (>30), hyperlipidemi, nedsatt insulinkänslighet, diabetes mellitus typ 2, graviditetsdiabetes, polycystiskt ovariesyndrom, vissa trombofilier och hög maternell ålder [15]. Rökning [24], genomgången abort (spontan eller legal) och partnerbyte efter genomgången preeklampsi tycks minska risken för preeklampsi [25].
PREDIKTION OCH PREVENTION
Otaliga analyser och undersökningar för att identifiera patienter med ökad risk att utveckla preeklampsi har tagits fram. Ingen av dem har emellertid uppvisat tillräckliga prestanda för att kunna introduceras som screeningtest.
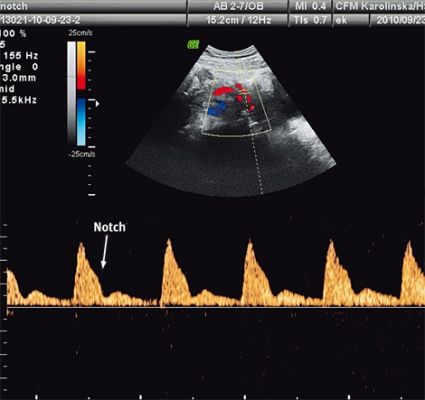
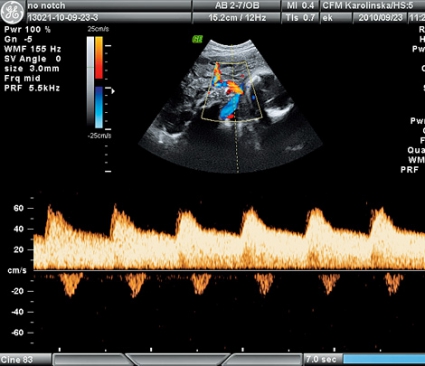
Den i dag mest använda undersökningen för att bedöma risken att utveckla preeklampsi är dopplerundersökning av uterinartärerna. Ökad resistens (i synnerhet vid förekomst av »diastolisk notch«) i graviditetsvecka 22–24 är förenad med ökad risk att utveckla preeklampsi. Normalfynd vid undersökningen har ett högt negativt prediktivt värde för utveckling av svår preeklampsi [26]. Undersökningen kan användas hos kvinnor med ökad risk för preeklampsi men är inte lämplig för screening av en lågriskpopulation [27].
Ett flertal plasmamarkörer har utvärderats i syfte att identifiera högriskpatienter. Mest studerat är plasmanivåer av sFLt1 och PLGF (placental growth factor). Förhöjda nivåer av det förra och sänkta nivåer av det senare i andra trimestern förekommer oftare hos kvinnor som senare under graviditeten insjuknar i preeklampsi än hos kvinnor som förblir friska [28].
Många farmakologiska metoder har prövats för att minska risken för insjuknande i preeklampsi, men få har visat reproducerbar effekt. Lågdos acetylsalicylika (50–100 mg dagligen) ger sannolikt en viss minskning av risken för att insjukna och förbättrar den neonatala utgången hos kvinnor med hög risk för preeklampsi, speciellt bland dem med tidigt insjuknande i preeklampsi i en föregående graviditet, och bör användas preventivt i denna grupp [29].
Hos omföderskor som vid första graviditeten diagnostiserades med preeklampsi har lågmolekylärt heparin (4 000–6 000 enheter dalteparin) visats reducera risken för insjuknande markant. Detta intressanta och lovande resultat måste dock konfirmeras i större studier innan det kan introduceras i klinisk praxis [30].
Kalciumbehandling har visats ge en riskreduktion hos högriskpatienter med samtidig kalciumbrist och bör användas hos sådana [31].
Eftersom ökad oxidativ stress antas bidra till utvecklingen av preeklampsi har antioxidanter prövats för att minska risken för insjuknande. Fiskolja [32], vitamin E och vitamin C [33] har inte visat reproducerbara riskreducerande effekter. Tvärtom såg man snarast en ökad risk för fetala komplikationer vid profylaktisk behandling med vitamin E och C.
BEHANDLING
Den i dag enda kurativa åtgärden vid preeklampsi är förlossning; i övrigt syftar behandling till att lindra symtomatologin och förbättra den maternella och fetala prognosen. Kvinnor med nyupptäckt preeklampsi bör generellt läggas in på sjukhus.
Antihypertensiv behandling vid i övrigt okomplicerad preeklampsi är alltid indicerad vid systoliskt blodtryck ≥160 mm Hg och/eller diastoliskt blodtryck ≥110 mm Hg. Syftet med behandlingen är i första hand att minska risken för maternell hypertensiv encefalopati och stroke. Det är viktigt att erinra sig att antihypertensiv behandling inte har några positiva dokumenterade effekter för fostret utan i stället kan öka risken för intrauterin tillväxthämning [34, 35]. Internationellt används ofta α-metyldopa vid underhållsbehandling av hypertoni vid preeklampsi. I Sverige är dock användningen av α-metyldopa vid preeklampsi begränsad. I vårt land används i första hand labetalol (oselektiv β-receptor- och α-receptorantagonist), pindolol (oselektiv β-receptorantagonist) eller nifedipin (kalciumflödeshämmare) vid underhållsbehandling av preeklampsi. Målblodtrycket vid antihypertensiv behandling av preeklampsi bör ligga kring 140/90 mm Hg eftersom en alltför intensiv antihypertensiv behandling kan leda till ytterligare försämring av den redan reducerade uteroplacentära genomblödningen och därmed till fetal påverkan i form av kronisk hypoxi och tillväxthämning [35].
Akut trycksänkande behandling är indicerad vid systoliskt blodtryck ≥160 mm Hg och/eller diastoliskt blodtryck ≥110 mm Hg med samtidiga symtom på CNS-påverkan på grund av risken för hypertensiv encefalopati och bör då ske skyndsamt. För akutbehandling kan dihydralazin intramuskulärt, labetalol intravenöst eller nifedipin peroralt användas [36-38].
Vid svår preeklampsi, där beslut att avsluta graviditeten är taget, bör infusionsbehandling med magnesiumsulfat övervägas för att minska risken för eklampsi [39]. Denna behandling ges även vid etablerade kramper [40].
Vid HELLP har behandling med glukokortikoider använts, och det finns data som talar för en viss förbättring vid behandling [41]. Evidensläget är dock oklart i dag för att kunna införa detta i praxis [42].
Vid lindrig preeklampsi bör man överväga induktion av förlossning snarast då patienten nått fullgången tid [15]. Under nogrann fetal och maternell kontroll kan man dock, speciellt vid omoget cervixstatus, invänta spontan värkstart alternativt utmognad av cervix inför senare induktion [43].
Vid svår preeklampsi eller tecken till fetal påverkan bör ställningstagande till induktion eller kejsarsnitt tas senast när patienten nått 32–34 graviditetsveckor [15]. Förlossning bör dock inte äga rum innan kvinnans läge bedöms vara stabilt.
Patienter med svår preeklampsi före 32–34 graviditetsveckor erbjuder ofta komplicerade överväganden avseende lämplig tidpunkt för förlossning. Här måste riskerna för en försämring av mammans och fostrets tillstånd vid exspektativ behandling vägas mot neonatala problem på grund av en för tidig förlossning. 30 procent av alla fall med HELLP och eklampsi insjuknar efter förlossningen, och patienter med preeklampsi bör därför monitoreras avseende blodtryck och laboratoriemarkörer även på BB. Insjuknande efter 48–72 timmar är dock ovanligt [16]. Kvinnor med preeklampsi under graviditeten bör övervakas på sjukhus 3–4 dygn post partum. Hos kvinnor som varit normotensiva före graviditeten kan man oftast seponera antihypertensiv behandling under BB-vistelsen. Vid persisterande blodtryck ≥150/100 mm Hg bör patienten skrivas ut med någon form av antihypertensiv behandling och följas upp inom några veckor.
LÅNGTIDSPROGNOS
Genomgången svår preeklampsi utgör en klart ökad risk för kardiovaskulär sjukdom senare i livet. Risken för hypertoni (relativ risk (RR) 3,7), ischemisk hjärtsjukdom (RR 2,2),
stroke (RR 1,8) och död (RR 1,5) är ökad [44].
Kvinnor som insjuknar i graviditetsdiabetes har ökad risk att senare i livet insjukna i diabetes mellitus typ 2 [45]. Graviditeten sänker insulinkänsligheten. Kvinnor med redan nedsatt insulinkänslighet och därmed ökad risk att senare i livet utveckla diabetes kommer därför i stor utsträckning att utveckla graviditetsdiabetes. I analogi med det kan man tänka sig att ökad risk för hypertoni och kardiovaskulär sjukdom avmaskeras under graviditeten vid graviditetsinducerad hypertoni och preeklampsi.
I en nyligen publicerad studie noterades att kvinnor med svår preeklampsi fortfarande uppvisade hypertoni (18 procent) och proteinuri (2 procent) två år efter partus och att preeklampsins svårighetsgrad och tiden mellan diagnos och partus korrelerade med postpartal förekomst av hypertoni och proteinuri [46].
Kvinnor med preeklampsi bör därför informeras om den ökade risken för kardiovaskulär sjukdom redan på BB och bör remitteras till distriktsläkare för vidare uppföljning avseende riskreduktion.
*
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.