Sammanfattat
Tocilizumab hämmar interleukin-6, vilket ofta reducerar synoviter och systemisk inflammation vid reumatoid artrit.
Hämningen av interleukin-6 leder till minskad produktion av C-reaktivt protein (CRP).
Akutfasreaktionen kan utebli eller vara mycket svag också vid svår infektion hos patienter som behandlas med tocilizumab.
Vid klinisk misstanke om svår infektion under behandling med tocilizumab bör diagnostiken aktivt drivas vidare och patienten oftast behandlas, också vid avsaknad av CRP-stegring.
Alla läkare som i sin verksamhet möter patienter med infektioner behöver vara medvetna om att immunsuppression kan påverka infektionsrisken, men också att immunsuppressionen kan modifiera den kliniska bilden vid en infektion.
Tocilizumab (RoActemra) är en humaniserad monoklonal antikropp mot interleukin (IL)-6-receptorn, registrerad 2009 för behandling av reumatoid artrit med måttlig eller hög inflammatorisk aktivitet. Preparatet ges som intravenös infusion 1 gång i månaden och kan kombineras med metotrexat eller ges som monoterapi [1]. Hämning av IL-6 med tocilizumab vid reumatoid artrit minskar ofta effektivt den inflammatoriska aktiviteten [2].
I följande beskrivning av ett fall av reumatoid artrit i samband med tocilizumabterapi åskådliggörs hur en allvarlig bakteriell infektion gav endast en mycket begränsad påverkan på akutfasreaktionen.
Fallbeskrivning
Patienten var en 50-årig fastighetsskötare med mångårig reumatoid artrit. Han hade haft behandling med de flesta konventionella antireumatiska preparaten. Av de biologiska läkemedlen hade etanercept, rituximab och adalimumab tidigare prövats. I sjukhistorien noterades, förutom vänstersidig höftprotesoperation och handledsartrodes, en traumatisk hälseneruptur 2008 med komplicerat förlopp postoperativt på grund av infektion.
Vid det nu aktuella insjuknandet behandlades han med ciklosporin och prednisolon (6,25 mg/dygn), omeprazol och naproxen vid behov. I februari 2011 hade behandling med tocilizumab påbörjats. Eftersom den första dosen gav en infusionsreaktion, gavs reducerade doser i mars och april. Infusionen i juni och den senaste, 28 juli, gavs i full dos utan komplikationer, och behandlingen hade god effekt.
Under kvällen den 17 augusti kände patienten klåda och en stickande känsla i huden på höger underarm. Under natten tillkom värk och svullnad i höger armbågsled.
Den 18 augusti togs prov på vårdcentralen inför nästa planerade tocilizumabinfusion, men han sökte läkare först den 19 augusti, då besvären från armbågen tilltagit.
Armbågsleden var då kraftigt svullen, palpationsöm och värmeökad. På underarmen noterades ett långsträckt område med rodnad, indurerad och ömmande hud, med några enstaka, maximalt knappnålshuvudstora pustler. Kroppstemperaturen var 36,7 °C, och kapillärt CRP (C-reaktivt protein) uppmättes till <8 mg/l. Efter kontakt med reumatologjouren remitterades patienten till Norrlands universitetssjukhus i Umeå.
Ultraljudsundersökning på reumatologmottagningen bekräftade vätska i armbågsleden, och i punktat från leden påvisades 76,7 × 109 leukocyter/l. Patienten lades in på infektionskliniken med fortsatt opåverkat allmäntillstånd, normalt blodtryck, puls och saturation. I blodstatus noterades lätt leukocytos, 10,2 × 109/l med neutrofil övervikt, ej avvikande från patientens tidigare värden, och högsensitivt CRP (hsCRP) i plasma var endast 8 mg/l.
Eftersom septisk artrit inte kunde uteslutas, påbörjades behandling med 1 g cefotaxim intravenöst 3 gånger dagligen. I analys av ledvätska konstaterades förhöjt laktat 9,2 mmol/l (referensvärde <7 mmol/l) men inga bakterier i direktmikroskopi. I odling av ledvätskan, liksom i blododlingar, påvisades Staphylococcus aureus. Kirurgisk spolning och inläggning av drän utfördes den 22 augusti. Fortsatt antibiotikabehandling i 3 månader planerades.
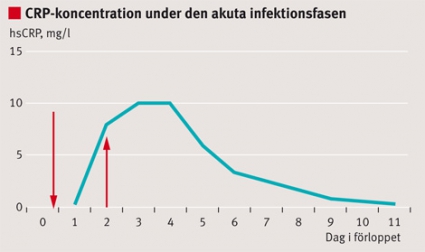
Den maximala kroppstemperaturen under vårdtiden var 37 °C och CRP maximalt 10 mg/l (Figur 1).Diskussion
Vår patient hade en säkerställd septisk artrit med en symtomduration på nära 2 dygn när han sökte. Trots detta sågs bara en blygsam akutfasreaktion, utan feber, sjukdomskänsla, annan allmänpåverkan eller signifikant CRP-stegring (Figur 1). Inflammationsreaktionen över armbågen var tydlig, men inte typisk för en septisk artrit. Dock fanns nedom armbågen en hudreaktion med enstaka, knappt synliga pustler. Värt att observera är också att vid den planerade provtagningen, dagen efter symtomdebuten, var koncentrationen av CRP lägre än metodens detektionsnivå (<0,6 mg/l) (Figur 1).
Akutfasreaktion kännetecknas av bl a feber, trötthet, matleda, katabolism, leukocytos och trombocytos [3]. Koncentrationen av flera plasmaproteiner (akutfasproteiner) förändras, men undersökning av CRP har störst kliniskt användningsområde. Av de proinflammatoriska cytokiner (IL-6, IL-1β och tumörnekrosfaktor [TNF]) som är involverade i akutfasreaktionen anses cirkulerande IL-6 ha störst betydelse. Produktionen av CRP i hepatocyter medieras huvudsakligen av IL-6 [4]. Syntesen av IL-6 induceras av både IL-1β och TNF, men också av bakteriella endotoxiner [3].Doctor’s delay en risk vid avvikande akutfasreaktion
Risken att akutfasreaktionen försvagas vid tocilizumabbehandling är kopplad till verkningsmekanismen (IL-6-hämningen) och påtalas också i Fass-texten [1]. I en kohortstudie av incidensen av infektioner vid tocilizumabbehandling sågs dock CRP-stegring vid svår infektion hos 6 av 8 individer [5]. Man förklarar detta med att infektionerna debuterat 3–4 veckor efter senaste infusion och att IL-6-hämningen då var i avtagande. Också i vårt fall debuterade infektionen 3 veckor efter den senaste tocilizumabinfusionen, men den begränsade akutfasreaktionen talar för att en kraftfull suppression kvarstod. Patienten hade i samband med tidigare infektioner haft tydlig CRP-stegring.
En av riskerna med den avvikande akutfasreaktionen är s k doctor’s delay. Det finns flera orsaker till att detta undveks i detta fall, såsom hudreaktionen, ledpunktionen och det höga antalet vita blodkroppar i ledvätskan. Av avgörande betydelse var också att vi gemensamt diskuterade både handläggningen av patienten och risken att tocilizumabbehandlingen påverkade den kliniska bilden.
Patienten har tillfrågats om sin medverkan och sin uppfattning av förloppet. Han tyckte inte att artriten var påtagligt avvikande. Han var i första hand intresserad av lokal kortisoninjektion, och han var tveksam till om remitteringen till Umeå verkligen var nödvändig. Han kände till att behandlingen kunde öka risken för infektioner men mindes ingen information om att behandlingen kunde påverka hur en infektion yttrar sig.Risk att infektioner får förändrat kliniskt uttryck
Med detta patientfall vill vi påminna om den ökade risken för infektioner hos immunsupprimerade patienter och risken att infektioner får ett förändrat kliniskt uttryck hos dessa patienter. Vi vill också påminna om vikten av att alltid kontrollera vilka läkemedel en patient tar eller får och att ta hänsyn till de specifika modifikationer av immunsvaret som dessa läkemedel kan orsaka. Vid osäkerhet om handläggningen av misstänkt infektiösa tillstånd hos patienter med immunsuppressiv terapi bör behandlande klinik konsulteras.
*
Potentiella bindningar eller jävsförhållanden: Lotta Ljung har arvoderats för utbildningsuppdrag av Bristol-Myers Squibb.
*
Patienten har varit delaktig i beskrivningen av förloppet och haft synpunkter på det färdiga manuskriptet.