Cogans syndrom är en ovanlig inflammatorisk sjukdom med en triad av inflammatorisk ögonsjukdom, audiovestibulära symtom och vaskulit.
Hälften av patienterna drabbas av systemiska komplikationer.
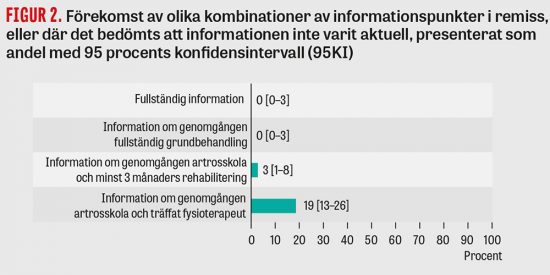
Diagnosen är klinisk. Infektiösa och autoimmuna differentialdiagnoser bör uteslutas innan diagnosen ställs.
Behandlingen består av steroidbehandling i hög dos, lokala kortisondroppar till drabbat öga och eventuellt tillägg av utökad immunsuppressiv terapi om svar på kortisonbehandling är otillräckligt.
En 53-årig tidigare väsentligen frisk kvinna insjuknade i mars 2015 med yrsel, illamående, kräkningar och tinnitus i vänster öra. Yrseln upplevdes som en konstant ostadighetskänsla med svårigheter att stå på benen och sekundlånga attacker av rotatorisk yrsel. Några dagar senare tillkom små rundade, ca 2 mm upphöjda, spridda icke-kliande utslag över ben och bål samt nedsatt hörsel på framför allt vänster öra. Initiala labbprov visade CRP 108 mg/l, TPK 50 × 109/l, normalt LPK. Inga kliniska infektionstecken noterades vid undersökning. Audiogram visade uttalad vänstersidig hörselnedsättning; öron-, näs- och halsspecialist fann inga tecken till mellanörepåverkan. Insjuknandet tolkades som laesio auris interna, det vill säga någon form av akut skada i innerörat på vänster sida (Figur 1).
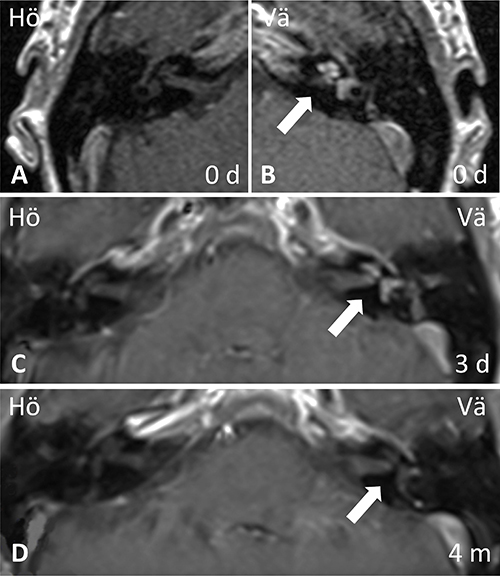
Patienten lades in för kortisonbehandling i hög dos, men något dygn senare tillkom plötslig irritation i höger öga och dimsyn. CRP hade då sjunkit till 40 mg/l, TPK normaliserats och LPK stigit till 16,5 × 109/l. Ögonläkare bedömde detta som en kraftig irit, och lokalbehandling för misstänkt herpes zoster-infektion initierades. Lumbalpunktion visade en cellbild förenlig med viral infektion, LPK över 600 × 109/l i likvor med monoövervikt, laktat 4,6 mmol/l samt albumin 851 mg/l. Systemisk herpes zoster-infektion misstänktes, vilket dock kunde avskrivas efter negativ PCR på likvor. Även syfilisserologi, bakteriell odling samt prov för enterovirus, TBE och Borrelia var negativa i likvor. I avsaknad av infektionsfokus tolkades leukocytstegringen som en inflammatorisk reaktion och utredningen utvidgades med reumatiska prov och röntgenundersökningar. Vaskulitscreening med analys av PR3-ANCA (antikroppar mot proteinas 3) och MPO-ANCA (antikroppar mot myeloperoxidas) var negativ. DT av torax och DT-angiografi utfördes utan att man fann tecken på vare sig sarkoidos eller storkärlsvaskulit. MR-undersökning av hjärna och MR-angiografi visade inga tecken på central vaskulit, pakymeningit, stroke eller expansiv process, men en patologisk kontrastuppladdning påvisades i koklea, vestibulum och båggångar på vänster sida (Figur 2).
Fallet diskuterades på öron-, näs- och halskliniken och ögonkliniken, Centralsjukhuset i Karlstad, och den sammansatta bilden av ögonsymtom, nytillkomna hudutslag och öronpatologi väckte misstanken om Cogans syndrom. Kraftfullare immunsuppression med cyklofosfamid lades till behandlingen, efter kontakt med reumatolog, med planering för övergång till metotrexat eller azatioprin efter 6 månader. Patienten kunde skrivas hem med kvarstående kortisonbehandling i hög dos och lokalbehandling för ögat. Vid återbesök efter 3 månader hade hennes hudutslag försvunnit, ögat förbättrats och yrsel och tinnitus hade minskat, medan ostadighetskänsla och sensorineural hörselnedsättning i vänster öra kvarstod. Uppföljande MR i samband med återbesöket visade ingen kvarvarande kontrastuppladdning i innerörat på vänster sida (Figur 2).
Historik
Cogans syndrom och atypiskt Cogans syndrom är ovanliga inflammatoriska sjukdomar utan klarlagd patofysiologi. De karaktäriseras av en kombination av audiovestibulära symtom och inflammatoriska ögonsjukdomar. Vissa patienter drabbas även av vaskulit med systemiska komplikationer [1-8].
Symtombilden presenterades för första gången av Morgan och Baumgartner 1934 i en fallrapport om en patient med interstitiell keratit och misstänkt Ménières sjukdom [9]. 1945 sammanställde den amerikanske oftalmatologen David Cogan observationer från 4 patienter (utvidgat 1959 till 13 patienter). Han beskrev ett syndrom karakteriserat av »icke-syfilisorsakad interstitiell keratit i kombination med yrsel, susningar och sensorineural hörselnedsättning« [10, 11]. 1964 publicerade han en fallbeskrivning om en patient som obducerats, där man funnit inflammatoriska förändringar i aorta, och tanken på ett möjligt samband med vaskulit föddes [12]. 1980 beskrevs en atypisk form av Cogans syndrom, och termen har kommit att användas för fall med andra typer av uveit än interstitiell keratit [4, 7, 13].
Över 70 år efter att den första patienten presenterades har vi fortfarande en begränsad förståelse av detta ovanliga syndrom med mycket varierande symtombild [4, 5]. En stor del av vad som finns beskrivet i litteraturen är fallrapporter [2]. Varken prevalens eller incidens är helt klarlagda. Symtomdebut sker oftast i 20–30-årsåldern, men även fall med patienter äldre än 50 år och barn har rapporterats. Män och kvinnor drabbas i samma utsträckning och det finns ingen känd etnisk skillnad i prevalens [5]. Det finns studier som tyder på att Cogans syndrom är vanligare hos patienter med inflammatorisk tarmsjukdom (IBD) [5, 7]. Omkring 30 fall finns beskrivna med patienter drabbade av både Cogans syndrom och IBD [5].
Patofysiologi
Patogenesen bakom Cogans syndrom är okänd [2, 4, 8]. Obduktionsmaterial från temporalben och kornea har visat en ospecifik infiltration av lymfocyter och plasmaceller, och man har ännu inte funnit några säkra histologiska tecken på vaskulit vare sig i ögon eller inneröron. Materialet som studerats har dock tagits från patienter som behandlats med kraftfull immunsuppression, vilket skulle kunna maskera en eventuell småkärlsvaskulit histologiskt. I fall med systemiska manifestationer har histologi påvisat akut och kronisk inflammation i kärlväggen från aorta [5]. Förändringarna liknar den histologiska bilden vid spridd Takayasus arterit [14]. I en studie upptäcktes antikroppar riktade mot en peptid som fick namnet Cogans peptid [15]. Den liknar CD148 och connexin 26 som båda uttrycks i endotelceller och i innerörat. I djurstudier har man visat att passiv immunisering med antikroppar mot peptiden minskar symtomen av Cogans syndrom hos möss [5]. Specifika anti-HSP (heat shock protein) 70-antikroppar har tidigare föreslagits som potentiella markörer [1, 2, 4, 5, 16] för Cogans syndrom, men har i senare studier visat sig vara ospecifika och vanligt förekommande i normalpopulationen [17-18].
Symtomatologi
Sjukdomen har i allmänhet en plötslig debut och snabb progress, men symtom från ögon och öron uppkommer inte alltid simultant.
De audiovestibulära besvären börjar oftast med isolerade vestibulära symtom, precis som i det beskrivna fallet. Detta kan likna debuten av Ménières sjukdom med tinnitus, yrsel samt illamående och kräkningar [3, 19]. Symtomen är till skillnad från vid Ménières sjukdom oftast bilaterala [3] men kan även uppkomma unilateralt [5]. I de allra flesta fall tillkommer hörselnedsättning i takt med att de vestibulära symtomen minskar. Hörselnedsättningen är oftast sensorineural och progredierande, och resulterar i irreversibel dövhet hos 30–50 procent av alla patienter. De okulära symtomen kan uppstå före eller efter de audiovestibulära och består i smärta, rött öga, ljuskänslighet samt nedsatt synskärpa [3]. Dessa symtom går dock oftast i total regress efter behandling. Cogans syndrom betraktas som en kronisk vaskulit som i ca 50 procent av alla fall [5] har systemiskt engagemang [4, 20]. Feber, viktnedgång, lymfadenopati, hudutslag och kardiovaskulära symtom är de mest frekvent beskrivna systemiska manifestationerna. Av allvarliga komplikationer är de kardiovaskulära mest fruktade [3]. Aortainsufficiens ses i 15 procent av alla fall, vilket kan kräva klaffoperation. Fall med mitralisinsufficens, bukaortaaneurysm och patologi i kranskärlen finns också beskrivna [5].
Diagnostik
Diagnosen är klinisk och i utredningen ingår att utesluta differentialdiagnoser. Noggrann ögonundersökning med spaltlampa av ögonspecialist, undersökning av öron-, näs- och halsspecialist samt hörseltest bör ske tidigt i förloppet. DT eller i vissa fall MR-undersökning av hjärnan hos patienter med oklara audiovestibulära symtom är viktig för att utesluta möjlig tumör, stroke eller tecken till pakymeningit [5]. Den systemiska vaskuliten kan även drabba hjärnans kärl och orsaka ischemi [21]. Det finns flera fall beskrivna där man sett labyrintitliknande kontrastuppladdningar i innerörat vid MR-undersökning [22]. I en liten studie av 3 patienter korrelerade uppladdningen i labyrinten med aktiv och inaktiv fas av sjukdomen [5].
Differentialdiagnoser som bör finnas med i utredningen är en rad autoimmuna sjukdomar som SLE (systemisk lupus erythematosus), granulomatös polyangit, IgG4-relaterad pakymeningit, primärt Sjögrens syndrom, sarkoidos och polyarteritis nodosa [3, 8, 19, 23, 24]. Laboratorietest kan visa tecken på kronisk inflammation som anemi, leukocytos, trombocytos, CRP- och SR-stegring. Provtagningen bör omfatta analys av PR3-ANCA och MPO-ANCA. I differentialdiagnostiken ingår även ett flertal infektiösa sjukdomar, och därför bör prov även tas för syfilis, borrelios, klamydia och TBE vid misstanke [2, 4, 5].
Röntgenologisk utredning, motsvarande den vid Takayasus arterit, med ultraljud, DT- eller MR-angiografi bör övervägas vid tecken på Cogans syndrom med misstanke om systemiskt engagemang.
Behandling
Prognosen förvärras avsevärt om patienten förblir obehandlad eller behandling sätts in sent [3, 4, 6]. Behandlingen ska därför initieras så snart som möjligt för att minska risken för snabb progress till blindhet och dövhet eller dödligt systemiskt engagemang [1, 2, 4, 6, 7]. I de fall där vaskuliten är begränsad och orsakar ischemi i innerörats labyrint kan en förbättring ske med endast steroidterapi i hög dos [3, 8]. Initialt bör patienten behandlas med prednisolon 1 mg/kg/dag i minst 2 veckor följt av nedtrappning över 3–6 månader [5, 6]. För den okulära inflammationen rekommenderas lokala steroider. Om patienten inte svarar kliniskt på steroider bör immunsuppresionen utvidgas [3, 5, 7, 8]. Alternativa behandlingar som använts i fallbeskrivningar men som inte har testats i randomiserade studier är till exempel cyklofosfamid, metotrexat, rituximab, azatioprin och infliximab. I en studie från 2015 beskrivs ett fall där man provat transtympaniska steroidinjektioner med framgång avseende hörsel [7]. Dessa behandlingar är olämpliga vid infektion, vilket är ytterligare en anledning att utesluta infektioner differentialdiagnostiskt före behandlingsstart [3, 8]. För patienter som utvecklar bilateral dövhet rekommenderas kokleaimplantat så snart som möjligt då innerörat med tiden blir fibrotiskt, vilket kan försvåra senare operation [25].
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Omnämnanden: Tommy Vingren, Karlstad, för bidrag med information om patientens tillstånd och avsedd behandling, och Göran Edlund, Karlstad, för information och tolkning av MR.