Tyreotoxisk kris är ett ovanligt men livshotande tillstånd som karakteriseras av hög feber, konfusion, illamående/kräkningar, takykardi/hjärtsvikt och biokemiska tecken på ökad ämnesomsättning.
Denna fallbeskrivning rör en tidigare frisk man i 30-årsåldern som insjuknade i en tyreotoxisk kris och diabetisk ketoacidos. Kombinationen är mycket ovanlig och kan försvåra diagnostiken då diabetisk ketoacidos sannolikt döljer det för tyreotoxisk kris typiska symtomet feber.
Ökad kännedom om tyreotoxisk kris och diabetisk ketoacidos förbättrar chansen till korrekt diagnos och tidigt insatt behandling, vilket i många fall kan vara livräddande.
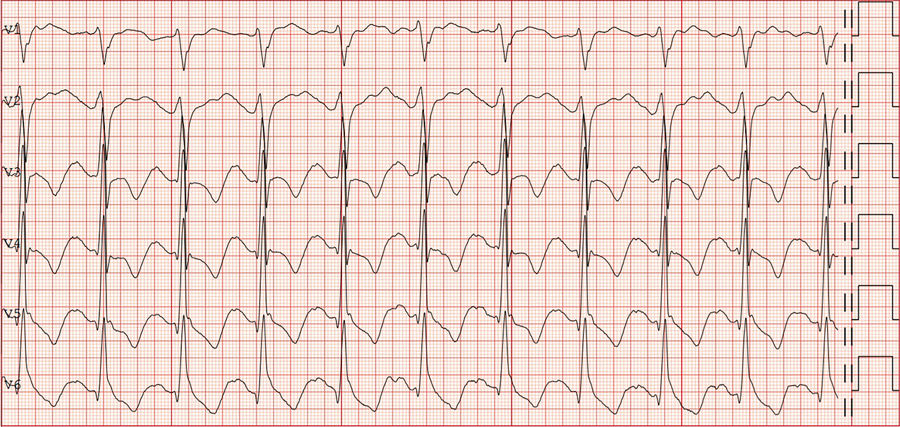
Figur 1. EKG från dag 1, utbredda ST–T-förändringar och T-inverteringar.
Fallet rör en 37-årig man som kom in i ambulans till akutmottagningen. Han hade takykardi med hjärtfrekvens 125 slag per minut och hypotoni med systoliskt blodtryck 80 mm Hg. Kussmauls andning och ketondoft noterades. Patienten var desorienterad. Hans anklar var svullna och en sårighet runt ändtarmen uppdagades. Ingen feber kunde uppmätas vid ankomst.
Vid anamnestagande från anhöriga framkom att patienten sedan tidigare var frisk; ingen anamnes på autoimmun sjukdom fanns. Patienten hade tidigare varit något överviktig men minskat ca 25 kg i vikt senaste året. Han hade haft frekventa diarréer i någon vecka och kräkningar det senaste dygnet. Inga tidigare journalanteckningar fanns.
Rutinmässigt labbstatus visade kraftig leukocytos (LPK 26 × 109/l), stegrat CRP (104 mg/l), hypokalemi (2,5 mmol/l), njursvikt (kreatinin 162 μmol/l) och metabol acidos (pH 7,06; BE [basöverskott] –26) med partiell respiratorisk kompensation (pCO2 2,1 kPa) samt kraftigt stegrat P-glukos på 32 mmol/l. Symtombilden tolkades som atypisk diabetisk ketoacidos, där hypokalemin grumlade bilden men bedömdes vara orsakad av diarréer och kräkningar. Troponin var lätt stegrat (P-hsTnT [högkänsligt troponin T] 33 ng/l), EKG visade kraftigt avvikande ST–T-sträckor och T-invertering anteriort (Figur 1) men det bedömdes som sekundärt till elektrolytrubbningen.
Patienten överfördes till intensivvårdsavdelning. Behandling av diabetisk ketoacidos med vätska, insulin- och kaliuminfusion inleddes. Patientens syra–bas- och elektrolytbalans var efter ca 12 timmar korrigerad och patienten bedömdes cirkulatoriskt stabil. Dock var han fortsatt konfusorisk, och EKG var fortsatt avvikande. En tilltagande motorisk oro och konfusion krävde sedering.
Under natten mot dag 3 drabbades patienten av hastigt påkommen respiratorisk svikt, varför han intuberades akut. Cefotaxim och erytromycin samt en engångsdos gentamicin gavs mot misstänkt pneumoni. Tilltagande cirkulatorisk påverkan medförde behov av noradrenalin, 0,2 µg/kg/minut, för att hålla det arteriella medelblodtrycket (MAP) > 65 mm Hg. Den hemodynamiska instabiliteten relaterades till septisk chock i frånvaro av annan förklaring. Labbprov visade CRP 283 mg/l och prokalcitonin 1,74 µg/l (referensvärde < 0,5 µg/l).
HsTnT steg kontinuerligt till som högst 892 ng/l. På morgonen dag 3 genomgick patienten transtorakal ekokardiografi som utföll väsentligen normalt. EKG var fortsatt patologiskt, och tilltagande generella ST-höjningar ingav misstanke om perimyokardit.
Efter 3 vårddygn sågs multipel organpåverkan trots korrigerad diabetisk ketoacidos. För att föra diagnostiken vidare fick patienten genomgå DT av hjärna, torax och buk. Undersökningen visade mindre infiltrat i höger lunga, atelektaser i vänster lunga, små mängder bukvätska, multipla lätt förstorade lymfkörtlar i buken och en prominent tyreoidea.
Patienten var under kvällen dag 3 högfebril och gravt cirkulatoriskt påverkad med stigande behov av noradrenalin. Med anledning av den radiologiskt förstorade sköldkörteln kontrollerades tyreoideastatus, som visade TSH < 0,01 mE/l (0,4–3,7 mE/l), T4 46 pmol/l (11–22 pmol/l), T3 6,0 pmol/l (3,1–6,7 pmol/l), det vill säga en bild som vid hypertyreos. Kontakt togs med endokrinolog, och diagnosen tyreotoxisk kris ställdes. Patienten ordinerades som följd av diagnosen propyltiouracil (Tiotil) i hög dos, 200 mg peroralt var fjärde timme, samt hydrokortison 100 mg 1 × 4 intravenöst. Som led i tyreotoxikosbehandlingen gjordes även försök med metoprolol intravenöst, men detta fick avbrytas på grund av tilltagande hypotension.
Under natten blev patienten ytterligare cirkulatoriskt instabil med behov av både noradrenalin, adrenalin och vasopressin. Ekokardiografiskt sågs dock normala förhållanden med ejektionsfraktion visuellt nu 50 procent. EKG-mässigt sågs tilltagande ST-höjningar, och hsTnT var över 800 ng/l. På grund av hög feber (40,0 °C) och vasoplegi påbörjades dialys. Kroppstemperaturen föll, blodtrycket steg och situationen stabiliserades något.
På förmiddagen dag 4 förvärrades patientens cirkulatoriska situation ånyo. Labbprov visade CRP 309 mg/l och prokalcitonin 167 µg/l, det vill säga kraftig förhöjt trots bredspektrumantibiotika. Ännu en transtorakal ekokardiografi genomfördes som visade tillkomst av grav vänsterkammarsvikt med synlig spontankontrast i både vänster och höger kammare och LVEF (vänsterkammarens ejektionsfraktion) på 20–30 procent. EKG visade ST-höjningar i både bröst- och extremitetsavledningar. Kontakt med toraxkirurgisk klinik togs och patienten överfördes dit för beredskap för maskinellt cirkulatoriskt stöd.
Patienten genomgick koronarangiografi som visade rena kranskärl. Förnyad ekokardiografi visade något förbättrad LVEF på 40 procent. Patienten förbättrades successivt cirkulatoriskt och respiratoriskt. Den enda odling som var positiv var från trakealsekret och visade växt av Staphylococcus aureus. Utökad provtagning visade C-peptidvärde 0,16 nmol/l (0,73–1,47 nmol/l), och då patienten var positiv för anti-GAD (glutaminsyradekarboxylas) ställdes diagnosen diabetes typ 1. TSH-receptorantikroppar (TRAK) uppmättes till 39 E/l (< 1,2 E/l) och tyreoperoxidasantikroppar (anti-TPO) till 263 kE/l (< 49 kE/l), vilket är väl förenligt med Graves sjukdom. Vasopressorstöd trappades ut och förnyad ekokardiografi visade återhämtad LVEF på 60 procent. Patienten extuberades och överfördes till medicinavdelning. Han hade då övergått till kombination av kort- och medellångverkande insulin, kortison var seponerat, substitution med levotyroxin (Levaxin) hade påbörjats och propyltiouracil i hög dos hade ersatts med tiamazol (Thacapzol) i ordinarie dos som tyreostatikum. Efter ytterligare några dagar skrevs patienten ut efter en total vårdtid om 21 dagar.
Diskussion
I efterhand får det antas att patienten redan vid ankomst hade en tyreotoxisk kris, utöver diabetisk ketoacidos. Principiellt bör tyreoideaprov inte analyseras hos kritiskt sjuka patienter beroende på hög förekomst av NTI (non-thyroidal illness). Endast vid stark misstanke om tyreoideadysfunktion rekommenderas provtagning. Patienten i fallbeskrivningen hade en stor sköldkörtel och klinisk bild som vid tyreotoxisk kris. T4 var förhöjt och T3 normalt, till skillnad från vid NTI då T3 är lågt, som en följd av minskad konversion från T4 till T3, och T4 lågt eller normalt. Vid tyreotoxisk kris, liksom vid andra hypertyreosformer, finns ingen självklar korrelation mellan klinisk bild och nivå av T4-stegring utan bedömningen är klinisk. Ett av den tyreotoxiska krisens kardinalsymtom, hög feber, har tidigare rapporterats kunna döljas av en ketoacidos [1]. I övrigt uppfylldes samtliga kriterier för tyreotoxisk kris: desorientering, gastrointestinala symtom och takykardi. I det aktuella patientfallet ställdes diagnos tyreotoxisk kris med kännedom om förstorad sköldkörtel, biokemiskt förhöjd ämnesomsättning samt typisk klinisk bild. En förväxlingsfaktor var kraftigt stegrat LPK, talande för i första hand sepsis. Ett successivt stigande prokalcitonin, i klinisk praxis i dag framför allt använt för att differentiera en bakteriell infektion från en inflammation, förvirrade bilden då det steg till mycket höga nivåer. Inga bakterier kunde dock fås att växa i blododlingar och patientens tillstånd försämrades trots tidigt insatta antibiotika. Patientens kardiogena chock samt överaktiva tyreoidea torde båda ha bidragit till de stegrade prokalcitoninnivåerna, även i frånvaro av infektion.
Diagnostik och behandling
Symtom vid tyreotoxisk kris är hög feber, rikliga svettningar, buksmärta, kräkningar och diarréer. Cirkulatoriskt ses takyarytmier, framför allt förmaksflimmer och förmaksfladder, samt en ökad risk för hypotension och cirkulationskollaps. Ökad adrenerg aktivitet föreligger, med nervositet, rastlöshet och förhöjd puls. Leverpåverkan med ikterus kan ses, liksom hyperkalcemi. Patienten kan också vara desorienterad och uppvisa psykotiska symtom, och tillståndet kan progrediera till koma. Med denna symtombild ska tyreostatikabehandling i hög dos påbörjas omedelbart. I aktuellt fall blev diagnosen något ifrågasatt vid ankomst till universitetssjukhus, varför det är intressant att retrospektivt applicera internationella diagnoskriterier på den kliniska bilden. 1983 publicerades ett poängsystem baserat på förekomst respektive gradering av dysfunktion i olika organsystem (temperaturreglering, centrala nervsystemet, gastrointestinal, lever- samt kardiovaskulär påverkan) hos patienter > 18 år med biokemisk tyreotoxikos [2]. Vid poäng > 45 enligt dessa Burch–Wartofsky-kriterier är tyreotoxisk kris högst sannolik och behandling ska därmed insättas. Patienten i det aktuella fallet erhöll ca 60 poäng. Diagnostiska kriterier har även utarbetats av Japan Thyroid Association och Japan Endocrine Society [3], och dessa är mer lättanvända än Burch–Wartofsky-kriterierna. Också enligt de japanska diagnostiska kriterierna hade den aktuella patienten en klar tyreotoxisk kris. Det essentiella kriteriet förhöjd ämnesomsättning uppfylldes, och patienten uppvisade samtliga fem symtom (CNS-påverkan, feber, takykardi, hjärtsvikt och gastrointestinala symtom), om än feber först i ett senare skede.
Fakta 1 sammanfattar de fyra huvudsakliga principerna vid tyreotoxisk kris. Hörnstenen i behandligen är hög dos av tyreostatika, där propyltiouracil 200 mg per os var fjärde timme förespråkas [4]. Tyreostatika hämmar hormonsyntesen samt minskar konvertering av T4 till T3. Vidare ges hydrokortison 100 mg intravenöst var sjätte timme för att behandla en relativ binjurebarksinsufficiens samt hämma den perifera konverteringen av T4 till T3 [5]. För att öka hormonclearance kan kolestyramin övervägas. Därutöver är allmän understödjande behandling indicerad (inte sällan intensivvård) på grund av cirkulationspåverkan (vasopressorer), takyarytmi (betablockad), feber och dehydrering. Ett högt kaloriintag eftersträvas med infusion av glukos 100 mg/ml, 1 000 ml × 2. Tiamintillskott, 100 mg, förespråkas. Slutligen är det av stor betydelse att adressera den misstänkta utlösande orsaken till den tyreotoxiska krisen för framgångsrik behandling [5].
I det aktuella fallet sattes hög dos tyreostatika samt kortison in när diagnosen aktualiserats, men patienten var då på väg in i en svårbruten cirkulationskollaps och av kardiella skäl fördes han till universitetssjukhus med beredskap för kardiell intervention. Redan vid ankomst till universitetssjukhuset hade dock tillståndet vänt. Han förbättrades successivt, fördes över till vanlig vårdavdelning där han lärde sig hantera sin diabetes och skrevs till sist hem i gott skick.
Detta fall illustrerar det dramatiska förlopp som kan ses vid tyreotoxisk kris och de differentialdiagnostiska svårigheter som kan uppstå när patienter drabbas av mer än ett sjukdomstillstånd. Att patienten en tid före det akuta insjuknandet gått ned i vikt är förenligt med debutsymtom vid både diabetes typ 1 och tyreotoxikos. Det är värt att notera att patienten drabbades av inte bara en utan två autoimmuna sjukdomar; slutligen övergick patientens obehandlade typ 1-diabetes i en ketoacidos, och möjligen är det detta som utlöser den tyreotoxiska krisen som i sin tur orsakade den akuta hjärtsvikten. Därtill kommer att patienten drabbades av pneumoni under vårdtiden, vilket sannolikt bidrog till den kliniska bilden.
Kombinationen av ovanstående symtom är ovanlig, och endast ett fåtal fall har beskrivits [6]. En viktig påminnelse är att obehandlad hypertyreos/tyreotoxikos innebär risk för övergång till livshotande tyreotoxisk kris om patienten utsätts för någon form av stress, såsom annat akut sjukdomstillstånd, trauma eller ett operativt ingrepp.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1. Behandling av tyreotoxisk kris
Hämma hormonsyntesen:
- Propyltiouracil 200 mg × 4 peroralt
Hämma hormonutsöndring:
- Lugols lösning 8 droppar × 4 peroralt (om tyreoidektomi planeras)
Blockera hormoneffekten perifert:
- Betablockad, till exempel metoprolol 0,5–1 mg × 1–8 intravenöst
- Hydrokortison 100 mg × 4 intravenöst
Öka hormonclearance:
- Kolestyramin 1–4 g × 2 peroralt



















