Troponinstegring är ett uttryck för myokardskada och ska utredas då flera underliggande orsaker är förenade med försämrad prognos.
Trots myokardskada utan signifikanta stenoser eller helt normal koronarangiografi kan det finnas underliggande ischemi.
Myokardskintigrafi kan vara otillräcklig för att påvisa ischemi och innebär en inte obetydlig mängd strålning.
Positronemissionstomografi (PET), företrädesvis med isotopen 15O-vatten, medger kvantitativ bestämning av myokardperfusion, även segmentvis, och kan påvisa mikrovaskulär dysfunktion.
Troponin är en sensitiv och specifik hjärtskademarkör [1]. Hos 5–15 procent av patienter med hjärtinfarkt ses icke-signifikanta (mindre än 50 procent lumenförträngning) eller normala kranskärl [2, 3]. Begreppet MINOCA (myocardial infarction with non-obstructive coronary arteries) används som arbetsdiagnos för denna patientgrupp. Möjliga orsaker kan vara plackruptur/erosion utan påvisbar tromb, kärlspasm, förmaksarytmi med kranskärlsemboli, inflammatorisk hjärtsjukdom, takotsubo-kardiomyopati eller mikrovaskulär dysfunktion.
Fallbeskrivning
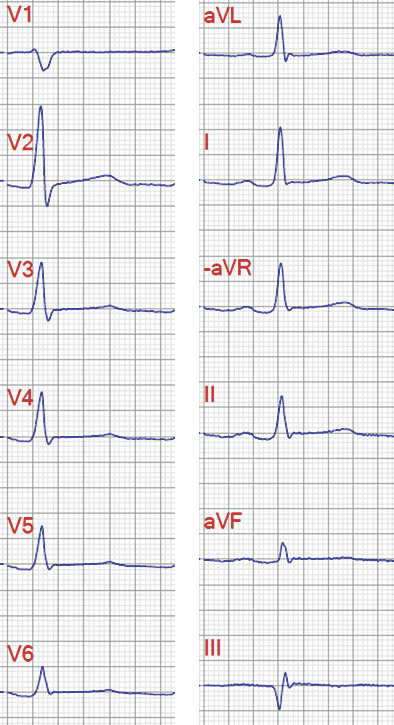
En 47-årig man inkom till akutmottagningen med fyra dygns tryckande obehag förlagt till bröstregionen med utstrålning mot vänster axel. EKG visade inferior Q-våg i avledning III samt flack T-våg i inferiora och laterala avledningar (Figur 1). Troponin T var stegrat (referensvärde < 15) med följande serie: 48–45–41–30 ng/l, och telemetri visade icke-ihållande ventrikeltakykardi. En koronarangiografi genomfördes som emellertid inte påvisade något anmärkningsvärt.
Det framkom att patienten hade flera riskfaktorer för ischemisk hjärtsjukdom. Han hade ett stillasittande arbete som chaufför, var överviktig och fysiskt inaktiv, men använde inte tobak. Sedan 5 år tillbaka behandlades han med läkemedel för hypertoni och diabetes mellitus typ 2. Hans far drabbades av hjärtinfarkt i 50-årsåldern, och modern dog plötsligt vid 64 års ålder där obduktion påvisade kranskärlssjukdom.
Mot bakgrund av multipla riskfaktorer för ischemisk hjärtsjukdom fortsatte utredningen. Vid stress-myokardskintigrafi presterade patienten 137 W, nådde en maxpuls på 146 slag/minut (betablockerare) och en antydd upptagsdefekt apikalt-septalt sågs, men någon skillnad mellan vila och arbete kunde inte påvisas. Vänsterkammarens ejektionsfraktion enligt EKG-styrd myokardskintigrafi bedömdes nedsatt, vilket också konstaterats med ekokardiografi.
Magnetkameraundersökning (MR) fem dagar efter inläggning bekräftade nedsatt ejektionsfraktion (42 procent), indexerad vänsterkammarvolym 91 ml/m2 (referensvärde 64–99 ml/m2) och diameter 59 mm medan massa bedömdes som ordinär. Några tecken till myokardit sågs inte; inget ödem, normal tidig/sen kontrastförstärkning och inget avvikande i T1/T2-mappning.
Laborativt sågs ett förhöjt fasteglukos 16,3 mmol/l, HbA1c 84 mmol/mol medan övriga prov var normala: NT-proBNP (97 ng/l), kreatinin (63 μmol/l), kolesterol (3,3 mmol/l), LDL (1,8 mmol/l), D-dimer (2,8 ng/ml) och CRP (2,8 mg/l).
I avsaknad av förklaring till stegring av hjärtskademarkörer och påverkad ejektionsfraktion trots extensiv utredning beslutades om remiss för positronemissionstomografi (PET) med spårämnet 15O-vatten inklusive adenosinbelastning. PET-undersökningen bekräftade globalt och relativt homogent nedsatt perfusion som, vid negativ koronarangiografi, utgör tecken på mikrovaskulär dysfunktion.
Patientens läkemedelsbehandling blev därefter acetylsalisylsyra 75 mg × 1, tikagrelor 90 mg × 2, metoprolol 150 mg × 1, atorvastatin 40 mg × 1, eplerenon 50 mg × 1, losartan 100 mg × 1, sitagliptin 25 mg × 1 och empagliflozin 10 mg × 1.
Diskussion
I det aktuella fallet förelåg troponinstegring konstaterad efter episod av bröstsmärta hos patient med bestickande riskprofil för kranskärlssjukdom, varför vår bedömning är att det rört sig om kranskärlsrelaterad myokardskada mot bakgrund av påvisad ischemi vid PET-undersökning samt EKG-tecken motsvarande inferiora segment. Prognosen vid akut koronart syndrom utan signifikanta stenoser är likvärdig som för de med signifikanta stenoser efter justering för riskfaktorer (9 procent drabbades inom 2 år av död, hjärtinfarkt eller stroke) [4].
Kontrastförstärkt MR kan möjliggöra differentialdiagnostik mellan hjärtinfarkt och myokardit eller kardiomyopati. Sensitiviteten för att påvisa nekros/fibros hos patienter med hjärtinfarkt och patologisk kranskärlsröntgen är cirka 95 procent och har medfört prioriteringen 8 (av 10) i Socialstyrelsens nationella riktlinjer för hjärtsjukvård [5].
Europeiska hjärtförbundet (ESC) har inga särskilda rekommendationer i sina riktlinjer avseende utredning med myokardskintigrafi eller PET av patienter med hjärtinfarkt utan signifikanta stenoser [1, 6]. Trots detta gjordes myokardskintigrafi i det aktuella fallet.
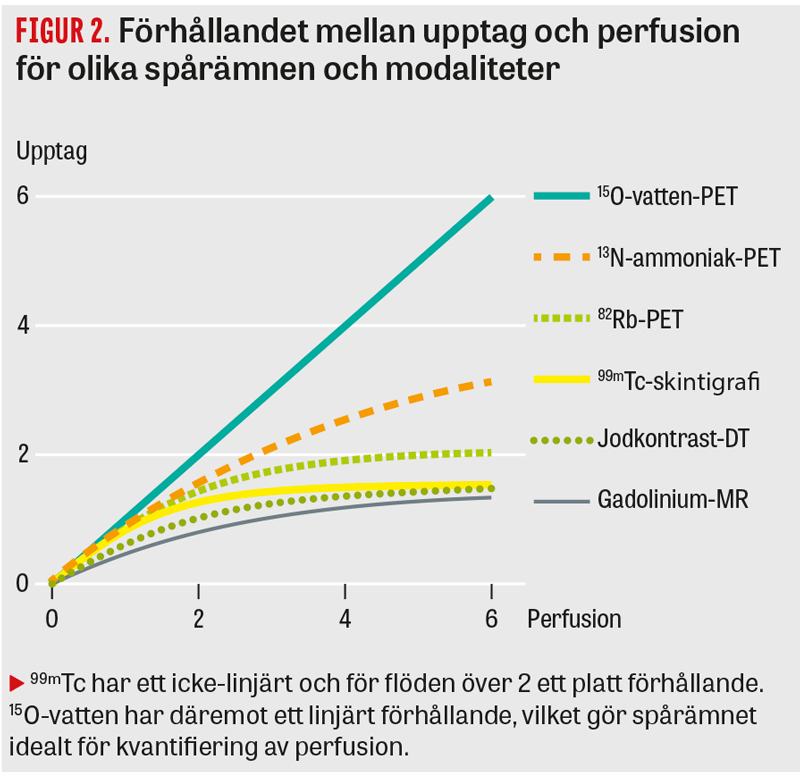
Myokardskintigrafi är en teknik där man använder sig av radioaktiva spårämnen, vanligen teknetium-99m,99mTc-sestamibi eller 99mTc-tetrofosmin. Spårämnets upptag och retention i myokardiet ger kontrast till omkringliggande vävnad och möjliggör visualisering i form av upptagsbilder. Bilderna rekonstrueras till en relativ färgskala som normaliseras mot området med det högsta upptaget. Därmed detekteras perfusionsdefekter endast om de skiljer sig signifikant i upptag jämfört med det högsta upptaget som bilden normeras mot. Det är anledningen till att det med myokardskintigrafi är svårt att detektera mikrovaskulär dysfunktion, som ofta visar på en global och homogen minskning av perfusionen med en otillräcklig skillnad mellan det högsta och lägsta upptaget. De spårämnen som används vid myokardskintigrafi har dessutom ett icke-linjärt och ganska platt förhållande mellan upptag och perfusion (Figur 2). Detta leder till att skillnaden i upptag mellan olika flöden inte blir så stor, vilket ytterligare försvårar detektionen.
15O-vatten
Med PET går det i stället att utföra dynamiska undersökningar och mäta aktivitetsfördelningen av spårämnet över tid. Från den dynamiska undersökningen kan man sedan med kinetisk modellering kvantifiera perfusionen i absoluta värden, vilket görs med automatiserade mjukvaror. 15O-vatten är ett metabolt inert spårämne som diffunderar fritt över cellmembran och har ett linjärt förhållande mellan upptag och perfusion (Figur 2). 15O-vatten är därför ett utmärkt spårämne för kvantifiering av perfusion, och PET med 15O-vatten är i dag bästa referensmetod för icke-invasiv kvantifiering av perfusion i hjärtat. Med en kvantifierad absolut skala ses om patienten har en global och homogen försämring i perfusion som är beroende av signifikant skillnad mellan det högsta och lägsta upptaget. Att 15O-vatten har ett linjärt förhållande mellan perfusion och upptag gör också att det är lättare att upptäcka tidigare förändringar än när man använder 99mTc (Figur 2).
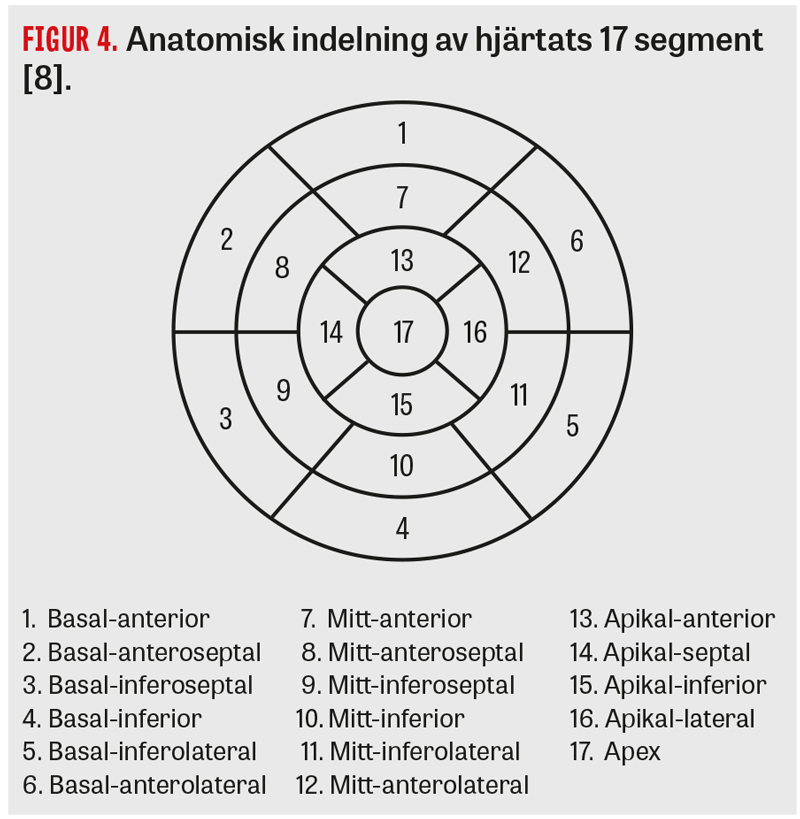
Vid PET med 15O-vatten ligger perfusionen i hjärtat hos en frisk person utan riskfaktorer kring 4 ml/g/min vid adenosin-inducerad stress och kring 1 ml/g/min i vila. Gränsen för signifikant perfusionsreduktion förenlig med ischemi ligger på 2,3 ml/g/min för stress, vilket är oberoende av vilken PET-kamera som används och reproducerbart i kliniska prövningar [7, 8]. Vår patient hade en globalt nedsatt perfusion till 2,45 ml/g/min under stress, alltså nära gränsen för ischemi. Hela inferiora väggen ligger på 1,95 ml/g/min och basal-anteriort och anteroseptalt 1,90 ml/g/min, det vill säga under gränsen för ischemi.
Figur 3 visar diagram med perfusionsfördelningen i vila och stress och i Figur 4 ses en beskrivning av 17-segmentmodellen som diagrammen är uppdelade i [9]. Det högsta segmentet ligger på 2,99 ml/g/min och det lägsta på 1,88 ml/g/min med en differens av 1,11 ml/g/min som alltså myokardskintigrafi inte kunnat urskilja.
Lägre stråldos med 15O-vatten
Nackdelen med PET är den begränsade tillgängligheten, speciellt avseende 15O-vatten som spårämne. Det kräver då en cyklotron där spårämnet skapas, som måste ligga i nära anslutning till PET-kameran då halveringstiden är 2 minuter. Rubidium-82 (82Rb) är det spårämne som används mest för perfusionsmätning med PET, då det elueras från en generator och inte kräver en cyklotron på plats. Nackdelen med 82Rb är dock det icke-linjära förhållandet mellan perfusion och upptag, vilket försvårar kvantifieringen och gör det svårare att skilja mellan subtila förändringar kring gränsvärdet för ischemi samt den höga kostnaden.
Stråldosen för PET med 15O-vatten är cirka 1 mSv, medan den för myokardskintigrafi är cirka 8 mSv. Från strålskyddssynpunkt är alltså 15O-vatten-PET att föredra framför myokardskintigrafi. Sensitiviteten för myokardskintigrafi är för låg vid frågeställningen mikrovaskulär dysfunktion och kan då medföra onödig strålning. MR-hjärta med förstapassageperfusion delar myokardskintigrafins tillkortakommande med en icke-kvantitativ bedömning. Kvantifiering av perfusion med MR är ett intressant alternativ, men metoden har än så länge inte nått tillräcklig överensstämmelse med bästa referensmetod (15O-vatten-PET).
Tillgängligheten för myokardiskintigrafi är betydligt högre än för PET och kostnaderna är lägre. I det aktuella fallet fakturerades remitterande klinik 12 010 kronor för PET-undersökningen. Kunskapen om myokardskintigrafins svårigheter med att detektera mikrovaskulär dysfunktion är därför viktig då en patient med den frågeställningen bör remitteras till ett sjukhus där kvantitativ PET kan utföras. För ett bredare införande av metoden bör dock prospektiva studier genomföras och värderas.
Potentiella bindningar eller jävsförhållanden: Peter Magnusson har erhållit föreläsararvoden från Abbott, Alnylam, Boehringer Ingelheim, Medtronic, Novo Nordisk och Pfizer. Mark Lubberink har erhållit föreläsararvoden och forskningsstöd från GE Healthcare. Jens Sörensen och Mark Lubberink är medgrundare av Medtrace Pharma AS, som utvecklar aQuant-mjukvaran för kvantifiering av hjärtperfusion med 15O-vatten och PET.