Dystrophia myotonica typ 1 är en sällsynt men viktig differentialdiagnos vid bradykardi hos unga.
Framför allt anses höggradigt atrioventrikulärt block II–III orsaka synkope, men det kan även orsakas av sinusarrest, vilket denna fallbeskrivning visar.
Dödligheten vid dystrophia myotonica typ 1 är 7 gånger högre än hos normalbefolkningen, och plötslig död står för mer än en tredjedel av dödsfallen.
Livshotande ventrikulära arytmier förekommer, och vid nedsatt systolisk vänsterkammarfunktion bör indikation för primärpreventiv implanterbar kardiell defibrillator värderas.
Samtliga patienter med dystrophia myotonica typ 1 bör årligen genomgå klinisk bedömning och utredning med 12-avlednings-EKG, 24-timmars Holter-EKG och ekokardiografi.
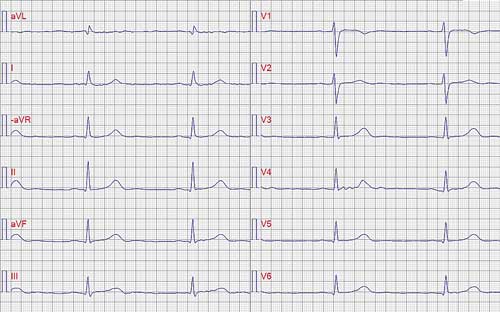
Figur 1. Vid ankomsten till akutmottagningen visade 12-avlednings-EKG sinusrytm med 60 slag/minut.
Synkope hos unga har oftast en godartad underliggande orsak; dock har en liten andel en potentiellt livshotande genes såsom kardiell synkope. Bradykardi vid högre ålder orsakas ofta av åldersrelaterad retledningsfibros, medan annan underliggande sjukdom ska misstänkas hos yngre patienter. Under 2017 gjordes i Sverige 101 nyimplantationer av pacemaker på grund av bradykardi hos patienter under 40 år, endast 1,5 procent av alla nyimplantationer [1].
Denna artikel beskriver en ung kvinna med upprepade synkopeepisoder, där orsaken var en sjuk sinusknuta till följd av en tidigare odiagnostiserad neuromuskulär sjukdom.
Fallbeskrivning
En 24-årig kvinna sökte akutmottagningen efter att ha svimmat tre gånger under samma dygn: på morgonen i samband med tandborstning, på vårdcentralen och i bilen på väg till akutmottagningen. Hon hade även i tonåren svimmat vid två tillfällen. Patienten hade fötts för tidigt och vårdats på sjukhus de första 4 månaderna, men hade i övrigt inga kända sjukdomar.
Det faktum att svimningarna skedde utan förvarning eller eftersymtom gjorde att kardiell genes kunde misstänkas [2]. EKG på akutmottagningen var dock normalt (Figur 1). Ortostatiskt prov var utan anmärkning, och anamnesen tydde inte på ortostatism. Telemetri på hjärtavdelningen påvisade bradykardiepisoder med hjärtfrekvens ner till 30 slag per minut samt sinusarrester med RR-intervall på uppemot 6,5 sekunder.
För att utreda annan genes till medvetandeförlusten utfördes EEG, som påvisade mindre epileptogen aktivitet vid ytlig sömn, vilken bedömdes vara ospecifik. Datortomografi av hjärnan visade inget avvikande, och MRT av hjärnan visade förändringar som bedömdes vara förenliga med prematur födsel.
Patienten erhöll en DDDR-pacemaker (dual pacing, dual sensing, dual response, rate-responsive) på grund av upprepade svimningar och dokumenterad sinusarrest. Implantationen visade fullgoda mätvärden. Den till storleken minsta pacemakern valdes, eftersom området för dosfickan uppvisade mycket lite underhudsfett och tunna muskelskikt.
Under vårdtiden noterades att patienten inte kunde räta ut sina fingrar ordentligt efter att hon greppat föremål. En remiss skickades därför till neurologkonsult, som kunde verifiera att patienten hade svårt att släppa taget då de skakat hand och att ansiktsmuskulaturen var påtagligt tunn. Patienten själv upplevde inga problem med generell muskelsvaghet men medgav besvär från händerna. I släkten fanns ingen känd ärftlig sjukdom och ingen i familjen hade liknande symtom som patienten.
Lumbalpunktion med likvorprovtagning utfördes utan tecken till borrelios. På misstanke om möjlig muskelsjukdom utfördes EMG, som visade uttalad myotoni men ingen dystrofi. Genetisk utredning påvisade patologiska CTG-expansioner på kromosom 19 omfattande 100 repetitioner, vilket bekräftade diagnosen dystrophia myotonica typ 1 (Steinerts sjukdom).
Efter pacemakerimplantationen upphörde synkopeepisoderna. Vid avläsning av pacemakern konstaterades 12 procent stimulering i förmaket och mindre än 1 procent kammarstimulering. Upprepade ekokardiografiundersökningar var invändningsfria. MRT av hjärtat visade normala förhållanden. Blodprov inklusive tyreoideaprofil och NT-proBNP (N-terminalen av prohormonet till BNP [natriuretisk peptid av B-typ]) (28 ng/l) var utan anmärkning.
Diskussion
Sinusbradykardi eller atrioventrikulärt (AV)-block II typ 1 (Wenckebach-fenomen) utan symtom är vanligt förekommande hos vältränade unga och vanligtvis enbart ett uttryck för parasympatikustonus [3].
Bradykardi hos unga kan även orsakas av bl a hypotyreos, läkemedel, hyperkalemi, borrelios, dysfunktion av autonoma nervsystemet, inlagringssjukdomar som amyloidos eller hemokromatos, autoimmuna sjukdomar som systemisk lupus erythematosus, medfödda hjärtfel, anorexia nervosa, iatrogena skador på retledningssystemet i samband med hjärtkirurgi/kateterablation och neuromuskulära sjukdomar [4].
Dystrophia myotonica typ 1 är den vanligaste formen av muskeldystrofi hos vuxna med en incidens på 1/8 000 födda [5]. Sjukdomen medför bl a varierande grad av muskeldystrofi, myotoni och katarakt, men den kan även påverka hjärtat, hormonproducerande körtlar och kognitiva funktioner [6].
Dystrophia myotonica typ 1 orsakas av en mutation i genen DMPK på kromosom 19 (19q13.2-q13.3), som kodar för proteinet dystrophia myotonica-proteinkinas [7]. Vid dystrophia myotonica typ 1 är antalet kopior av DNA-sekvensen CTG ökad, vilket ger instabilitet och innebär att ytterligare påbyggnad av antalet kopior kan ske när genen nedärvs [7]. Dystrophia myotonica nedärvs autosomalt dominant med antecipation, och det finns stora variationer vad gäller såväl vid vilken ålder sjukdomen ger symtom som dess utbredning och svårighetsgrad [6].
Hjärtpåverkan
De flesta patienter med dystrophia myotonica typ 1 får hjärtaffektion; hur stor andel är svårt att uppskatta eftersom många är symtomfria. Vanligast är rytmrubbningar såsom AV-blockering eller grenblock. Omkring 65 procent av patienterna har avvikande EKG [8]. I en metaanalys av 18 studier omfattande 1 828 patienter med dystrophia myotonica uppvisade 28 procent AV-block I, 22 procent förlängd QTc-tid (korrigerad QT-tid) och 14 procent frekventa ventrikulära extraslag, medan förmaksflimmer/-fladder, grenblock och ventrikeltakykardi förekom hos ca 5 procent [9].
Vår patient hade sinusarrest, mest sannolikt till följd av dystrophia myotonica typ 1. Detta är ovanligt, men styrks av att patienten hade 12 procent förmaksstimulering, ingen ventrikulär stimulering och att ingen annan förklaring till sjuk sinusknuta framkommit under uppföljningen [10].
I en artikel där 300 patienter med dystrophia myotonica undersökts uppvisade bara 1 patient sinusbradykardi [11]. Av 81 patienter (medelålder 29,9 år) med dystrophia myotonica typ 1 i en retrospektiv observationsstudie hade 13,8 procent dysfunktion av sinusnoden efter en medeluppföljningstid på 5,7 år [12].
I en studie av 49 patienter (medelålder 45,5 år) med dystrophia myotonica typ 1, vilka vid elektrofysiologisk undersökning hade tecken på förlängd överledning i AV-noden (His–ventrikulärt intervall ≥70 ms) uppvisade 42,9 procent AV-block III, medan 8,2 procent uppvisade sinoatriellt block vid pacemakeravläsning efter medeluppföljningstid på 4,5 år [13].
Den bakomliggande patologin som orsakar hjärtbesvär är fibros och fettinfiltration i hjärtmuskulaturen, vilket drabbar retledningssystemet och orsakar ledningsblock, ektopisk aktivitet och återkommande arytmier med symtom som hjärtklappning, synkope och plötslig hjärtdöd [14]. Vid en 10-årsuppföljning av patienter med dystrophia myotonica typ 1 var medellivslängden 53 år och mortaliteten 7,3 gånger den hos den friska kontrollgruppen [15].
Dödsorsaken är respiratorisk svikt i ca 40 procent av fallen och kardiell i 30 procent av fallen [7, 15, 16]. Bradyarytmi med asystoli eller bradykardiinducerad ventrikeltakykardi anses vara huvudorsaken till plötslig hjärtdöd hos patienter med dystrophia myotonica [8]. Då patienter med symtomgivande bradykardi erhållit pacemaker har man även sett fall av ventrikeltakykardi som orsakat plötslig död [5, 9]. Män, äldre och patienter med mer uttalad muskelsjukdom har högre risk för både bradyarytmi och ventrikulär takyarytmi [17].
Antalet CTG-repetitioner korrelerar med ökad risk för plötslig död, retledningsdefekter, vänsterkammardysfunktion och supraventrikulära arytmier [18].
Pacemakerbehandling
Det finns ett generellt stöd för tidig behandling med pacemaker till patienter med dystrophia myotonica och påverkan på retledningssystemet [14]. Pacemaker ska övervägas till patienter med AV-block II och III eller sjuk sinusknuta [4, 3, 14]. Vissa studier indikerar att profylaktisk implantation av pacemaker hos patienter med sjukdomen och högriskfaktorer kan vara gynnsam.
I en retrospektiv studie var överlevnaden högre hos dem med tecken på fördröjd retledning (PQ-tid >200 ms eller QRS-duration >100 ms) som genomgick elektrofysiologisk undersökning och erhöll pacemaker om His–ventrikulärt intervall var >70 ms än hos dem som inte genomgick elektrofysiologisk undersökning [19]. Den kliniska relevansen av detta är dock inte fastställd och det saknas randomiserade prövningar.
För patienter som överlevt hjärtstillestånd eller ventrikeltakykardi med hemodynamisk påverkan är implanterbar kardiell defibrillator (ICD) indicerad. Primärpreventiv ICD ska övervägas vid nedsatt ejektionsfraktion (≤35 procent) trots 3 månader med optimal medicinsk behandling [3, 4, 14].
Sammanfattning
Vid bradykardi hos unga personer bör dystrophia myotonica typ 1 finnas med i de differentialdiagnostiska övervägandena. Vanligtvis manifesterar sig bradykardin som höggradigt AV-block. Vårt fall illustrerar dock att sjuk sinusknuta med synkope också förekommer.
Det är värdefullt att vara observant på tecken till muskeldystrofi hos dessa patienter, och det kan vara motiverat med ytterligare utredning inklusive genetisk testning. Samtliga patienter med dystrophia myotonica typ 1 bör årligen genomgå klinisk bedömning, 12-avlednings EKG, 24-timmars Holter-EKG och ekokardiografi [5].
Plötslig död förekommer till följd av såväl bradykardi som ventrikeltakykardi men också hjärtsvikt, varför samverkan mellan neurolog, kardiolog och klinisk genetiker samt återkommande uppföljning är värdefullt.
Potentiella bindningar eller jävsförhållanden: Peter Magnusson har erhållit föreläsararvoden från Abbott, Alnylam, Bayer, Boehringer Ingelheim, Medtronic, Novo Nordisk och Pfizer.



















