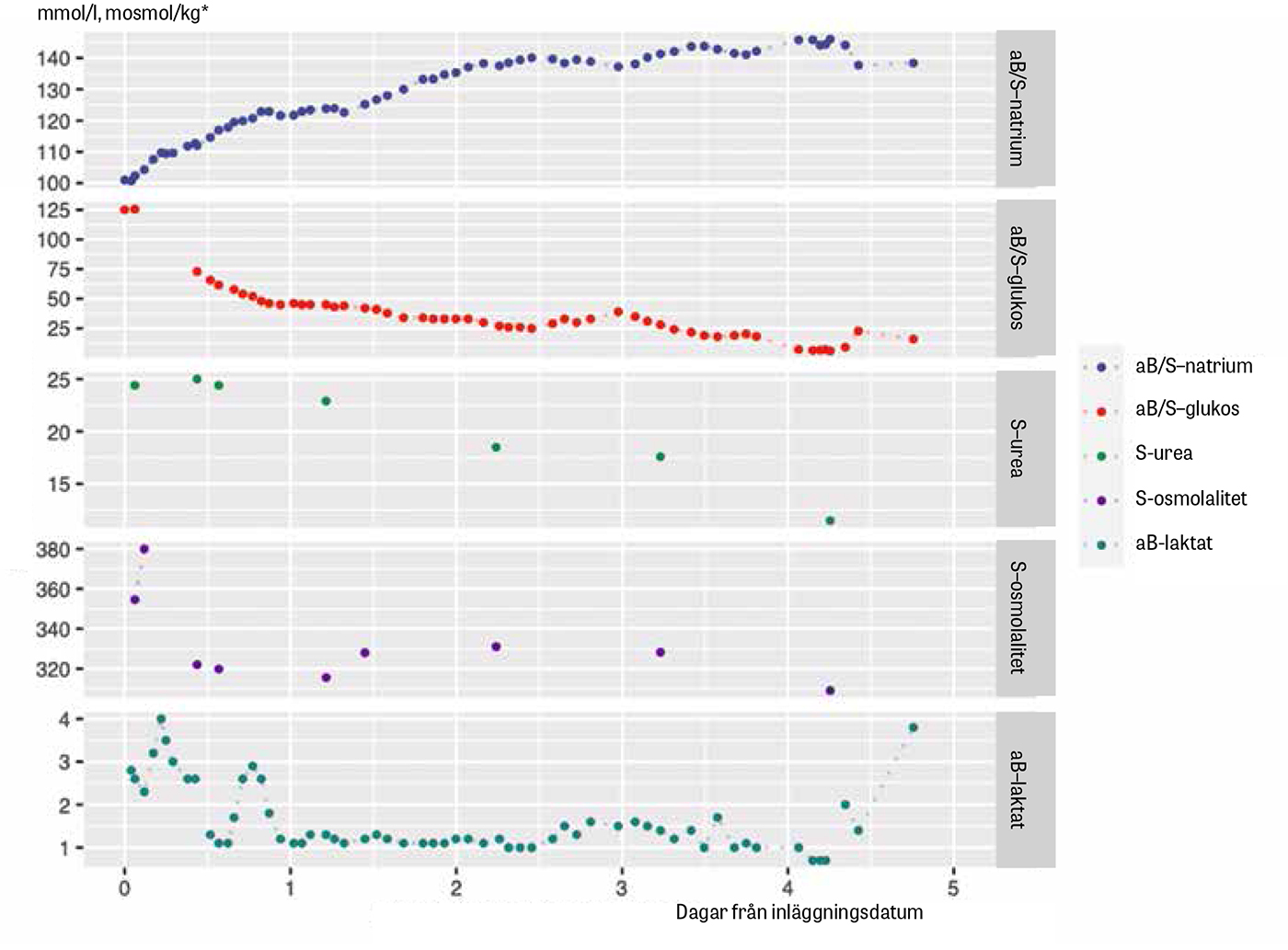
Fallet belyser en patient med extrem hyperglykemi med kompensatorisk hyponatremi och den kliniska utmaningen som samtidig hyperglykemi medför vid bedömningen av natriumnivåer, speciellt vid uttalade rubbningar.
Det finns flera modeller för att uppskatta förväntad hyponatremi vid hyperglykemi, men det vetenskapliga underlaget är begränsat vid extrema värden.
Snabba skiften i osmolalitet vid hyperosmolärt non-ketotiskt syndrom (HNKS) kan medföra risk för cerebralt ödem. Det kan vara svårt att kontrollera korrigeringstakten av natrium och glukos vid uttalat förhöjda glukosnivåer.
Fallbeskrivning. Fallet rör en man i 70-årsåldern som inkom som ett prio 1-larm nattetid i ambulans till akutmottagningen på grund av sänkt medvetandegrad. Ur journalen kunde utläsas en känd diabetes mellitus typ 2 med senaste HbA1c 74 mmol/mol, flera års bristfällig glukoskontroll och komplikationer i form av bland annat njursvikt med estimerad GFR på 31 ml/min × 1,73 m2. Patienten behandlades med insulin, GLP-1 (glukagonlik peptid 1)-analog samt metformin. Två veckor före insjuknandet hade tiaziddiuretika satts ut och metformindosen halverats till 500 mg × 1 på grund av successivt försämrad njurfunktion. Patienten hade även betametason i nedtrappning för en kryptogen organiserad pneumoni (COP).
Patienten hade varit trött en längre tid och sängliggande i tre dagar av okänd anledning. Dagen för ankomst till sjukhus hade patienten blivit mer och mer svårkontaktbar men hade vid lunchtid varit talbar. Det fanns inga uppgifter om kramper. Ambulanspersonalen fann patienten i hans säng, men patienten hade kunnat förflytta sig till ambulansen med hjälp av levande stöd. Pulsoximeter visade perifer saturation på 88 procent. Glukosmätaren i ambulansen visade »high« vid kapillär provtagning.
På akutmottagningen var patienten somnolent, reagerade ej på tilltal och hade snarkande andning med en perifer saturation på 72 procent på luft. Detta förbättrades till 90 procent med tillförsel av syrgas och käklyft. Patienten var afebril med fluktuerande vakenhetsgrad på akutrummet, och han var motoriskt orolig. Andningsljuden var normala, med andningsfrekvens 20–25 per minut. Blodtrycket uppmättes till 168/83 mm Hg. Palpatoriskt förelåg en diffus ömhet i buken. Pupillerna var isokora, normalvida och reagerade på ljus; inga fokalneurologiska symtom noterades. EKG visade sinusrytm med frekvens 91 slag/minut och breddökade QRS-komplex på 130 ms.
Venösa blodprov visade kraftig hyperglykemi med S-glukos på 125,6 mmol/l, hyponatremi med S-natrium på 101 mmol/l, hyperkalemi på 5,9 mmol/l och kreatininstegring till 285 µmol/l från habituellt kring 160 µmol/l. Den arteriella blodgasen visade metabol acidos med pH på 7,24 och ett basöverskott på –10,4 mmol/l. Hb var 91 g/l.
Patienten togs till intensivvårdsavdelningen (IVA), där kompletterande prov visade S-osmolalitet 380 mosmol/kg, U-osmolalitet 148 mosmol/kg och U-Na på 20 mmol/l. Patienten bedömdes vara euvolem efter ultraljudsundersökning av hjärta och centrala kärl, men proven talade för dehydrering. B-ketoner var 0,8 mmol/l.
På IVA var patienten motoriskt orolig och sederades med propofol och dexmedetomedin. Patienten utvecklade feber utan tydlig klinisk fokalitet. S-CRP var följande morgon 28 mg/l, prokalcitonin 6,9 µg/l, B-leukocyter 14,3 × 109/l. Lungröntgen visade ett mindre infiltrat och patienten ordinerades cefotaxim och erytromycin på misstanke om atypisk pneumoni.
Osäkerhet kring en lämplig korrigeringstakt gjorde att patienten initialt behandlades med långsam korrigering av natriumnivåerna enligt vårdprogrammet för kronisk hyponatremi från Svensk förening för anestesi och intensivvård [1]. För att sänka plasmaglukos, häva acidemin och sänka hyperosmolariteten startades en insulininfusion med starttakt 0,5 IE/kg/timme och mål om korrigering med 4 mmol/timme. I takt med att plasmaglukos sjönk steg S-natrium snabbare än önskat, varför man tillförde elektrolytfria vätskor intravenöst och via sond. Detta för att undvika en för snabb korrigering. Korrigeringen av patientens elektrolyter försvårades av en polyurisk fas med urinmängder på >8 l redan under första dygnet. En högre ökningstakt för natrium kunde senare accepteras, då det fastslogs att det rörde sig om enbart en kompensatorisk hyponatremi. Behandlingen kunde därefter styras efter osmolalitet och glukosnivåer.
Med tanke på kortisonbehandlingen i kombination med hyponatremin och hyperkalemin sattes hydrokortison in som behandling för eventuell iatrogen binjurebarksvikt. Detta trappades ut efter svar på kortisol och ACTH.
Patientens elektrolyter, osmolalitet och glukosnivåer korrigerades framgångsrikt och kreatininstegringen gick spontant i regress. Inga neurologiska sekvele noterades. Efter 10 dagars vårdtid, varav 5 dagar på IVA, skrevs patienten ut till hemmet och blev inom kort helt återställd.
Vid uppföljning två månader efter utskrivning mådde patienten fortsatt väl. Medicineringen var oförändrad frånsett att kortisonbehandlingen kunnat avslutas. Det framkom att patienten hade feltolkat nedtrappningsschemat av betametason för sin COP och fortsatt ta 2 mg dagligen fram till insjuknandet. Flera faktorer, såsom hög kortisondos, minskad dos metformin, dålig följsamhet till insulinbehandlingen samt en nedre luftvägsinfektion tros ha samverkat och resulterat i den extrema hyperglykemin.
Diskussion
Det är känt sedan länge att hyperglykemi kan leda till kompensatorisk hyponatremi [2]. Glukos är osmotiskt aktivt, vilket leder till en ökad serumosmolalitet, vätskeutträde från cellerna och hyponatremi till följd av utspädningen [3]. Kliniskt är det dock vanligt att en kompensatorisk hyponatremi, som i fallet ovan, initialt leder till osäkerhet och bedöms som en reell hyponatremi. Beräkning av korrigerat natrium och kontroll av osmolalitet är viktig, och förhöjd osmolalitet styrker att det rör sig om en kompensatorisk hyponatremi.
Katz publicerade 1973 en korrigeringsfaktor för natrium som länge var allmänt accepterad [4]. Flera studier har följt, och i dag är Hilliers korrigeringsfaktor (Fakta 1) mest etablerad [5-7]. Ingen av formlerna är testade för så uttalat stegrade glukosvärden som i det här fallet, och Hillier själv påpekar att sambandet inte är linjärt och att korrigeringsfaktorn därmed är svårvärderad vid uttalat förhöjda nivåer [7]. I vårt fall fås ett korrigerat natrium på 135 mmol/l (Katz) respektive 152 mmol/l (Hillier), vilket talar mot en signifikant reell hyponatremi.
Hyperglykemin, hyperosmolaliteten och avsaknaden av ketoner tyder på att patienten drabbats av hyperosmolärt non-ketotiskt syndrom (HNKS), ett allvarligt tillstånd med en mortalitet på upp till 60 procent [8,9]. Riklig vätsketillförsel i form av 0,9 procent NaCl-lösning eller Ringeracetat rekommenderas, vilket kommer att leda till att blodsockernivåerna går ned. Vid 5,5 mmol/l minskning av glukos kommer också natrium att stiga med 2,4 mmol/l, och en stegring är alltså förväntad. Om osmolaliteten inte sjunker som förväntat kan man övergå till hypotona lösningar. Lämplig korrigeringsnivå är 3–8 mosmol/kg/timme, och osmolaliteten bör därför initialt kontrolleras tätt. Målsättningen bör vara att blodsockret sjunker med 4–6 mmol/timme till en slutnivå på 10–15 mmol/l. Ett riktmärke är att hälften av vätskebehovet ska gå in under de första 12 timmarna, men givetvis bör bakomliggande sjuklighet vägas in. Insulin bör endast övervägas då glukossänkningen avstannat och då ges i lågdos, 0,05–0,1 IE/kg/timme [9, 10].
I det här fallet försvårades möjligheten att reglera korrigeringstakten, då blodgasapparaten inte kunde analysera så pass förhöjda glukosvärden. Man begränsades till venös provtagning med medföljande fördröjning av provsvar.
Vi har inte funnit någon rapport om att en patient med sådan extrem hyperglykemi vårdats inom svensk sjukvård. Vi har även sökt på Pubmed utan att finna någon publicerad rapport med lika högt eller högre blodglukos hos någon patient vårdad internationellt. I en fallrapport från 2017 beskrevs att en kvinnlig patient från Asien med diabetes typ 2 haft blodglukos på 110,2 mmol/l [11]. Guinness rekordbok anger att det högsta blodglukosvärdet uppmätts hos Michael Patrick Buonocore, en amerikansk 7-årig pojke som 2008 vårdades på sjukhus i Pennsylvania med 147,6 mmol/l [12].
Sammanfattningsvis finns formler för att beräkna förväntade natriumnivåer vid hyperglykemi. De studier som gjorts har dock utförts på lägre glukosnivåer, och patientfallen är ovanliga. Principer för rekommenderad korrigeringstakt avseende hyperglykemi vid HNKS finns beskrivna. Vårt fall belyser en patient med kraftig metabol rubbning i form av uttalad hyperglykemi, hyperosmolalitet och kompensatorisk hyponatremi som framgångsrikt korrigerades genom normalisering av glukosnivåerna medelst tillförsel av vätska och insulin.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1.
Beräkning av justerat natriumvärde:
Justerat natrium (Hillier) = uppmätt natriumvärde + 2,4 × [(uppmätt glukosvärde – 5,6) / 5,6]
Beräkning av osmolalitet:
Osmolalitet = 2 × natrium + glukos (+ urea)
Samtliga värden i mmol/l. Källor [7, 9]