Diabetisk ketoacidos drabbar ca 1 procent av patienterna som behandlas med PD-1-hämmare.
Insjuknandet är oftast akut, och regelbunden provtagning fångar inte upp alla patienter med PD-1-hämmarbehandling som insjuknar i ketoacidos.
Det är i nuläget oklart om patientutbildning tillsammans med möjlighet att själv kunna mäta blodsocker i hemmet kan reducera insjuknandet i diabetisk ketoacidos.
Under livets gång kommer många att utveckla cancer; däremot har mortaliteten över tid generellt gått ned, till stor del på grund av förbättrade behandlingsmöjligheter. Immunkontrollpunktshämmare är ett av de modernare behandlingsalternativen mot cancer. Dessa mediciner ökar överlevnaden vid flertalet cancersorter. De förväntas användas i allt större utsträckning och på fler indikationer [1].
Flera immunkontrollpunktshämmare har identifierats, bland annat CTLA-4 (cytotoxiskt T-lymfocytantigen 4), PD-1 (programmerad celldödreceptor 1) samt PD-L1 (liganden för PD-1) [2].
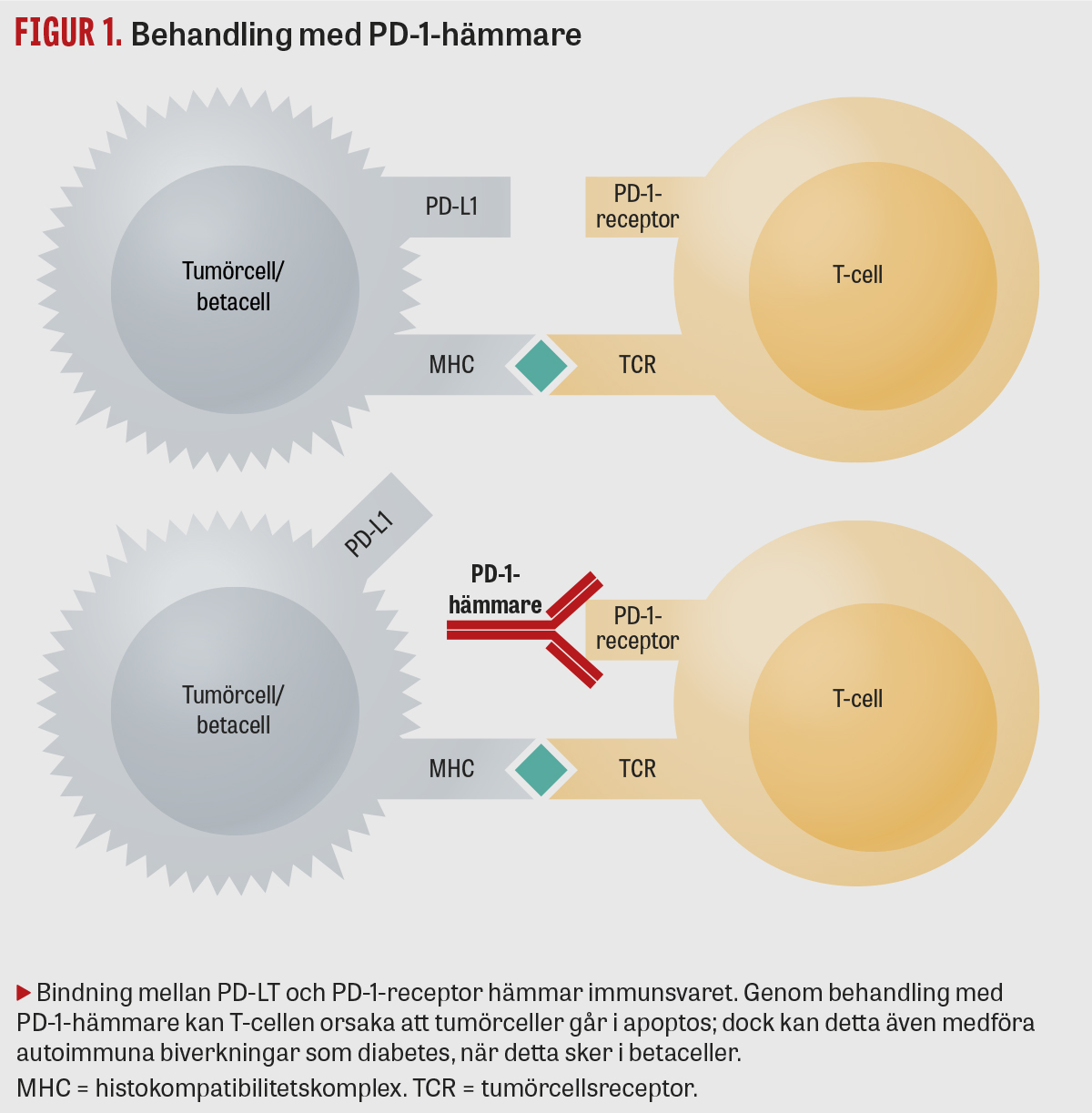
PD-1-receptorn uttrycks på ytan av aktiva T-celler, och när PD-1 binder till PD-L1 genereras en inhibitorisk signal som reglerar T-cellsaktivitet och dämpar immunsvaret. Genom att hämma PD-1 kan man således återställa funktionen och på så vis behandla tumörer som själva uttrycker PD-L1 och utlösa celldöd. Som en biverkan kan dock autoreaktiva T-celler överleva och orsaka cytotoxiska biverkningar [2]. Några vanliga biverkningar utgörs således av hudutslag av varierande karaktär, klåda, pneumonit eller kolitbild med bland annat neutrofila kryptabscesser och epitelial cellapoptos [3, 4]. Vissa studier har visat på bättre behandlingssvar om patienterna drabbas av lindrigare immunrelaterade biverkningar såsom hudutslag.
Patienter kan även drabbas av endokrinologiska biverkningar [5]; bland annat har man sett hypofysiter, tyreoiditer samt diabetes typ 1 [4, 6, 7]. Utveckling av snabbt påkommen insulinkrävande diabetes är en sällsynt, om än känd, biverkan. Incidensen av denna har noterats vara runt 1 procent [8].
Det verkar också finnas en koppling mellan PD-1 och diabetes även utan behandling, då en studie påvisat minskat PD-1-uttryck i T-celler hos personer med typ 1-diabetes jämfört med friska individer [9].
Betaceller i pankreas uttrycker PD-L1, och när man startar behandling med PD-1-hämmare fungerar således inte PD-1–PD-L1-signaleringen och hämning av autoreaktiva T-celler sker ej. Autoreaktiva T-celler kan då förstöra betacellerna och orsaka insulinkrävande diabetes [4, 7] (Figur 1). Insulinkrävande diabetes verkar även vara vanligare vid behandling med PD-1-hämmare än med immunkontrollpunktshämmare av typen anti-CTLA-4 [10]. Insulinkrävande diabetes är en sällsynt biverkan, där tidigare studier visat en incidens på 0,6–1,9 procent [7, 11].
Nivolumab är en av dessa immunkontrollpunktshämmare. Det är en IgG4-monoklonal antikropp som binder till PD-1-receptorn och hämmar dess effekt. Detta leder till ett förstärkt T-cellssvar och ger en antitumoral effekt. Nivolumab är för närvarande indicerat som behandling av avancerat melanom hos vuxna. Indikation föreligger även vid bland annat icke-småcellig lungcancer, pleuramesoteliom, Hodgkinlymfom samt vissa gastrointestinala maligniteter. Studier har visat god effekt på malignt melanom, där man sett ökad återfallsfri överlevnad [12, 13].
Vi beskriver ett fall där en patient med metastaserat malignt melanom uppvisar diabetesrelaterad ketoacidos kort tid efter nivolumabbehandling.
Fallbeskrivning
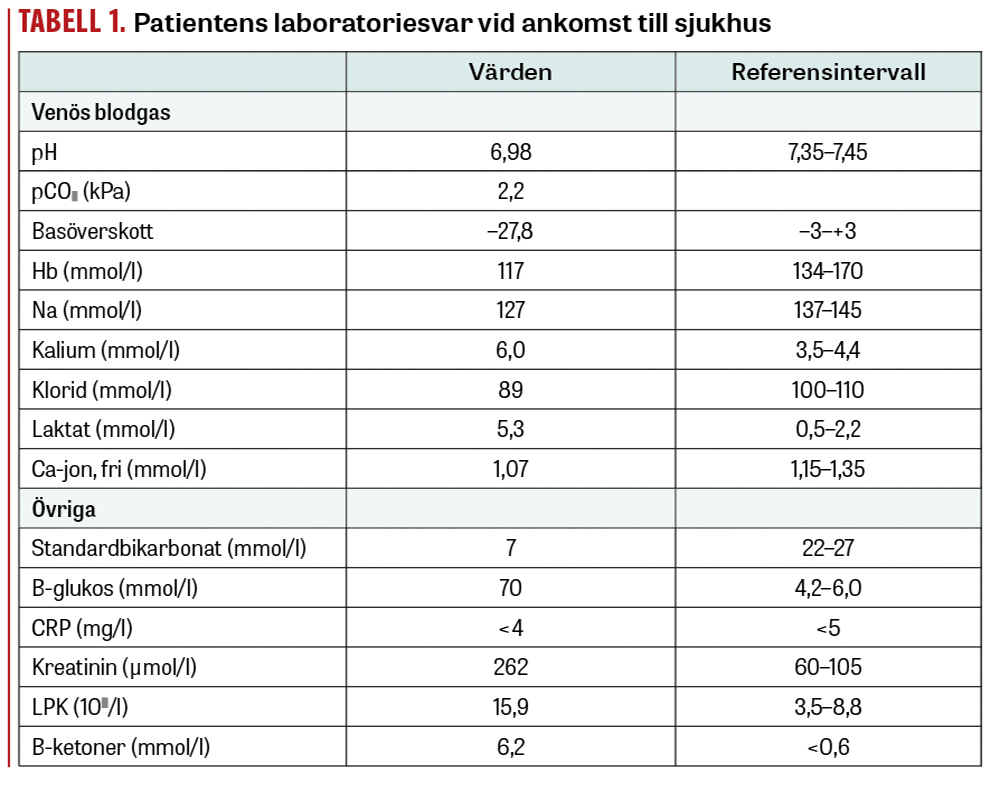
En 72-årig man med hypertoni, obstruktivt sömnapnésyndrom behandlat med CPAP (kontinuerligt positivt luftvägstryck) samt metastaserat malignt melanom med pågående immunterapi kom till akutmottagningen med ambulans på grund av illamående och sänkt allmäntillstånd. Patienten hade före det akuta insjuknande varit i gott skick, vital samt aktiv. Patienten hade stabila vitalparameterar med saturation 98 procent på luft, andningsfrekvens 20/min, blodtryck 112/64 mm Hg, puls 97/min samt temperatur 35,7 °C. I status noterades patienten ha sluddrigt tal och vara trött och tagen, men adekvat och fullt orienterad. För laboratoriesvar, se Tabell 1.
Patienten insjuknade akut med diabetes, uttalad ketoacidos och sekundär akut njurfunktionspåverkan. Patienten handlades enligt lokalt vårdprogram för diabetisk ketoacidos. Efter insulininfusionsbehandling i 32 timmar var acidosen hävd och patienten fick insulin i 4-dosregim. Kreatininnivån normaliserades successivt under vårdtiden. Provtagning visade negativa GAD- och IA2-antikroppar. HbA1c vid återbesök var 65 mmol/mol. Tyvärr togs ej C-peptid under vårdtiden.
Patienten hade 11 dagar tidigare fått åttonde dosen av nivolumab, en PD-1-hämmare. Tidigare blodsockervärden vid månatliga kontroller hade varit normala. Patienten hade insjuknat snabbt, hade ingen känd hereditet för diabetes samt hade negativa autoantikroppar. Sammantaget bedömdes detta som insjuknande i diabetes med ketoacidos orsakad av nivolumab i avsaknad av andra rimligare förklaringar.
Patienten är ett år efter insjuknandet fortsatt insulinkrävande. Nivolumab sattes ut i samband med ketoacidosen. Behandlingsregimen ändrades till en kombination av BRAF- och MEK-hämmare (dabrafenib och trametinib), läkemedel som blockerar ett kinas som bidrar till att driva tumörutveckling vid malignt melanom med BRAF-mutation.
Diskussion
Endokrina biverkningar är inte ovanliga vid behandling med immunkontrollpunktshämmare. Diabetes är en känd, men sällsynt biverkan. Insjuknandet sker ofta akut, vilket stöds av att C-peptidnivån är låg och HbA1c ofta måttligt lågt vid debuten [4]. Autoantikroppar förekommer hos ca 50 procent av patienterna som får diabetes vid behandling med immunkontrollpunktshämmare, jämfört med 85 procent av patienterna med vanlig diabetes typ 1 [4, 8]. De patienter som är positiva för GAD-antikroppar tycks dock ha en tendens att utveckla diabetes tidigare vid PD-1-hämmarbehandling än de som är negativa [8, 14]. Även om majoriteten (76 procent) debuterar med ketoacidos, har de med positiva antikroppar förutom tidigare debut även ökad risk för ketoacidos [8].
Med tanke på allvarligheten i akut insjuknande i diabetes finns rekommendationer att följa blodsocker inför läkemedelsadministration under pågående behandling med immunkontrollpunktshämmare [15, 16]. Diabetes utlöst av behandling med PD-1-hämmare har tendens att debutera fort, och vissa menar att regelbunden blodsockermätning inte hjälper till att förutsäga när diabetes kommer att debutera [7], vilket också var fallet hos vår patient. Andra rekommenderar en kombination av patientutbildning, blodsockerkontroller och blodsockermätare i hemmet [4].
Diabetes utlöst av immunkontrollpunktshämmare uppträder när en stor andel betaceller har förstörts, och dessa patienter blir insulinberoende tills vidare [4, 8]. Försök har gjorts med högdos kortison för att behandla biverkningen, men utan framgång [17].
Konklusion
Immunkontrollpunktshämmare är tämligen nya preparat som används kliniskt i allt större utsträckning. Utveckling av diabetes med ketoacidos är en sällsynt men allvarlig biverkan av PD-1-hämmare. Man har inte kunnat förutsäga när under pågående behandling patienten kan drabbas. Insjuknandet är ofta akut, och ca 75 procent insjuknar med ketoacidos, varav ca 50 procent har ett lågt C-peptidvärde och endast en tredjedel är antikroppspositiva [18]. Då insjuknandet i stor utsträckning är akut är det viktigt att patienter informeras för att kunna känna igen symtomen och söka akut vård vid behov. Det är även viktigt med kännedom hos vårdgivare på grund av det ökande antalet patienter som behandlas med PD-1-hämmare.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.