Användning av lustgas (N2O) i berusningssyfte har ökat under de senaste åren.
Ett brett spektrum av tromboemboliska (både venösa och arteriella) komplikationer har rapporterats vid hög konsumtion av lustgas.
Den bakomliggande mekanismen är inte helt kartlagd, men mycket tyder på att lustgas inaktiverar vitamin B12, vilket ger en funktionell vitamin B12-brist som leder till hög homocysteinnivå i blodet.
Med stor sannolikhet är högt homocystein drivande för tromboembolism.
Vid lustgasinducerad trombos ges sedvanlig tromboembolismbehandling samt vitamin B12. Total avhållsamhet från lustgas är nödvändig.
Inneliggande patienter med anamnes på lustgasmissbruk med komplikationer och höga homocysteinnivåer bör få tromboembolisk profylaxbehandling.
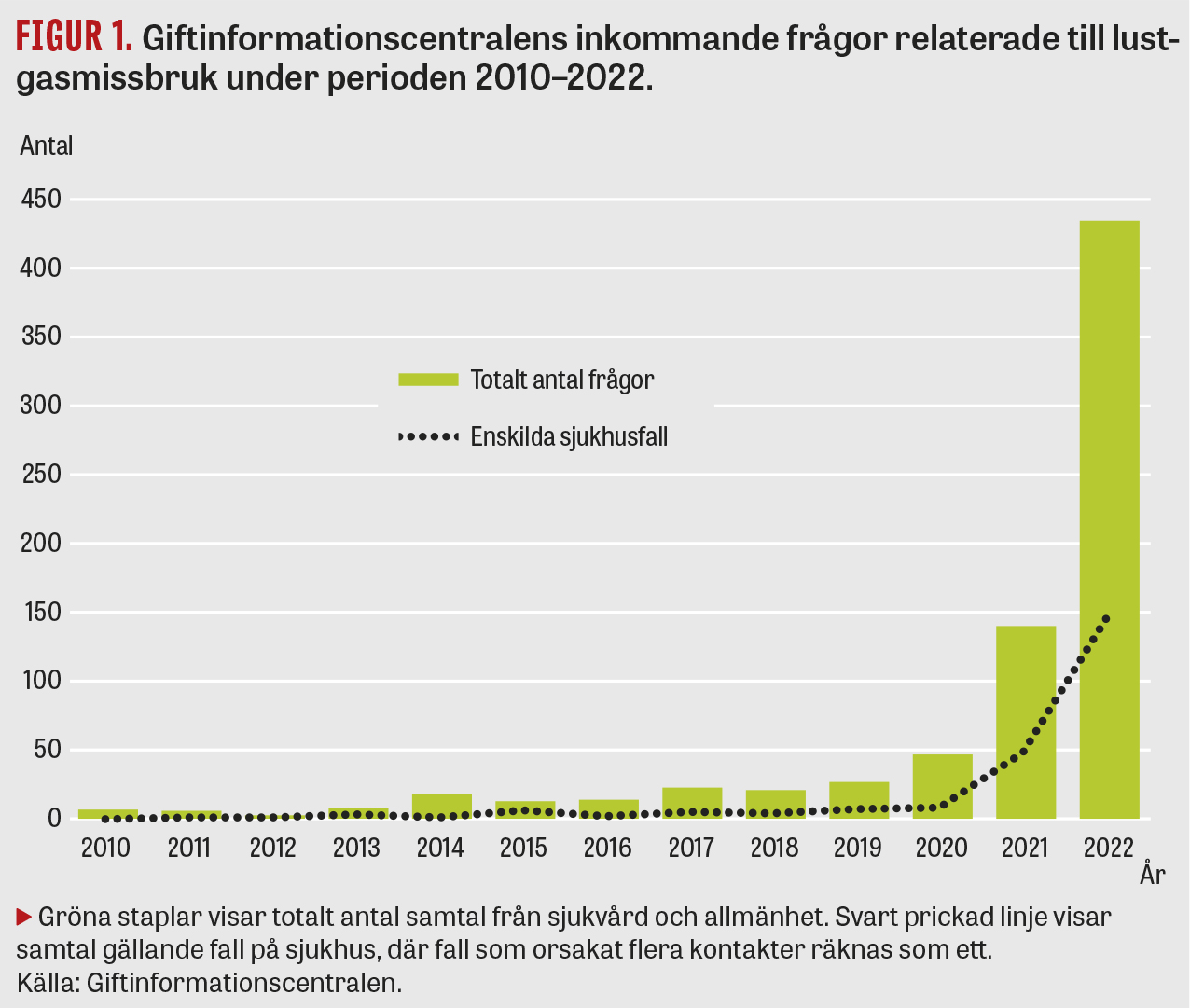
Användning av dikväveoxid (lustgas) i berusningssyfte har under senare år fått en stor spridning. Giftinformationscentralens statistik visar en stigande trend i antalet frågor relaterade till lustgasmissbruk (Figur 1). Lustgas får i dag säljas helt fritt. Det tänkta användningsområdet är framför allt tillverkning av sprutgrädde i gräddsifoner. Vid inhalation av lustgas ses ett kortvarigt rus med eufori där hallucinationer kan förekomma, vilket gjort det attraktivt som berusningsmedel [1]. Vid upprepad, extensiv lustgasanvändning finns en påtaglig risk för komplikationer. Vanligast, och mest välbeskrivet, är neurotoxisk skada med polyneuropati och ryggmärgspåverkan [2]. Förutom neurotoxicitet har också fall av tromboemboliska komplikationer rapporterats vid hög konsumtion av lustgas [3]. Vi rapporterar här om en omfattande livshotande trombotisering efter missbruk av stora mängder lustgas.
Fallbeskrivning
En 21-årig kvinna sökte akut med andningsbesvär och nytillkomna neurologiska symtom. Hon hade sedan tidigare depressiva besvär och stod på kombinerade p-piller, men var annars väsentligen frisk. Hon rökte inte och hade inte tidigare haft tromboser. Patienten uppgav att hon under de senaste åren hade brukat lustgas i berusningssyfte enstaka gånger, men att hon under de 4 månader som föregick insjuknandet hade använt ökande mängder. Under den 5-veckorsperiod som föregick akutbesöket uppgav hon ett bruk om 6–12 lustgastuber (om ca 600 g lustgas/tub) dagligen. Denna mängd motsvarar dagliga lustgasanestesier om ca 10–20 timmar (med 50 procent N2O och en respiratorisk minutvolym på 6 liter). Under denna period hade hon sökt primärvården på grund av andfåddhet som misstänktes bero på förkylning. På grund av lätt förhöjda infektionsparametrar hade hon remitterats för poliklinisk lungröntgen. Innan denna hann genomföras sökte patienten akut till följd av försämrat allmäntillstånd, uttalad andfåddhet samt tillkomst av yrsel och parestesier bilateralt i extremiteterna.
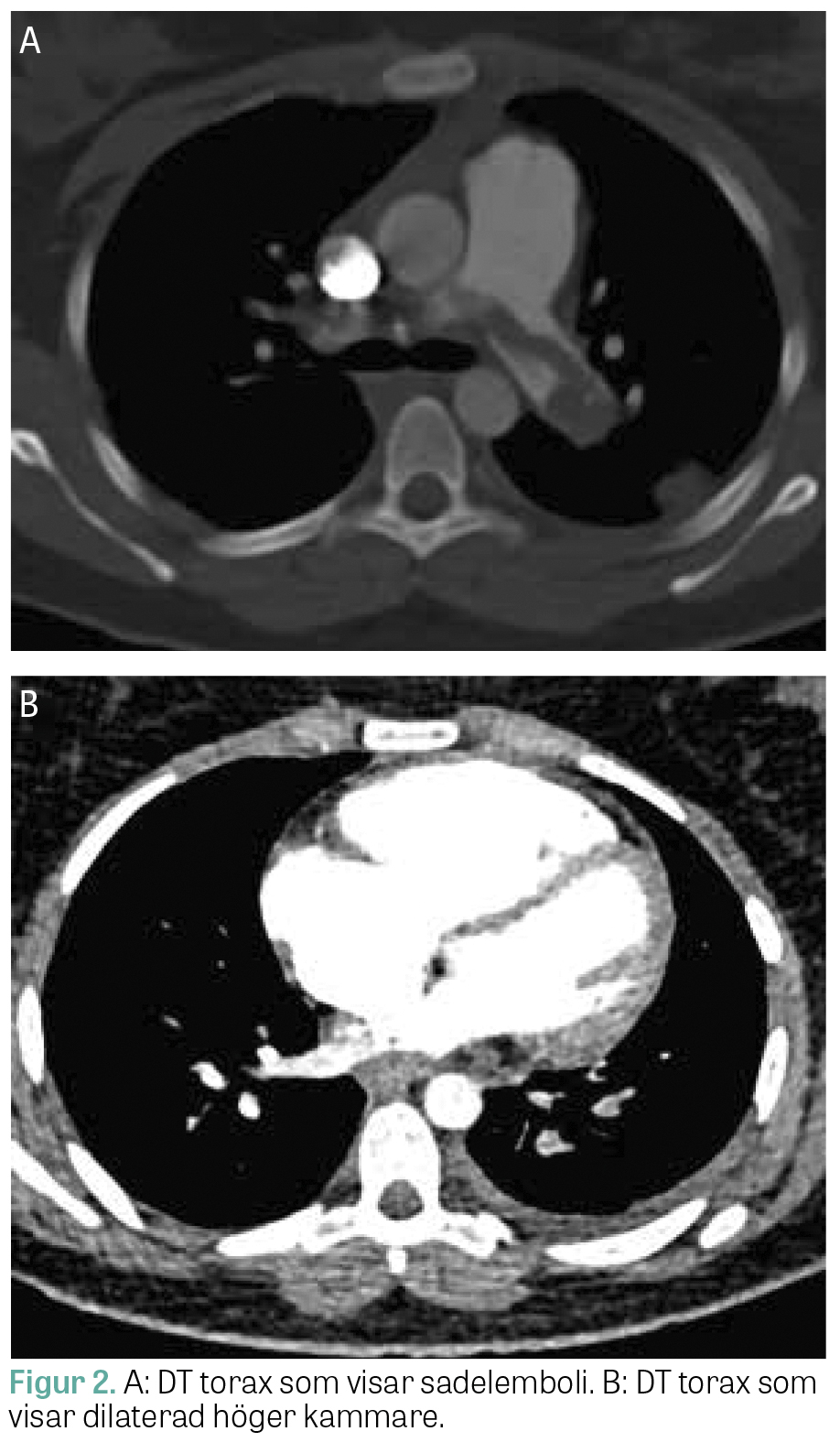
På akuten var patienten blek, takykard (130 slag/minut) och behövde 6 l syrgas för att hålla en saturation över 95 procent. Blodtrycket låg mellan 90 och 110 mm Hg systoliskt. EKG visade tecken på högerkammarbelastning, och datortomografi (DT) av lungartärer påvisade sadelemboli med bild som vid högerkammarpåverkan (Figur 2). Översiktligt ultraljud av hjärtat visade dilaterad högerkammare. Vid ankomst visade laboratorieprov förhöjt P-troponin T, 50 ng/l (referensvärde <15 ng/l), och P-NT-proBNP, 4 600 ng/l (<300 ng/l), samt förhöjt P-homocystein, 78 µmol/l (<15 µmol/l), medan S-kobalamin var 500 pmol/l (inom referensintervall). Patienten lades in för trombolysberedskap och behandlades med lågmolekylärt heparin och cyanokobalamin 2 mg × 2 per os. Patienten hade ingen tydlig fokalneurologi vid ankomst till akuten förutom upplevda parestesier i extremiteter samt yrsel, intermittent förvirring och desorientering. Vid närmare observation på avdelningen dag 2 noterades fortsatt förvirring, konfabulering och generell svaghet, som antogs vara sviter av lustgasbruket. Då det neurologiska tillståndet försämrades och talsvårigheter tillstötte gjordes dag 3 akut DT hjärna med venografi, vilken påvisade en färsk vänstersidig central infarkt. Parallellt genomfördes fullständig ekokardiografi som visade trombmassa i höger kammare samt shunt med höger–vänsterriktning på förmaksnivå. Trombolys bedömdes i detta läge vara kontraindicerad på grund av cerebral infarkt med blödningsrisk. Patienten behandlades i stället med heparinfusion och genomgick pulmonell endovaskulär trombektomi, vilken förlöpte komplikationsfritt.
Magnetkameraundersökning av hjärnan genomfördes dag 4 och visade basilaristrombos samt bekräftade förekomst av utbredda vänstersidiga ischemiska infarkter. Baserat på dessa fynd genomfördes intrakraniell endovaskulär trombektomi. Patienten behandlades med heparininfusion från dag 3 till dag 8, det vill säga inför och efter endovaskulär interventionsbehandling. Under vårdförloppet påvisades, förutom den ovan beskrivna trombotiseringen, en långsträckt trombos från vena poplitea till i vena femoralis i vänster ben och trombmassa utgående till muskelven från vena poplitea i höger ben, trombos i arteria femoralis och arteria iliaca i höger ben samt mjält- och njurinfarkter. Hon fortsatte således att trombotisera trots antikoagulantiabehandling.
Koagulationsutredning för venös tromboembolism (VTE) genomfördes vid flera tillfällen. Sammanfattningsvis påvisades vid upprepad provtagning inga kardiolipinantikroppar och inte heller beta-2-glykoprotein 1-antikroppar av IgG, IgM eller IgA-typ. Lupusantikoagulans var negativt. Utredning av antitrombin, protein C, protein S, mutation i FV-gen (APC-resistens) eller polymorfi i FII (protrombin)-gen visade inga tecken på ärftlig trombofili. Det höga homocysteinvärdet minskade snabbt efter inläggning, från P-homocystein 78 µmol/l till 29 µmol/l dagen därpå, och normaliserades sedan helt. Genetisk analys av polymorfi för metylentetrahydrofolat-reduktas (MTHFR) visade att varianten MTHFR 1286 A>C kan leda till lätt förhöjda homocysteinvärden. Patienten var homozygot för den varianten. Avseende övriga möjliga orsaker till trombotisering uppvisade patienten inga klassiska tecken på hemolys, som vid exempelvis paroxysmal nokturn hemoglobinuri (PNH). Multipla röntgenologiska undersökningar och blodprov ingav ingen misstanke om cancer.
Patienten förbättrades sedan successivt och flyttades efter 14 dagars inneliggande vård till en avdelning för neurologisk rehabilitering, där hon vårdades i drygt 3 månader. Vid överflyttningen var patienten rullstolsburen och dysfatisk och hade perifer nervpares. 3 månader efter insjuknandet hade hennes motorik förbättrats, homocysteinnivån kvarstod normal och inga nya tromboser hade diagnostiserats.
Diskussion
Nervpåverkan efter lustgas är välbeskriven [4]. Här rapporterar vi om en annan, ovanligare och mindre känd komplikation: trombotisering. Den beskrivna patienten stod på kombinerade p-piller, men bortsett från detta fanns ingen rimlig förklaring förutom lustgasmissbruk till den omfattande och livshotande trombotiseringen. Koagulationsutredning visade inga uppenbara avvikelser som kunde förklara tillståndet.
Komplikationer till extensivt lustgasmissbruk orsakas av effekter på vitamin B12 (kobalamin). Gasen oxiderar koboltatomen i vitaminet, vilket inaktiverar vitaminet och leder till en funktionell B12-brist [5, 6]. Uppmätta serumnivåer av B12 är dock ofta normala eftersom vitamin B12-analys inte skiljer på oxiderat och icke-oxiderat vitamin [5, 6]. Vitamin B12 är essentiellt för funktionen hos metioninsyntas, ett enzym som ingår i metionincykeln, en process där homocystein omvandlas till metionin, som är nödvändigt för nybildning av myelin [7]. Om metioninsyntas binder oxiderat vitamin B12 bildas ett ickefungerande komplex och metioninsyntesen avstannar. En effekt av den inbromsade metionincykeln är en ansamling av homocystein, och hyperhomocysteinemi är typiskt vid uttalad lustgasanvändning.
Tromboemboliska komplikationer efter extensivt lustgasmissbruk har beskrivits tidigare [3]. Fenomenet kan vara underrapporterat; till exempel har Giftinformationscentralen under de senaste 2 åren kontaktats om 4 fall där lustgas misstänkts vara genesen till trombotisering. Den exakta patofysiologiska mekanismen bakom trombotisering efter lustgasanvändning är delvis oklar, men tros vara sammankopplad med den hyperhomocysteinemi som uppkommer sekundärt till utslagning av vitamin B12. Höga homocysteinnivåer antas kunna leda till en ökad benägenhet för arterioskleros samt ha en protrombotisk effekt [3]. Ärftlig homocysteinuri, som ofta leder till homocysteinhalter >100 µmol/l, är en känd riskfaktor för arteriell såväl som venös trombos [8[. Även lägre nivåer av hyperhomocysteinemi har misstänkts vara associerade med ökad risk för såväl venös som arteriell tromboembolism, men dessa fynd har under senare tid ifrågasatts [9, 10]. Förhöjda homocysteinnivåer (>15 µmol/l) kan, förutom vid homocysteinuri och lustgasmissbruk, också ses vid primär brist på vitamin B6 och vitamin B12 samt vid påverkan av metylentetrahydrofolat-reduktas (MTHFR). Dessutom kan rökning, olika maligna sjukdomar, njursvikt, hypotyreos, diabetes, obesitas, hyperkolesterolemi och hypertoni samt medicinering med statiner, metotrexat och fenofibrat leda till påverkade homocysteinnivåer [9, 10]. Vid dessa tillstånd är homocysteinnivåerna dock endast lätt eller måttligt förhöjda. Möjligen gäller oklarheten kring sambandet mellan hyperhomocysteinemi och tromboembolism endast tillstånd med förhållandevis lindrig homocysteinstegring [11]. Höga nivåer (>60 µmol/l) ses vanligen endast vid homocysteinuri [11] eller vid lustgasmissbruk [7], varvid sambandet med trombos torde vara mindre kontroversiellt.
MTHFR-polymorfi är en mycket vanligt förekommande (cirka 60–70 procent i befolkningen) genetisk variation som kan leda till lätt förhöjda homocysteinnivåer. Två varianter med minskad aktivitet av MTHFR finns beskrivna: MTHFR 677 C>T och MTHFR 1286 A>C [8, 11]. Patienten i det beskrivna fallet var positiv för den senare. Denna polymorfi har en allelfrekvens på 34 procent i svensk befolkning, vilket innebär att drygt 10 procent av befolkningen är homozygot [12, 13]. Testning av MTHFR-varianter har tidigare förordats vid utredning av trombosbenägenhet. I senare studier har dock sambandet mellan MTHFR-polymorfi och trombos kraftigt ifrågasatts, och numera avråds denna analys [13, 14]. Man kan dock spekulera kring om risken för kraftigt förhöjda homocysteinnivåer och tromboemboliska händelser är högre vid extensivt lustgasmissbruk om man samtidigt har en MTHFR-polymorfi. Patientens homocystein normaliserades helt efter B12-behandling och avhållsamhet från lustgas. Möjligen skulle MTHFR-variationer även kunna predisponera för neurologiska komplikationer till lustgasmissbruk. Denna potentiellt olyckliga kombination av en, i normalfallet, ofarlig genetisk variant och yttre miljöpåverkan behöver studeras närmare.
Rekreationsanvändning av lustgas har blivit mycket vanligare de senaste åren [15], vilket åtminstone delvis måste bero på den utbredda tillgängligheten. Sådan användning kan leda till allvarliga och till och med livshotande skador. Nederländerna har kriminaliserat försäljning av lustgas till allmänheten från och med januari 2023. Vi anser att det även i Sverige krävs restriktioner för att minska tillgängligheten för allmänheten.
Lärdomar
Tromboembolism är mycket ovanlig i den yngre populationen. Hos patienter med uttalad lustgasanvändning i berusningssyfte kan det dock föreligga en ökad risk. Om det framkommer att patienten använder lustgas bör man därför ha en ökad vaksamhet vid symtom förenliga med tromboembolisk händelse.
Läs även fallbeskrivningar:
Lustgas i stora mängder kan ge psykiska och neurologiska symtom
Lustgasbruk gav pseudodemens
Läs även medicinsk kommentar:
Allvarliga och mångfasetterade följder av användning av lustgas
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.