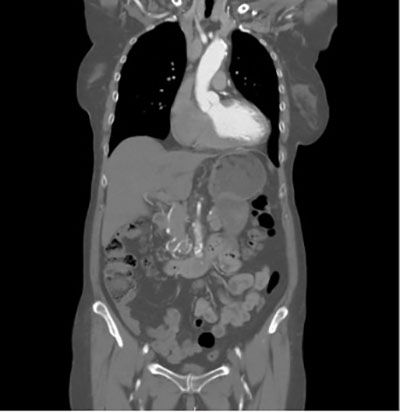
Dissektion av aorta ascendens (typ A) är ett akut och livshotande tillstånd.
Iatrogen aortadissektion, som sker under hjärtkirurgi eller perkutan kateterisering av hjärtat, har en hög dödlighet framför allt vid aortaruptur.
Behandlingen av iatrogen aortadissektion med ruptur är akut kirurgi med resektion av intimalesionen och så mycket av den dissekerade aortan som möjligt.
Kanylering av a femoralis eller a axillaris har använts traditionellt, men en ny teknik för snabb direktkanylering av aortas sanna lumen (»samurajkanylering«), som är både snabb och enkel, kan användas i akuta situationer.
En aortadissektion är en bristning av kärlets intima som leder till blödning in i kärlväggens media med dissektion och spridning av blödningen som följd [1]. Aortadissektion indelas i Stanford typ A och B [2], där typ A involverar aorta ascendens medan typ B endast engagerar aorta descendens. Typ A har en hög dödlighet på grund av aortaruptur, kranskärlsdissektion, uttalad aortainsufficiens och organischemi [3]. Spontan aortadissektion kan orsakas av långvarig hypertension, cystisk medianekros och bindvävssjukdomar som till exempel Marfans syndrom.
En undergrupp av aortadissektioner är iatrogen aortadissektion som sker under hjärtkirurgi eller perkutan kateterisering av hjärtat. Risken för iatrogen aortadissektion ökar om blodtrycket är högt under operationen eller om patienten har en försvagning av aortaväggen, såsom vid arterioskleros eller cystisk medianekros [4]. Vid öppen hjärtkirurgi sker dissektionen på ställen där ett hål har gjorts i aortaväggen under operationen, till exempel för kanylering, kardioplegi eller proximala anastomoser för vengraft, eller där man har placerat en tång på aortan. Incidensen är låg: 0,06–0,23 procent vid öppen hjärtkirurgi och runt 0,01 procent vid perkutana ingrepp [4, 5]. Dissektioner vid öppen hjärtkirurgi är främst av typ A, där den intimala lesionen oftast finns i aorta ascendens, men dissektionen kan även uppstå i retrograd riktning från kanylering av femoralisartären eller operation på aorta descendens.
Fallbeskrivning
Undersökning av en 70-årig kvinna, före detta rökare, med angina pectoris och tablettbehandlad hypertoni visade trekärlssjukdom och lindrigt nedsatt vänsterkammarfunktion (ejektionsfraktion 50 procent). Patienten genomgick elektiv koronar bypasskirurgi (CABG, coronary artery bypass grafting) med tre distala anastomoser (LIMA [vänster a mammaria interna] till LAD [vänster nedåtstigande a coronaria], vengraft till marginalgren och höger kranskärl) med standardkanylering i aorta ascendens (artärkanyl 22 French) och höger förmak. Aorta hade normal diameter, men väggen var förtjockad av arterioskleros, vilket inte syntes på lungröntgen eller andra preoperativa undersökningar.
Operationen utfördes av en specialist i toraxkirurgi med hjälp av en icke-specialist. Blodtrycket var kortvarigt högt (upp till 160 mm Hg systoliskt) i början av anestesin. Antegrad kall blodkardioplegi användes under operationen och flödet i kardioplegikanylen var långsamt, men hjärtat stannade fullständigt. I övrigt noterades inget onormalt under operationen förrän de proximala venanastomoserna syddes fast på aorta ascendens med hjälp av en sidotång. Då uppstod en ökad blödning från aorta, vilket på några minuter ledde till aortaruptur och massiv blödning. Kirurgen använde båda händerna för att stoppa blödningen från aorta och assistenten använde sugen från hjärt–lungmaskinen för att återföra blodet till patienten. Endast det falska lumen perfunderades via aortakanylen med mycket lågt blodtryck (medelartärtryck 30–40 mm Hg) som följd. Detta ledde till tecken på minskat blodflöde i hjärnan, vilket enligt rutin monitorerades under hela operationen med Invos (kontinuerlig icke-invasiv cerebral perfusionsmätning). En annan specialist inom toraxkirurgi tillkallades och bestämde sig för att utföra en så kallad samurajkanylering, det vill säga en snabb incision i aorta genom direkt kanylering av aortas sanna lumen (Figur 1).
Två tourniqueter placerades runt aorta, som skars av proximalt. En aortakanyl fördes in i aortas sanna lumen och tourniqueterna drogs åt. Det venösa blodet fortsatte att dräneras från höger förmak. Proceduren pågick i några minuter, men det tog 20 minuter för Invos-
värdena att återgå till nivåerna före dissektionen. Patienten kyldes till 21°C och antegrad kall blodkardioplegi användes. Den intimala lesionen i den dissekerade aorta resekerades och en vaskulär protes med sidoarm syddes in i aorta ascendens. Den distala anastomosen syddes först med kortvarig cirkulatorisk arrest (41 minuter), men kontinuerlig antegrad hjärnperfusion (34 minuter). Vengraften syddes in i kärlprotesen. Flödet i LIMA var lågt (<10 ml/min). Patienten lämnade hjärt–lungmaskinen med inotropt stöd.
Efter operationen låg patienten på intensivvårdsavdelningen i 6 dagar. Hon fick en perioperativ hjärtinfarkt (CK-MB [kreatinkinas-isoenzym MB] max 202 mikrog/l) med lindrigt nedsatt vänsterkammarfunktion, stroke med vänstersidig hemipares och dialyskrävande akut njursvikt. Efter lång rehabilitering på hemsjukhuset kunde patienten skrivas ut till hemmet. Hon har fortfarande viss angina pectoris och diskret svaghet i vänster hand, men är i övrigt fullt mobiliserad och intakt.
Diskussion
Den iatrogena aortadissektionen som uppstod hos patienten under elektiv bypasskirurgi hade kanske kunnat undvikas om man hade känt till att patienten hade en förtjockad och ateromatös aorta, men inga preoperativa undersökningar var tillräckligt känsliga för att avslöja förtjockningen av aorta, som var utan egentlig förkalkning. Patienten hade också hypertoni i början av operationen, vilket borde ha undvikits då hypertoni är en riskfaktor för aortadissektion. Det är troligt att dissektionen startade vid kardioplegikanylen, där flödet var långsamt. Man kunde ha opererat dissektionen som en spontan aortadissektion med kanylering i a femoralis eller a axillaris, om den inte lett till aortaruptur med massiv blödning.
En senior hjärtkirurg, som kände till samurajkanylering, tillkallades och ansåg att det var den snabbaste metoden för kanylering. På så sätt lyckades man snabbt ansluta patienten till hjärt–lungmaskin, perfundera aortas sanna lumen och etablera ett stabilt blodtryck. Komplikationerna efter operationen (stroke, akut njursvikt och perioperativ hjärtinfarkt) kan alla ha orsakats av själva dissektionen. LIMA skulle ha kunnat ersättas av ett ventransplantat, men det skulle ha förlängt operationen. Det är okänt om flödet i LIMA har återhämtat sig.
I dag utförs hjärtoperationer på gamla och mycket sköra patienter, så det är troligt att förekomsten av iatrogen aortadissektion kommer att stiga. Mortaliteten är hög (ca 30 procent), och de överlevande upplever komplikationer [5]. Iatrogen aortadissektion diagnostiseras perioperativt visuellt i 2/3 av fallen (aorta blir förtjockad, lila och blödande) eller med intraoperativ ekokardiografi. Näst vanligast är en massiv blödning postoperativt, vilket leder till reoperation. Mer sällan har patienter akut bröstsmärta efter operationen, då en datortomografi eller ekokardiografi ger diagnosen. Vid perkutana ingrepp ställs diagnosen nästan alltid under ingreppet, som utförs under röntgenfluoroskopi, och konservativ behandling kan användas för små lesioner [4].
Behandlingen av iatrogen aortadissektion vid öppen hjärtkirurgi är resektion av den intimala lesionen och så mycket av den dissekerade aortan som möjligt. Partiell eller fullständig resektion av aortabågen kan vara nödvändig. Selektiv perfusion av hjärnans artärer används, liksom övervakning av hjärnans genomblödning (Invos). Kylning används hos alla patienter och cirkulationsstopp är nödvändigt hos hälften av patienterna. Om dissektionen leder till bristning av aorta är snabb kirurgi livräddande. Kanylering i a femoralis eller a axillaris för att möjliggöra behandling i hjärt–lungmaskin kan vara svår och gå för långsamt om aortan har brustit [7, 8].
I ett försök att minska mortaliteten vid iatrogen aortadissektion har kliniker framför allt i Japan börjat använda snabb incision i aorta och direktkanylering av aortas sanna lumen, vilket har fått smeknamnet samurajkanylering. [9].
I en stor retrospektiv studie från Japan har resultaten för operation vid iatrogen aortadissektion, där samurajkanylering använts, jämförts med andra kanyleringstekniker [7]. Samma storlek på kanyl (24 French) med en knopp och dubbel tourniquet samt Trendelenburgs position användes för alla patienter som fick samurajkanylering. De japanska kirurgerna fann att tidig dödlighet och risken för stroke inte skilde sig signifikant mellan grupperna. De drar slutsatsen att samurajkanylering är en enkel, snabb och säker kanyleringsteknik för kardiopulmonell bypass under operation för iatrogen aortadissektion [10] [11]. Generellt har både korttids- och långtidsöverlevnad vid operation för aortadissektion typ A i Sverige förbättras signifikant sedan 1980-talet [12], men samurajkanylering utgör ett bra komplement för kritiska situationer.
Slutsats
Vi rapporterar ett fall från Sverige där en 70-årig kvinna drabbades av iatrogen aortadissektion och aortaruptur under en elektiv koronar bypassoperation. Hon överlevde tack vare direkkanylering i aorta ascendens sanna lumen med så kallad samurajteknik. Efter en lång sjukhusvistelse kunde patienten skrivas ut med enbart lindriga resttillstånd. Vårt fall belyser vikten av skyndsam kanylering, och vi vill lyfta fram att samurajkanylering är en både snabb och enkel metod som kan användas i kritiska situationer.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.





![Figur 1. Samurajkanylering, det vill säga en snabb incision i aorta genom direkt kanylering av aortas sanna lumen. Bildkälla: Översiktsartikel av Choudhary och Reddy [6]](https://lakartidningen.se/wp-content/uploads/2023/11/W_Figur1.png)