Primär aortoduodenal fistel orsakas oftast av ett bukaortaaneurysm som buktar mot duodenum med efterföljande erosion och fistulering.
Merparten av patienterna debuterar med en mindre gastrointestinal blödning, som efter några timmar resulterar i plötslig hemodynamisk chock.
Primär aortoduodenal fistel diagnostiseras endoskopiskt eller med datortomografi.
Behandlingen är endovaskulär eller kirurgisk, och dödligheten i avsaknad av intervention är 100 procent.
Primär aortoduodenal fistel (PADF) är ett sällsynt men livshotande tillstånd där en fistulering mellan infrarenala aorta och duodenum bildats, oftast av ett intilliggande komprimerande bukaortaaneurysm [1]. Den kliniska bilden vid PADF varierar men karaktäriseras ibland av en klassisk triad med blödning från gastrointestinalkanalen, buksmärta och en pulserande bukresistens orsakad av aneurysmet. I studier rapporteras denna triad endast hos ca 25 procent av patienter med PADF. Ibland insjuknar patienterna med synkopering och hemodynamisk chock på grund av blödning [1-4]. Tillståndet ska inte blandas ihop med de betydligt vanligare sekundära aortoduodenala fistlarna (SADF), som oftast orsakas av ett infekterat aortagraft [5]. Ett viktigt diagnostiskt tecken hos upp till 75 procent av patienter med både PADF och SADF är förekomst av en intermittent »skvallerblödning« som ofta föregår en livshotande massiv blödning. Efter spontant övergående skvallerblödning rapporteras vid PADF att massiv blödning inträffar inom de närmast följande 6 timmarna i en tredjedel av fallen, men livshotande blödning kan inträffa flera veckor efter en skvallerblödning [1, 6, 7]. Den typiska intermittenta blödningen orsakas av en tillfällig trombotisering av fisteln mellan aorta och tarm, och denna kan när som helst upplösas med risk för livshotande massiv blödning [6, 7].
Vid PADF kan fistlar bildas mellan aorta och hela gastrointestinalkanalen, men 80 procent av fistlarna bildas till duodenum, beroende på dess anatomiska närhet till infrarenala aorta. I två tredjedelar av dessa fall sker fistulering till duodenums pars horisontalis och i resten till pars descendens [1, 6].
Genesen till PADF kan i de flesta fall härledas till ett expanderande bukaortaaneurysm, som leder till kronisk mekanisk kompression av gastrointestinalkanalen. Sekundärt till denna kompression utvecklas fibros med inflammatorisk erosion av vävnad och därefter utveckling av en fistel [1, 8]. Av aneurysmen som orsakar PADF utgörs den stora majoriteten av degenerativa aneurysm (73 procent), och resterande fall orsakas av trauma eller har infektiös genes, såsom syfilis, salmonella, klebsiella eller tuberkulos [1, 3, 9, 10]. Det finns också rapporter om magsår, gallsten, pankreascancer och metastaser som orsakat erosion av tarmvägg med efterföljande fistulering till aorta [10].
PADF är ofta svårdiagnostiserat, och i flera rapporter beskrivs att diagnosen endast är känd hos en tredjedel av patienterna innan beslut om kirurgisk eller endovaskulär åtgärd fattats. Vid gastroskopi noteras ibland en extern, utifrån kommande pulserande kompression i tarmlumen, ibland med central ulceration eller koagelbildning på platsen för fistelmynningen [11]. Dock rapporteras att sensitiviteten vid gastroskopi är låg (25 procent), och därför bör misstanke om PADF bekräftas med datortomografi (DT) med intravenös kontrast. Man finner då typiskt ett reducerat spatium mellan infrarenala aorta och duodenum, intestinalt ödem och i enstaka fall aktiv extravasering av kontrast [1, 6, 12].
I obduktionsrapporter beskrivs en årlig incidens av PADF på 0,007 per 1 miljon individer och år. Män drabbas oftare av PADF än kvinnor, med fördelningen 3:1, vilket härleds till könsfördelningen av bukaortaaneurysm [1, 6, 12]. Mortaliteten vid PADF är 100 procent om man avstår från åtgärd, eftersom fisteln mellan aorta och gastrointestinalkanalen inte läker. Den viktigaste överlevnadsfaktorn beskrivs vara tiden från symtom till åtgärd: patienten bör komma till behandling innan massiv livshotande blödning inträffar [1, 7, 13].
Behandlingen av PADF är kirurgisk eller endovaskulär, med en rapporterad mortalitet mellan 61 och 77 procent [3, 13]. Det saknas studier som jämför kirurgisk med endovaskulär behandling av patienter med PADF. För patienter som åtgärdas för SADF rapporteras en 30-dagarsmortalitet på ca 34 och 7 procent efter kirurgisk respektive endovaskulär behandling, men ingen skillnad i överlevnad syns efter 2 år. Möjligen kan man anta att behandlingsresultaten av PADF och SADF är likvärdiga, eftersom tillstånden är likartade med liknande överlevnad [14]. Med anledning av skillnaden i mortaliteten mellan endovaskulär och kirurgisk behandling rekommenderas EVAR (endovascular aortic repair) som intervention hos hemodynamiskt instabila patienter, då man i senare skede rekommenderar att avlägsna fisteln operativt för att hindra ny infektion eller reblödning. Vid öppen kirurgi med graftinläggning i aorta hos cirkulatoriskt stabila patienter rekommenderas samtidig excision av fisteln och slutning av duodenum i samma seans [1, 8, 14-16].
Fallbeskrivning
En man i 70-årsåldern larmade ambulans då han under kvällen upplevt obehag i buken med illamående och blodig kräkning. Patienten var yr, perifert kall och fick prehospitalt Ringer-acetat och tranexamsyra intravenöst som behandling för övre gastrointestinal blödning av oklar genes. Patienten hade komorbiditet i form av hypertoni och gikt och drack dagligen flera enheter etanol. Vid ankomst till sjukhus var han fullt vaken och afebril, hade normal andningsfrekvens och saturerade 98 procent på luft. Blodtrycket var 100/50 mm Hg, och det förelåg en sinustakykardi med frekvens kring 110 slag per minut samt perifer kyla. Buken palperades mjuk och oöm, och vid rektalpalpation noterades normalfärgad avföring. Venös blodgasanalys visade på en metabol acidos (pH 7,26; pCO2 7,0 kPa; bikarbonat 20 mmol/l, basöverskott –3,2 mmol/l), lätt förhöjt anjongap (13,3 mmol/l) och laktatstegring (5,8 mmol/l).
Blodanalyser vid ankomst visade CRP 4 mg/l, LPK 16,0 × 109/l, Hb 110 g/l och kreatinin 127 μmmol/l. På akutmottagningen misstänkte man att detta var ett blödande ulcus eller esofagusvaricer, varför patienten behandlades med esomeprazol såväl som med terlipressin.
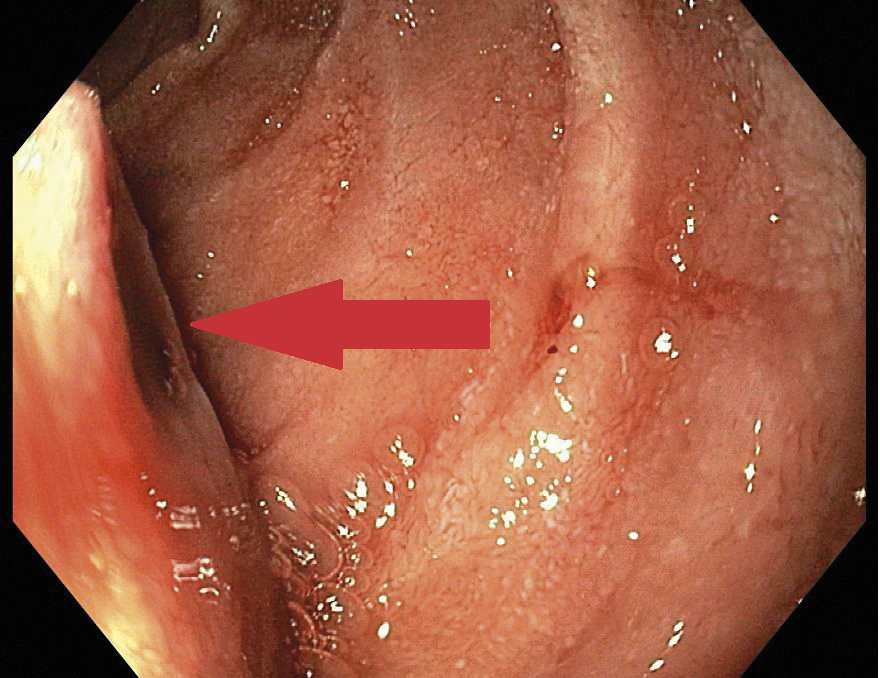
En V-sond sattes, ur vilken det tömde sig rödsvart magsäcksinnehåll. Eftersom patienten var hemodynamiskt stabil genomfördes gastroskopi först följande morgon med fynd av färskt blod i ventrikeln. I duodenums pars horisontalis noterades en submukös massa, ungefär 3 × 3 cm, med central navling täckt av koagel (Figur 1). Den endoskopiska bilden gjorde att misstanke väcktes om blödning från gastrointestinal stromacellstumör. Patienten kräktes under undersökningen, som därför inte blev fullständig, varför förnyad gastroskopi gjordes i narkos av en mer erfaren kollega. Den initiala misstanken om blödande stromacellstumör avfärdades, då förändringen var flack, mjuk och pulserande. Förändringen behandlades med adrenalininjektion samt clips för markering, och efter kontakt med kärlkirurg planerades för en efterföljande DT-angiografi.
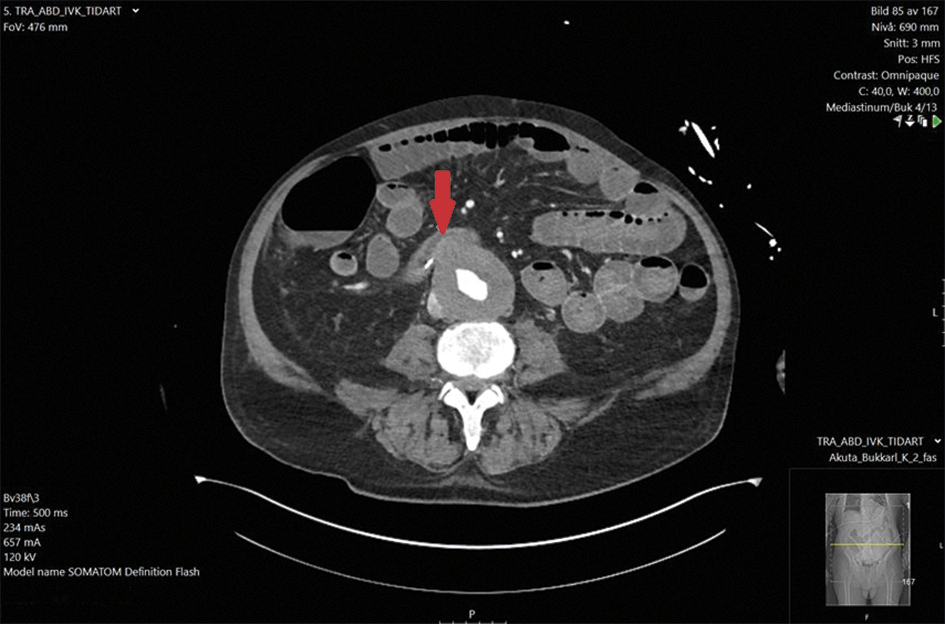
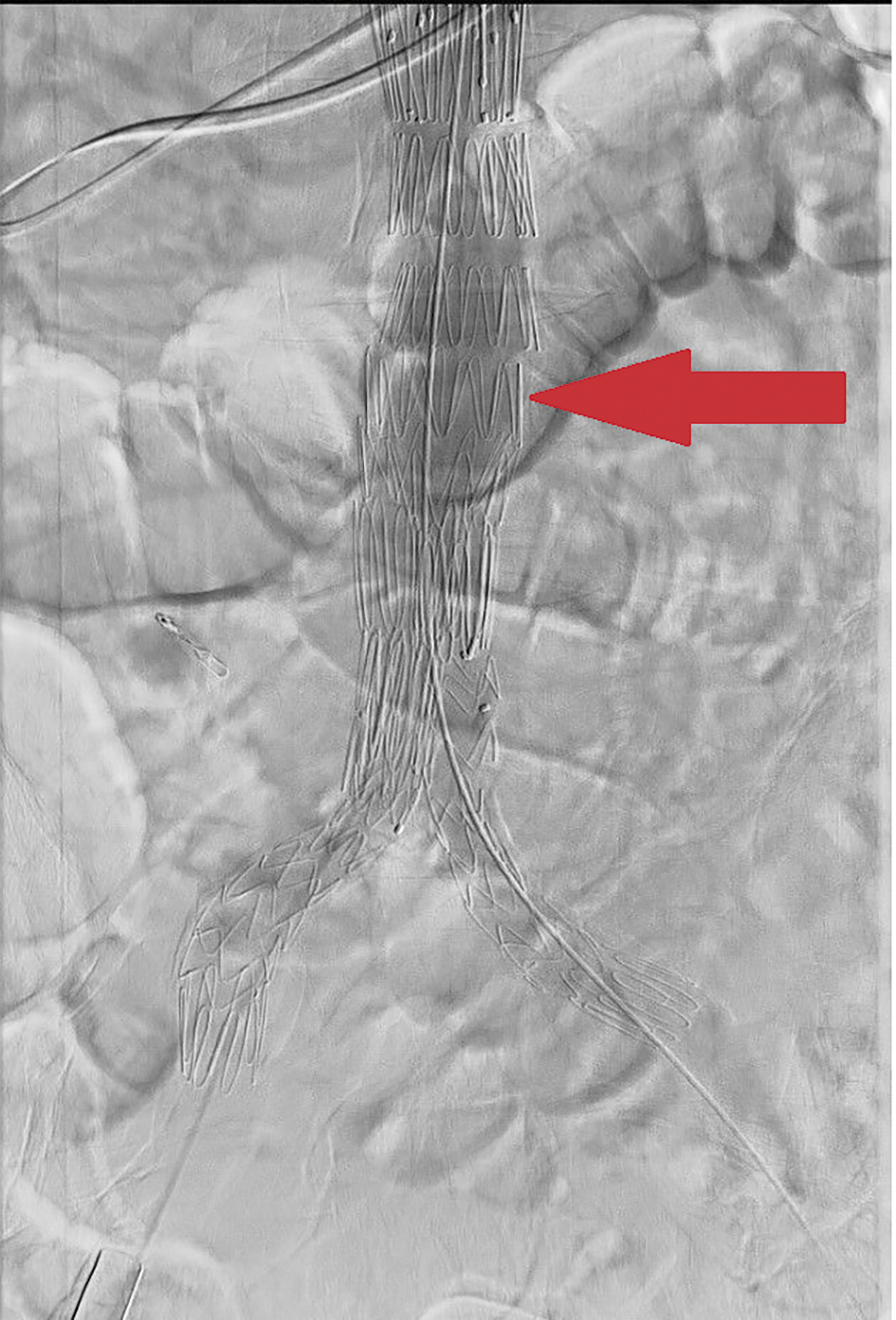
I väntan på DT-angiografi var patienten initialt hemodynamiskt stabil men drabbades under natten av ett bevittnat hjärtstopp och utbyte av färskt blod i V-sonden. På misstanke om hypovolemt hjärtstopp inleddes HLR, efter vilken patienten återfick egen cirkulation efter 45 minuter. Patienten togs till DT-angiografi, där man såg ett 6,0 cm stort bukaortaaneurysm som låg dikt an mot duodenums pars horisontalis, men det förelåg ingen pågående extravasering (Figur 2). På misstanke om PADF kontaktades åter kärlkirurg, och patienten bedömdes vara i behov av akut intervention för att förhindra ny blödning. Patienten togs direkt till operationssal där en EVAR utfördes utan omedelbara komplikationer (Figur 3).
Patienten vårdades de två följande dagarna på Iva och uppvisade inga tecken på ny blödning. Med anledning av upprepade misslyckade väckningsförsök gjordes en DT av hjärnan som visade generellt ödem, och på efterföljande EEG noterades förlångsammad aktivitet, vilket talade för anoxisk hjärnskada sekundär till hjärtstoppet. Vid vårdkonferens bedömdes prognosen som dyster, och beslut fattades om att avsluta Iva-vården, varefter patienten lugnt och stilla avled på vårdavdelning.
Konklusion
Så vitt vi känner till är detta det tredje beskrivna fallet av PADF i Sverige, även om det rimligen förekommit hos individer med liknande fall av gastrointestinal blödning [17]. Den aktuella patienten hade, likt tidigare fall i litteraturen, en skvallerblödning i hemmet som efter 24 timmar följdes av en massiv blödning som föranledde ett hemodynamiskt hjärtstopp. Fallet belyser också att PADF är svårdiagnostiserat, då patienten inte hade en fullständig klassisk triad med buksmärta, bukresistens och gastrointestinal blödning. I stället bör sammanvägd klinisk bild samt endoskopiska fynd väcka misstanke om fistel mellan gastrointestinalkanalen och aorta, även hos patienter som inte tidigare genomgått aorta- eller övre gastrointestinal kirurgi.
Fallet visar värdet av tidig endoskopisk diagnostik med intubationsnarkos vid misstanke om aktiv övre gastrointestinal blödning. På de sjukhus som har tillgång till hybridsal bör den användas, då det avsevärt underlättar snabb endovaskulär intervention, vilken kan vara livsräddande vid PADF.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.