Upptäckten av enzymet PCSK9 och dess funktion i leverns kolesterolhomeostas har inneburit nya behandlingsmöjligheter av högt kolesterol.
Tre monoklonala humana antikroppar mot PCSK9 är under utprövning i Sverige och internationellt.
Subkutana injektioner av substansen med 2–4 veckors intervall sänker LDL-kolesterol med 60–70 procent. Biverkningarna är få.
Särskilda målgrupper för behandling torde vara patienter med familjär hyperkolesterolemi och statinintoleranta patienter.
Program har utvecklats för övervakning av eventuella risker med särskilt låga LDL-kolesterolvärden.
Alla tre PCSK9-hämmarna undergår kliniska prövningar också med avseende på effekt på kardiovaskulär sjukdom och säkerhet.
Sedan 20 år är kolesterolsänkning en kliniskt väl etablerad metod att minska risken för hjärt–kärlsjukdom i sekundär och primär prevention. År 2013 intog ca 860 000 svenskar eller ca 9 procent av befolkningen lipidsänkande läkemedel, främst statiner [1]. Enligt de amerikanska riktlinjerna för kolesterolbehandling ska alla patienter med hjärt–kärlsjukdom och alla med mycket hög risk att drabbas av kärlsjukdom få högintensiv statinbehandling [2]. De europeiska riktlinjerna rekommenderar alltjämt att man använder sig av målvärden för aterogent LDL-kolesterol, och målvärdet om man har kärlsjukdom eller mycket hög risk för sådan är ≤ 1,8 mmol/l [3].
Även om statinbehandling har varit mycket framgångsrik finns dock vissa problem. Ett är biverkan i form av muskelvärk, som visserligen i allmänhet är ofarlig men ofta invalidiserande för patienten. Denna biverkan drabbar ca 10 procent av statinanvändare [4]. Ett annat problem är att även högintensiv statinbehandling ofta inte är tillräcklig för patienter med familjär hyperkolesterolemi, då målvärdena många gånger inte nås.
En ny spelare på kolesterolplanen
Behandlingen av högt kolesterol för att minska risken att drabbas av aterosklerotiska sjukdomar fick en ny vändning genom en iakttagelse av en fransk forskargrupp 2003 [5]. Familjär hyperkolesterolemi, en viktig orsak till tidig kardiovaskulär sjukdom, karaktäriseras av högt LDL-kolesterol. Mutationer i genen LDLR (som kodar för LDL-receptorn) eller apoB (som kodar för apolipoprotein B) orsakar dessa höga LDL-nivåer. De franska forskarna kartlade ett annat lokus med mutation i genen som kodar för PCSK9 (proprotein convertase subtilisin/kexin type 9) som orsak till familjär hyperkolesterolemi. Denna gen är starkt uttryckt i levern och bidrar på ett väsentligt sätt i kolesterolhomeostasen. PCSK9, som tidigare beskrivits i Läkartidningen [6], är ett sekretoriskt serinproteas som reglerar blodets LDL-kolesterolnivå genom att interagera med LDL-receptorn på levercellsytan. Efter bindning till LDL i cirkulationen omdirigerar PCSK9 LDL-receptorn efter internalisering i levercellen till lysosomal degradering. PCSK9 inhiberar därigenom återtransport av LDL-receptorn till ytan av hepatocyten och därmed katabolism av LDL.
Man har identifierat två viktiga typer av mutationer i PCSK9-genen, en som innebär ökad enzymatisk aktivitet och funktion och en med minskad aktivitet och funktion. Man har visat att mutationer som innebär funktionsnedsättning av PCSK9 minskar risken för hjärt–kärlsjukdom hos människa [7]. Två fall av homozygot form av sådana mutationer har beskrivits. Bärarna, som helt saknade PCSK9, mådde bra, var fertila och hade LDL-kolesterolvärden under 0,4 mmol/l. Det låga LDL-kolesterolet hos bärare av sådana PCSK9-varianter förmedlar också en överraskande stor effekt på hjärt–kärlrisken. Två mutationer, relativt vanliga hos afroamerikaner, medförde en 28 procent lägre LDL-kolesterolhalt jämfört med afroamerikaner med normalt PCSK9. Med en sådan LDL-kolesterolminskning skulle man förvänta sig en 25–35-procentig minskning av den kardiovaskulära risken utifrån statinstudierna. Den kardiovaskulära riskminskningen hos personer med mutationer i PCSK9-genen var emellertid 88 procent [7]. Skillnaden i utfall kan med stor sannolikhet tillskrivas att individer med mutation har åtnjutit ett lågt LDL-kolesterol under hela sin livstid.
I flera populationsstudier har man hos deltagarna kunnat relatera mutationer i PCSK9-genen till LDL-kolesterolvärden, och kunnat bekräfta mutationernas inverkan på hjärt–kärlrisken [8].
Olika vägar att minska PCSK9-aktiviteten
En terapeutisk minskning av PCSK9-aktiviteten, för att öka antalet LDL-receptorer på levercellsytan och därmed minska LDL-kolesterolhalten, skulle kunna bli en välkommen komplettering till standardterapin mot högt kolesterol. I detta syfte är åtminstone sex olika humana monoklonala antikroppar och tre antisensprinciper under utveckling [9]. Bland de antikroppar som utvecklats mot PCSK9 finns resultat från kliniska prövningar med tre, samtliga studerade inte minst i Sverige: alirocumab (Sanofi-Regeneron), evolocumab (Amgen) och bococizumab (Pfizer). Omfattande kliniska prövningsprogram pågår för alla tre substanserna. Fas II-studier visar på medelminskningar av LDL-kolesterol på 50–60 procent [10, 11].
PCSK9-hämning vid statinintolerans
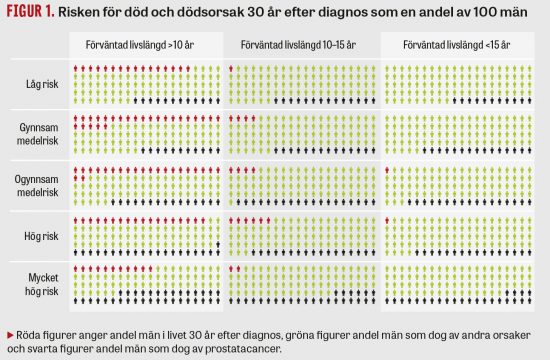
Vid Stockholm Heart Center studerades effekten på LDL-kolesterol av subkutana injektioner av evolocumab i jämförelse med ezetimib [12]; en studie som nyligen utökats [13]. I GAUSS-2-studien (Goal achievement after utilizing an anti-PCSK9 antibody in statin intolerant subjects), som var en 12-veckors dubbelblindad studie, randomiserades patienter till subkutana injektioner med evolocumab 140 mg varannan vecka, evolocumab 420 mg en gång i månaden eller ezetimib 10 mg dagligen. 307 patienter med medelvärde för LDL-kolesterol på 5,1 ± 1,6 (SD) mmol/l ingick i studien. Evolocumab reducerade LDL-kolesterol med 53–56 procent vilket innebar en behandlingsskillnad mot ezetimib på 37–39 procent (P < 0,001), Figur 1. Den totala biverkningsfrekvensen var 71 och 74 procent i evolocumab- respektive ezetimibgruppen. Muskelbiverkningar sågs hos 12 procent i evolocumabgruppen och hos 23 procent i ezetimibgruppen. Man iakttog inga fall av antikroppsutveckling mot evolocumab.
PCSK9-hämning vid familjär hyperkolesterolemi
För både alirocumab [14] och evolocumab finns prövningsprogram för behandling av patienter med heterozygot [15] och homozygot [16] familjär hyperkolesterolemi. I Rutherford-2-studien [15] randomiserades över 300 heterozygota patienter med familjär hyperkolesterolemi, med utgångsvärde för LDL-kolesterol ≥ 2,6 mmol/l, till fyra grupper med subkutana injektioner av evolocumab 140 mg varannan vecka, evolocumab 420 mg varje månad eller motsvarande placebo under 12 veckor. Samtliga patienter intog statiner, eventuellt kompletterade med andra lipidsänkare. Resultaten vad gäller LDL-kolesterol framgår av Tabell I. Jämfört med placebo ledde båda varianterna av doseringsscheman till avsevärda reduktioner av LDL-kolesterol. På samma sätt minskade behandlingen med evolocumab apolipoprotein B och icke-HDL-kolesterol med ca 50 procent, medan HDL-kolesterol ökade med ca 10 procent. Lipoprotein (a) minskade också med ca 30 procent.
Evolocumab tolererades väl. Något fler patienter fick nasofaryngit och muskelrelaterade besvär i den aktivt behandlade gruppen (p = 0,05).
Påverkar PCSK9-hämning klinisk sjukdom?
Alla tre PCSK9-hämmarna studeras i storskaliga interventionsstudier för att utröna effekt på klinisk sjukdom och säkerhet. I Odyssey outcome-studien (ClinicalTrials.gov NCT01663402) jämförs effekten av alirocumab med placebo på förekomsten av kardiovaskulära händelser hos patienter som haft ett akut koronart syndrom 4 till 52 veckor före randomiseringen. Alla ska vara behandlade med evidensbaserad lipidterapi med avseende på läkemedel och livsstil. Avsikten är att rekrytera 18 000 deltagare, och man beräknar få in tillräckligt många kliniska händelser på 70 månader. Alirocumab/placebo administreras subkutant, med dosen 75 eller 150 mg av den aktiva substansen, varannan vecka. Rekrytering av patienter pågår. Studien genomförs på 1 192 platser världen över, varav 13 är kliniker i Sverige.
I FOURIER-studien (ClinicalTrials.gov NCT01764633) är den primära hypotesen att ytterligare LDL-kolesterolsänkning med evolocumab, utöver annan lipidbehandling, tolereras väl och minskar risken för ischemiska händelser och död hos patienter med kardiovaskulär sjukdom. Män och kvinnor mellan 40 och 85 års ålder och med hög risk för återinsjuknande kan delta. LDL-kolesterol respektive icke-HDL-kolesterol ska vara ≥ 1,8 mmol/l respektive ≥ 2,6 mmol/l hos studiedeltagarna. FOURIER-studien genomförs på 1 193 kliniker världen över, varav 19 i Sverige. Rekrytering pågår, och man planerar att inkludera 27 500 deltagare. Studien ska vara klar 2018.
Med bococizumab har liknande kraftiga kolesterolreduktioner noterats. I studien SPIRE-1 (ClinicalTrial.gov NCT01975376) ska utrönas i vilken mån sänkning av LDL-kolesterol till nivåer väsentligt under nu gällande målrekommendationer ytterligare kan minska kardiovaskulära händelser. Högriskpatienter med LDL-kolesterol mellan 1,8 och 2,6 mmol/l inkluderas. 17 000 studiedeltagare planeras ingå. Rekrytering pågår vid 484 kliniker varav 8 i Sverige. I SPIRE-2 (ClinicalTrial.gov NCT01975389) studeras effekten och säkerheten av bococizumab hos högriskpatienter som inte nått LDL-kolesterolnivå under 2,6 mmol/l. 9 000 deltagare från 396 kliniker planeras ingå. Sverige är hittills inte med i SPIRE-2. I båda studierna ges läkemedlet 150 mg subkutant två gånger i månaden.
Biverkningar
Då PCSK9-hämning är en ny behandlingsform är det väsentligt att noga följa utveckling av eventuella biverkningar. Omfattande biverkningspaneler har därför ledsagat alla studier av PCSK9-hämmare. Generellt rapporteras få biverkningar från hittills genomförda kontrollerade studier med antikroppar mot PCSK9, och andelen är i alla studier liknande andelen i placebogruppen [17]. En vanligt förekommande biverkan är irritation på injektionsstället, en biverkan som i de flesta fall är lindrig och snabbt övergående och rapporteras hos ca 2 procent av de aktivt behandlade. Det föreligger inga tecken på att utveckling av antikroppar mot substanserna skulle utgöra ett problem. Erfarenheterna av långtidseffekter är emellertid begränsade på grund av den korta tid som substanserna varit föremål för kliniska test.
Kan man få för lågt kolesterol?
Ovan har refererats till två fall av homozygot form av mutationer med funktionsnedsättning av PCSK9. Bärarna, som helt saknar PCSK9, har LDL-kolesterolvärden under 0,4 mmol/l och är friska. Frågan är då om det också är ofarligt att terapeutiskt inducera mycket låga LDL-kolesterolnivåer i blodet hos individer som »är vana« vid vad vi kallar normala eller förhöjda kolesterolvärden. I evolocumabstudien LAPLACE-TIMI57 hade, i vecka 12, 47 procent av deltagarna LDL-kolesterolvärden under 1,0 mmol/l [15]. 7 patienter i studien kom ner i LDL-kolesterol under 0,5 mmol/l (ca 3 procent). Man föds med ett LDL-kolesterolvärde på ca 0,8 mmol/l [18], som därför kan anses vara fysiologiskt. Som framgår av LAPLACE-TIMI57-studien kan en minoritet nå LDL-kolesterolvärden till och med under de nyföddas. Även om individer med homozygoti för mutationer som ger funktionsnedsatt PCSK9 inte påverkas av sina låga kolesterolvärden, och även om patienter med hereditär apolipoprotein B-brist har i det närmaste total avsaknad av LDL-kolesterol och ändå mår bra, måste man ställa sig frågan om inducerat mycket lågt LDL-kolesterol är förenat med hälsorisker. Något lägsta LDL-kolesterolvärde under vilket risk för hälsan föreligger finns inte etablerat. Kliniskt beträder vi okänd mark här.
I de kliniska prövningarna av PCSK9-hämmarna ska alla patienter vara optimalt behandlade beträffande lipidnivåer i både aktivt behandlad och placebobehandlad grupp, det vill säga statiner ska vara rutinbehandling och gällande riktlinjer för hjärt–kärlprevention förstås följas. De kliniska prövningarna går ut på att undersöka i vilken mån ytterligare LDL-sänkning förmår minska sjukdomsrisken. Utgångsvärdena för LDL-kolesterol är därför redan ganska låga, i storleksordningen 1,8–2,0 mmol/l. Med 70 procents ytterligare LDL-kolesterolsänkning kommer man därför ner i värden runt 0,5 mmol/l i den aktivt behandlade gruppen.
Man kan tänka sig flera olika mekanismer för att ett mycket lågt LDL-kolesterol skulle kunna vara skadligt. För det första skulle en brist på substratet kolesterol kunna inverka menligt på syntesen av hormoner, enzymer och vitaminer som av kroppen syntetiseras från kolesterol: binjurebarkhormoner, könshormoner, gallsyror, vitamin D. För det andra kan man tänka sig att cellstrukturer som är beroende av kolesterol för sin funktion skulle kunna lida skada av för lite LDL-kolesterol i blodet. En känslig indikator på detta kan vara de röda blodkropparnas cellmembran, där en störd funktion tämligen lätt skulle kunna tänkas avslöjas genom tecken på hemolys. Risken för hemorragisk stroke kan kanske också räknas in i denna kategori. En tredje funktion som skulle kunna tänkas ta skada är LDL:s transport av andra essentiella ämnen. Ett exempel är vitaminer, som vitamin E och andra fettlösliga vitaminer, som till stor del transporteras på apoB-innehållande lipoproteiner.
En noggrann övervakning i monitoreringskommittéerna har därför iscensatts för alla dubbelblindade studier av PCSK9-hämmare. Förutom vanlig monitorering av biverkningar av olika svårighetsgrad har man fäst särskild uppmärksamhet på effekter som teoretiskt skulle kunna utlösas av en för låg halt av kolesterol i blodet. Även om den kliniska prövningen kräver dubbelblindning har man tillsatt oblindade säkerhetskommittéer, som regelbundet får rapporter om extremt låga LDL-kolesterolfall. Exempel kan nämnas från en studie (NCT01663402) där patienter som uppvisar LDL-kolesterolnivåer under 0,65 mmol/l blir föremål för särskild granskning. Mekanismer införs så att om man erhåller ett LDL-kolesterol under en viss nivå, till exempel 0,4 mmol/l, kan dosjustering eller utsättning av aktivt läkemedel genomföras. Naturligtvis måste mekanismerna införas i studiedesignen så att dubbelblindningen kan bibehållas.
Kommentar
Utvecklingen från den primära iakttagelsen av PCSK9-funktionen 2003 till ett kliniskt verksamt botemedel har gått rasande snabbt. Redan föreligger ansökan hos FDA för registrering på marknaden i USA. Man räknar med att PCSK9-hämning redan 2015 ska bli ett kliniskt tillgängligt botemedel mot för höga kolesterolvärden. Det finns dock anledning till försiktighet av flera skäl.
Läkemedelsprincipen är alltjämt studerad i begränsad omfattning, det rör sig bara om något enstaka års uppföljning och vi har hittills ingen kunskap om eventuella ogynnsamma långtidseffekter. Detta är särskilt relevant i detta fall, där vi når kolesterolnivåer i blodet som vi tidigare aldrig sett. Data om patienter med genetiska mutationer ledande till komplett funktionsbortfall av PCSK9 som lever ett normalt liv är uppmuntrande.
Det är en öppen fråga om ytterligare sänkning av LDL-kolesterol utöver vad som åstadkoms med statiner i hög dos kommer att leda till klinisk vinst. När vi med tillgänglig behandling kommer ner i LDL-kolesterolnivåer under 1,8 mmol/l är den ytterligare LDL-medierade kliniska vinsten begränsad på grund av den kurvlinjära funktionen mellan LDL-kolesterol och hjärtsjukdom. 1 mmols sänkning av LDL från 4 till 3 ger större absolut sjukdomsvinst än en sänkning från 2 till 1 mmol/l.
De monoklonala antikropparna är dyra att tillverka, och pågående interventionsstudier är kostnadskrävande. Läkemedlet kommer därför att bli dyrt. Man kan svårligen initialt tänka sig att behandlingen skulle bli allmänt tillgänglig i kardiovaskulär prevention. I första hand torde medlen riktas till patienter med terapiresistent familjär hyperkolesterolemi med särskilt hög kardiovaskulär risk liksom till högriskpatienter som inte tål statin.
Potentiella bindningar eller jävsförhållanden: Anders G Olsson har mottagit konsultationsarvoden och erhållit forskningsanslag från Amgen, AstraZeneca, Karobio, Lilly, MSD, Pfizer, Roche och Sanofi-Aventis.





![Figur 1. Procentuell minskning av LDL-kolesterol hos statinintoleranta patienter som behandlades med evolocumab subkutant alternativt ezetimib [13]. Patienterna fick evolocumab varannan vecka (A) och månatligen (B). Vertikala linjer representerar standardavvikelse.](https://lakartidningen.se/wp-content/uploads/EditorialFiles/AF/%5bDAAF%5d/DAAF_01.jpg)