Primär aldosteronism är en vanlig men underdiagnostiserad orsak till hypertoni.
Mindre än hälften av patienter med primär aldosteronism har lågt kaliumvärde.
Screening för primär aldosteronism är enkel med aldosteron/reninkvot i plasma.
Screening kan göras under pågående läkemedelsbehandling för hypertoni, dock aldrig under behandling med mineralkortikoidreceptorantagonister eller amilorid.
Hypertonirelaterade sjukdomar är vanligare än vid essentiell hypertoni.
Behandlingen är effektiv och består av minimalinvasiv binjurekirurgi eller specifik medicinsk behandling.
Primär aldosteronism orsakas av överproduktion av aldosteron från den ena eller båda binjurarna. Primär aldosteronism är den vanligaste orsaken till sekundär hypertoni med en uppskattad prevalens bland hypertonipatienter på 5–13 procent [1]. Bland patienter med svårbehandlad hypertoni är sjukdomen ännu vanligare [2]. Uppskattningsvis har 2 miljoner människor i Sverige högt blodtryck [3], vilket skulle ge en prevalens av primär aldosteronism på 100 000–260 000 individer. Endast en bråkdel av dessa identifieras i dag, vilket är ett misslyckande, eftersom patienterna kan erbjudas kurativ kirurgisk behandling eller specifik medicinsk behandling [4].
Hypertonin vid primär aldosteronism är ofta kombinerad med hypokalemi. Emellertid har drygt hälften av alla patienter med primär aldosteronism normalt S-kaliumvärde [1]. Patienter med primär aldosteronism har ökad kardiovaskulär morbiditet och mortalitet jämfört med patienter med essentiell hypertoni, oberoende av blodtrycksnivåer. För att kunna erbjuda effektiv sjukdomsspecifik behandling är det nödvändigt att diagnostisera sjukdomen.
Förekomst och patofysiologi
Tidigare ansågs primär aldosteronism vara mycket ovanlig och alltid förknippad med svårbehandlad hypertoni och hypokalemi. Med användning av kvoten mellan aldosteron- och reninnivå i plasma som ett enkelt screeningtest har antalet upptäckta fall ökat. Den första screeningstudien fann att 8,5 procent av en selekterad hypertonipopulation hade primär aldosteronism [5]. Liknande förekomst har rapporterats i en rad andra studier, både på specialistkliniker och inom primärvård från flera länder.
I Sverige har två studier undersökt prevalensen hos vuxna med hypertoni. I Skåne noterades sjukdomen hos 5 procent av nyupptäckta (icke-behandlade) patienter med hypertoni inom primärvården [6] och hos 8 procent av screenade patienter med behandlad hypertoni i primärvården i Västra Götaland [7]. Däremot hade 23 procent av screenade patienter på en hypertonimottagning primär aldosteronism [7].
Den underliggande orsaken är oftast idiopatisk hyperplasi i binjurebarken eller ett aldosteronproducerande binjurebarks-adenom (Tabell I). I ovanliga fall kan primär aldosteronism vara en ärftlig sjukdom. Tre former är kända: familjär hyper-aldosteronism typ I, II och III. Samtliga former är autosomala dominanta sjukdomar, där sjukdomen hos patienter med typ I och III oftast debuterar i ung ålder [8]. Familjära och övriga orsaker som aldosteronproducerande binjurecancer bör beaktas när den underliggande orsaken till primär aldosteronism utreds, vilket bör ske inom den specialiserade endokrinologin.
På senare år har man identifierat somatiska mutationer i gener som kodar för kaliumjonkanaler (KCNJ5 [9]) och kalcium-jonkanaler (CACNA1D) samt ATPaser (ATP1A1 och ATP2B3) hos patienter med aldosteronproducerande adenom. Det gemensamma för mutationerna är att de leder till aktivering av intracellulär Ca2+-signalering och ökad aldosteronsyntes via kronisk depolarisering av cellmembranet (KCNJ5, ATP1A1 och ATP2B3) eller direkt påverkan på kalciuminflödet i cellen (CACNA1D) [10]. Mutationer i dessa gener anses förklara ca 50 procent av aldosteronproducerande adenom, varav mutationer i KCNJ5-genen förekommer hos ca 40 procent [11]. Vilken betydelse detta kommer att få för framtida behandling av patienter med primär aldosteronism återstår att se.
Orsaken till den vanligaste formen av primär aldosteronism, idiopatisk binjurebarkshyperplasi, är mestadels oklar och inte associerad med de genmutationer som kännetecknar aldosteronproducerande adenom [12].
Följdsjukdomar och mortalitet
Patienter med primär aldosteronism har (liksom patienter med essentiell hypertoni) ökad förekomst av kardiovaskulär morbiditet [13] och mortalitet [14]. Två stora europeiska studier har dock, oberoende av varandra, visat att komplikationer är vanligare hos patienter med primär aldosteronism. I en studie från Frankrike såg man 2–5 gånger ökad risk för hjärtinfarkt, kranskärlssjukdom, hjärtsvikt och förmaksflimmer hos patienter med primär aldosteronism jämfört med patienter med essentiell hypertoni, matchade för ålder, kön och systoliskt blodtryck [15].
Likartade resultat presenterades nyligen i en studie från Italien, där man även såg ökad förekomst av stroke och ökad risk för typ 2-diabetes [16]. Nedsatt njurfunktion och albuminuri är också välkända komplikationer hos patienter med primär aldosteronism [17]. Det finns därför starka skäl att identifiera primär aldosteronism som orsak till hypertoni för att kunna erbjuda patienterna specifik behandling och därmed förbättra deras prognos.
Diagnostik
Utredningen av primär aldosteronism kan delas upp i tre steg:
- screening
- bekräftande av diagnos
- utredning avseende underliggande orsak.
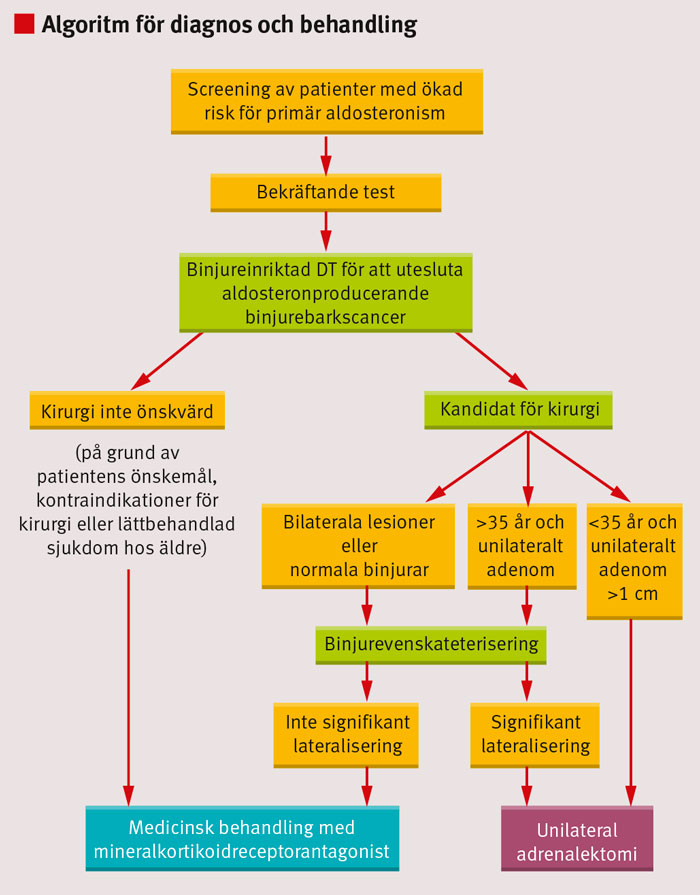
Det förslag till algoritm för utredning och behandling som presenteras här baseras på publicerade konsensusdokument och riktlinjer [1, 2, 18-21] (Figur 1). Algoritmen understryker vikten av screening av patienter med hypertoni, varefter kompletterande utredning avgör val av lämpligaste behandling. Screening bör ske på samtliga sjukvårdsenheter som handlägger patienter med hypertoni, medan verifiering av diagnos och fastställande av underliggande orsak bör ske på special-enheter för endokrinologi.
Screening. Med tanke på den höga prevalensen och den ökade risken för följdsjukdomar rekommenderas screening av alla patienter med ökad risk för sjukdomen. På vissa ställen (t ex Japan) rekommenderar man att samtliga patienter med hypertoni ska screenas [22]. Denna screeningsstrategi är dock sannolikt inte kostnadseffektiv, och därför väljer de flesta att screena selekterade patientgrupper (Fakta 1) [1].
Screening görs genom mätning av aldosteron och renin i plasma där kvoten mellan hormonnivåerna räknas. Proven tas efter 5–15 minuters vila i sittande på morgonen efter det att patienten har varit uppe i minst 2 timmar. Patienten behöver inte vara fastande [1]. I dag används samma analysmetoder på de flesta laboratorier i Sverige, men vad som anses vara en patologisk aldosteron/reninkvot varierar något. De flesta anser att patienter med aldosteron (pmol/l)/renin (mIE/l)-kvot >60 bör utredas vidare, medan vissa laboratorier anger något högre kvot och andra något lägre. Den som tolkar aldo-steron/reninkvot hos en patient med misstänkt primär aldo-steronism bör därför ta hänsyn till vilka analysmetoder som används och vilket referensområde som gäller på det lokala laboratoriet.
Flera faktorer kan påverka koncentrationerna av aldosteron och renin i plasma och därmed aldosteron/reninkvoten. Normokalemi bör eftersträvas vid screening, eftersom lätt sänkt kaliumvärde ger kraftfull hämning av aldosteron, vilket ger falskt låg aldosteron/reninkvot. Således ska hypokal-emiska patienter med misstanke om primär aldosteronism ha adekvat kaliumersättning i tablettform innan screeningproven tas. Vilken dos av kalium som behövs är individuellt, ibland kan upp till 20–40 kaliumkloridtabletter om dagen behövas.
Screening för primär aldosteronism kan emellertid göras under pågående läkemedelsbehandling för hypertoni, dock aldrig under behandling med mineralkortikoidreceptorantagonister (spironolakton eller eplerenon) eller kaliumsparande diuretikum (amilorid). De flesta läkemedel som används för behandling av högt blodtryck påverkar dock kvoten signifikant med undantag av alfa-receptorantagonister, kalcium-antagonisten verapamil och hydralazin (Tabell II). Det optimala vid screeningen är att patienten inte behandlas med läkemedel som påverkar aldosteron/reninkvoten.
I vissa fall kan det vara svårt att sätta ut den läkemedelsbehandling som patienten har, t ex patienter med ischemisk hjärtsjukdom och/eller mycket svårbehandlad hypertoni. I sådana fall är det viktigt att noggrant överväga vilka läkemedel man kan hålla upp med under utredningen och vilka som måste behållas. Provtagningsresultaten hos patienter som behöver stå kvar på mediciner som påverkar aldosteron/reninkvoten måste då tolkas utifrån aktuell medicinering.
Differentialdiagnoser. Den största utmaningen vid utredning av patienter med misstänkt primär aldosteronism är att skilja sjukdomen från essentiell hypertoni. Hypokalemi kan inte användas i detta syfte, eftersom mindre än hälften av patienter med primär aldosteronism har lågt kaliumvärde [23, 24]. Här krävs screening genom mätning av aldosteron och renin i plasma enligt ovan.
Ett flertal andra tillstånd kan ge hypertoni och hypokal-emi. Relativt vanliga är renovaskulär hypertoni på grund av njurartärstenos eller fibromuskulär dysplasi samt överdrivet lakritsintag. Laboratoriemässigt kännetecknas renovaskulär hypertoni av högt renin i plasma och normal aldosteron/reninkvot. Högt lakritsintag och de mer ovanliga sjukdomarna Cushings syndrom, Liddles syndrom och »syndrome of apparent mineralocorticoid excess« kännetecknas av låga värden aldosteron och renin och kallas tillsammans pseudohyperaldosteronism.
Glukokortikoidhämningsbar aldosteronism är ytterligare en ovanlig sjukdom som kännetecknas av hypertoni och hypokalemi med hög aldosteron/reninkvot. Sjukdomen är ärftlig och debuterar i ung ålder. Unga patienter med primär aldosteronism ska därför utredas vidare med dexametasonhämningstest, alternativt genetisk analys, för att utesluta denna ovanliga form, där behandlingen består av kortison i låg dos.
Bekräftande test. Nästa steg i utredningen av patienter med stegrad aldosteron/reninkvot och misstänkt primär aldosteronism är att bekräfta diagnosen. Detta bör utföras på en specialenhet, och fyra olika test kan utnyttjas: fludrokortisonhämningstest, oral eller intravenös saltbelastning eller kaptopriltest. Samtliga bekräftande test går ut på att hämma den egna aldosteronproduktionen. Kännetecknande för patienter med primär aldosteronism är autonom aldosteronproduktion som inte går att hämma. Vad som bedöms vara adekvat hämning av aldosteron varierar mellan de olika testen och analysmetoderna. Denna utredning är viktig att utföra under normokalemiska förhållanden och i möjligaste mån utan läkemedel som påverkar utfallet enligt ovan.
Utredning av underliggande orsak. Nästa steg i utredningen är att fastställa orsaken och att avgöra om det föreligger en ensidig dominans av aldosteronproduktionen eller om den är bilateral. Detta är helt avgörande för val av behandling och utförs också på specialenhet.
Samtliga patienter med konstaterad primär aldosteronism ska undersökas med datortomografi av binjurarna. Syftet är att dels utesluta aldosteronproducerande binjurebarkscancer (ytterst sällsynt), dels kartlägga binjurevenssystemet inför eventuell binjurevenskateterisering. Syftet med datortomografi av binjurarna är inte att skilja mellan patienter med unilateral respektive bilateral aldosteronöverproduktion [25].
I en väl genomförd studie från Italien fann man att 5 procent av patienter med normala binjurar och 33 procent med bilaterala förändringar i själva verket hade ensidig sjukdom [26]. Vidare såg man att en tredjedel av patienterna med unilaterala DT-fynd hade bilateral sjukdom.
Den undersökning som i dag bör användas för att skilja mellan unilateral och bilateral aldosteronöverproduktion är binjurevenskateterisering. Vid undersökningen kateteriseras höger och vänster binjureven och blodprov tas för analys av aldosteron och kortisol. Kortisolkoncentrationerna används både för att säkerställa adekvat kateterläge och för att kunna beräkna spädningseffekter från närliggande vener [25]. Aldosteron/kortisolkvoten beräknas för de båda sidorna och perifert.
Allmänt anses att patienter med fyra gånger högre aldosteron/kortisolkvot på den ena sidan har en ensidig dominans i sin aldosteronproduktion. På vissa centra bedöms även patienter med något mindre sidoskillnad (tre gånger högre) ha unilateral sjukdom, under förutsättning att aldosteronproduktionen från den kontralaterala sidan är supprimerad, dvs att aldosteron/kortisolkvoten är lägre än vad som mäts i perifer ven. Binjurevenskateterisering är en tekniskt svår undersökning som bör utföras av en erfaren och dedikerad läkare [25].
Tidigare användes binjureskintigrafi och s k posturaltest (gå och stå-test) för utredning avseende underliggande orsak, dvs för att skilja mellan aldosteronproducerande adenom och idiopatisk hyperaldosteronism. Sensitivitet och specificitet hos dessa undersökningar är dock låga, och de används därför sällan i dag. Den kliniska presentationen är inte heller till hjälp vid värderingen av underliggande orsak. Trots att patienter med aldosteronproducerande adenom i större utsträckning har mer svårbehandlat blodtryck och oftare hypokalemi, föreligger betydande överlappning med bilateral idiopatisk hyperplasi.
11C-metomidat-PET-DT har i en liten jämförande studie av binjurevenskateterisering givit lovande resultat [27]. I framtiden kan det således öppnas möjligheter till att genomföra utredning avseende lateralisering med icke-invasiva metoder.
Kirurgisk behandling
Kirurgisk behandling är indicerad vid primär aldosteronism med unilateral dominans av aldosteronproduktionen. Vid beslut om kirurgi ska hänsyn tas till patientens önskemål, eventuell komplicerande samsjuklighet, sjukdomens svårighetsgrad och patientens ålder (Figur 1). Patienter som inte anses vara kandidater för kirurgisk behandling bör inte genomgå binjurevenskateterisering.
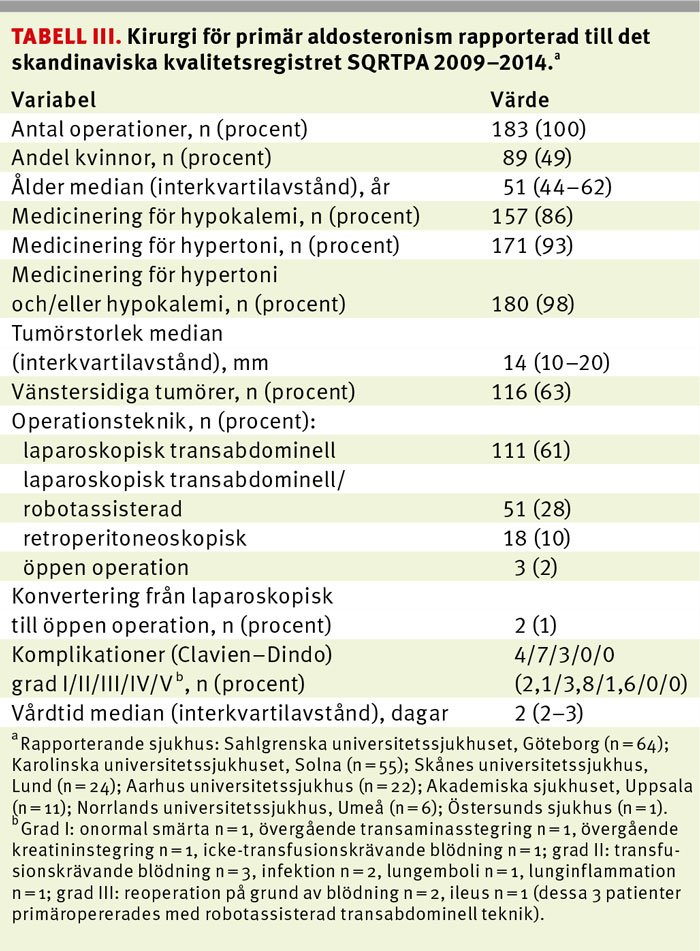
Resultat av binjurekirurgi rapporteras sedan 2009 till Scandinavian quality register for thyroid, parathyroid and adrenal surgery (SQRTPA). Under perioden 2009–2014 registrerades 183 operationer för primär aldosteronism. Könsfördelningen var jämn och medianåldern vid kirurgi var 51 år (Tabell III). Totalt 98 procent av patienterna medicinerade för hypertoni och/eller hypokalemi vid operationstillfället. Minimalinvasiv kirurgisk teknik användes nästan uteslutande, och den transabdominella laterala tekniken (utan eller med robotassistans) var vanligast. Direkt retroperitoneoskopisk teknik användes i 10 procent av fallen. Vårdtiden var kort (2–3 dagar) och allvarliga komplikationer sällsynta. Eftersom det finns ett signifikant bortfall i registret avseende postoperativa kontroller, kan säkra slutsatser om långtidsutfall inte dras från registerdata.
I publicerade kirurgiska serier uppnåddes biokemisk bot (normalisering av den hormonella rubbningen) hos 96–100 procent och normalisering av blodtrycket hos 42 procent (spann 20–72) av patienterna [4]. Identifierade positiva prediktiva faktorer för bot är låg ålder, kvinnligt kön, kort duration av hypertoni, färre olika antihypertensiva läkemedel, normal njurfunktion, histologiskt verifierat aldosteronproducerande adenom och mutationer i KCNJ5-genen. Resultaten var bättre i serier med längre uppföljning, vilket kan antyda positiva kardiovaskulära effekter av operation många år efter ingreppet. Ingen mortalitet vid detta ingrepp finns registrerad i SQRTPA eller i publicerade serier. Inga skillnader i resultat kunde påvisas mellan olika minimalinvasiva tekniker.
Eftersom unilateral aldosteronproduktion oftast orsakas av ett (godartat) adenom (Tabell I) har partiell adrenalektomi använts som ett alternativ till total adrenalektomi hos patienter med en dominant lesion. Syftet är då att spara så mycket normal binjurevävnad som möjligt. Partiell och total adrenalektomi har jämförts i två randomiserade kontrollerade studier utan att någon skillnad kunde påvisas [28, 29]. Detta står i kontrast mot studier med immunhistokemi och in situ-hybridisering, vilka påvisat hyperplasi, multipla adenom eller kombinationer av dessa hos 16–27 procent av patienter som opererats för unilateral sjukdom [30-33]. Immunhistokemisk karakterisering av enzymer för aldosteron- (CYP11B2) och kortisolsyntes (CYP11B1, CYP17A1) har således föreslagits som en metod för att styra uppföljning efter kirurgi [33].
Medicinsk behandling
Patienter med bilateral aldosteronöverproduktion och patienter med unilateral sjukdom som inte är aktuella för kirurgi bör behandlas med mineralkortikoidreceptorantagonist. Vid medicinsk behandling är det inte bara viktigt att sänka blodtryck och korrigera eventuell hypokalemi utan också att blockera aldosteronets skadliga effekter på bl a hjärta, kärl och njurar.
I Sverige finns två mineralkortikoidreceptorantagonister registrerade: spironolakton och eplerenon. Båda läkemedlen är effektiva vad gäller att sänka blodtrycket och att normalisera kaliumvärdet när de ges i adekvata doser. En gynnsam effekt även på hjärtfunktion, njurfunktion och glukosmetabolism har rapporterats i ett flertal studier (sammanfattade av Muth et al [4]).
Biverkningsprofilen skiljer sig dock avsevärt åt mellan spironolakton och eplerenon. Spironolakton påverkar inte bara mineralkortikoidreceptorn utan har också blockerande effekter på androgenreceptorn och stimulerande effekt på progesteronreceptorn. Minskad sexlust, impotens, mensrubbningar, bröstömhet och gynekomasti är därför vanliga – och dosberoende – biverkningar vid behandling med spironolakton [34]. Eplerenon har en mer selektiv bindning till mineralkortikoidreceptorn än spironolakton, och biverkningar av ovanstående slag är därmed betydligt mindre vanliga.
Vanlig startdos för spironolakton är 50–100 mg dagligen och för eplerenon 25–50 mg. Doserna trappas upp successivt vid behov. En vanlig dos spironolakton är 200–300 mg dagligen och en vanlig dos eplerenon är 100–150 mg [34].
Målet med behandlingen är att patienten blir normotensiv och normokalemisk. Efter insättning av mineralkortikoidreceptorantagonist bör således blodtryck följas regelbundet samtidigt som eventuell förekomst av hyperkalemi ska följas. Annan blodtryckssänkande behandling kan läggas till vid behov för att uppnå uppsatta målvärden för blodtryck.
I en nyligen genomförd systematisk översikt konstateras att det saknas randomiserade studier som jämför kirurgisk och medicinsk behandling [4]. Värdering av publicerade studier försvåras av skillnader i utfallsmått, otillräcklig storlek och att grupperna inte är helt jämförbara vad gäller ålder, samsjuklighet m m. Det framgår dock att medicinskt behandlade patienter kan ha överdödlighet [14] och behöver fler mediciner [35, 36], längre uppföljningstid och fler återbesök än de som opererats [37]. Adrenalektomi har även visats vara mer kostnadseffektiv än långtidsbehandling med läkemedel [38, 39].
Konklusion
Trots ökande kunskap och mycket goda behandlingsresultat är primär aldosteronism fortfarande ett kraftigt underdia-gnostiserat tillstånd. Screeningmetoden är enkel och välvaliderad, och med hjälp av denna har prevalensen hos patienter med hypertoni fastställts till mellan 5 och 13 procent beroende på om studierna utförts inom primärvård eller vid specialiserade hypertonienheter.
Efter kompletterande undersökningar rekommenderas adrenalektomi vid ensidig sjukdom och mineralkortikoidreceptorantagonister till patienter med bilateral sjukdom.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.
Fakta 1.
Tillstånd där screening för primär aldosteronism bör övervägas [1]
- Blodtryck >160/100 mm Hg
- Terapiresistent hypertoni (patienter med okontrollerad hypertoni [>140/90 mm Hg] som behandlas med tre olika läkemedel för högt blodtryck samt patienter med kontrollerad hypertoni som behandlas med fyra eller fler olika läkemedel för högt blodtryck)
- Hypertoni och spontan eller diuretikautlöst hypokalemi
- Binjureincidentalom och hypertoni
- Hypertoni i kombination med ärftlighet för cerebrovaskulär sjukdom i ung ålder (<40 år)