Antalet patienter med icke-valvulärt förmaksflimmer ökade mellan 2011 och 2017 från 41 008 till 51 266 i Stockholms läns landsting, och deras behandling har förbättrats avsevärt.
Behandlingen av alla patienter med förmaksflimmer med CHA2DS2-VASc ≥2 poäng med orala antikoagulantia (OAK) har ökat från 54 procent (warfarin) till 82 procent (varav 48 procent NOAK) medan användningen av ASA har minskat från 33 procent till 7,6 procent. Störst förbättring ses hos de äldsta patienterna med den högsta strokerisken.
En observationell studie visade att NOAK var minst lika säkra och effektiva som warfarin i Stockholms läns landsting, även bland patienter ≥80 år, och vi har även funnit en mycket god persistens med OAK-behandling.
NOAK har bidragit betydelsefullt till en förbättrad strokeprevention vid förmaksflimmer.
Förmaksflimmer har en prevalens av minst 3 procent i den vuxna befolkningen totalt och ökar kraftigt med stigande ålder till 10–15 procent hos individer ≥75 år [1]. Strokerisken är förhöjd, och av alla stroke relateras 20–30 procent till förmaksflimmer [2, 3]. Warfarin och acetylsalicylsyra (ASA) var länge de enda alternativen för strokeprofylax vid förmaksflimmer, och underbehandling med orala antikoagulantia (OAK) var ett stort problem. NOAK (non vitamin K OAK; icke vitamin K-beroende OAK) har givit oss goda möjligheter att förbättra behandlingen vid förmaksflimmer. I Stockholms läns landsting (SLL) har vi arbetat med införandet av NOAK dels i Läkemedelskommitténs (SLKs) berörda expertråd, dels i en särskild projektgrupp. Det har även funnits många aktiviteter från industrin och professionella organisationer som satt fokus på förmaksflimmer och dess behandling under dessa år. Vi beskrev situationen i SLL 2015 under den tidiga fasen av NOAK-introduktionen [4] och ger nu en lägesrapport för 2017 som visar markanta förbättringar av strokeprofylaxen vid förmaksflimmer.
Riskskattning viktigt
Strokerisken skattas med CHA2DS2-VASc-skalan vid ställningstagande till strokeprofylax med OAK [3, 5]. Den årliga strokerisken varierar från 1,3 procent vid 1 poäng till 15,2 procent vid 9 poäng [5]. Europeiska kardiologsällskapet har fram till 2016 ansett att CHA2DS2-VASc ≥2 poäng utgör indikation för OAK. 2016 ändrades detta till att kvinnor ska ha ≥3 poäng, eftersom strokerisken endast är större hos kvinnor med en hög riskprofil vilka ändå är kvalificerade för OAK-behandling [3]. För patienter med 1 poäng (2 poäng för kvinnor) ska man överväga OAK-behandling, varvid ålder 65–74 år är den starkaste riskfaktorn. Läkemedelsverket ansluter sig till dessa rekommendationer [6].
Även blödningsrisken ska vägas in i ställningstagandet till behandling. Skattningsskalan HAS-BLED introducerades 2010 [5] men ersattes 2016 av en rekommendation att minimera åtgärdbara riskfaktorer för blödning och sträva efter att ge OAK även om blödningsrisken är hög [3]. En anledning till detta är att riskerna för stroke och blödning samvarierar.
En rädsla för behandling med warfarin hos både patienter och läkare, besvären med INR-kontrollerna och troligen även en underskattning av behandlingsnyttan bidrog till en underbehandling med OAK vid förmaksflimmer medan ASA överskattades som ett »lindrigare« alternativ. Jämfört med placebo minskade warfarin dock strokerisken med 64 procent medan ASA endast minskade den med 19 procent [7]. Risken för stroke halverades med warfarin [7, 8] eller apixaban [9] jämfört med ASA, utan fler allvarliga blödningar. Vikten av att ge OAK i stället för ASA poängteras därför allt mer.
NOAK – värdefulla alternativ till warfarin
Dabigatran (Pradaxa) lanserades i slutet av 2011, följt av rivaroxaban (Xarelto; 2012), apixaban (Eliquis; 2013) och edoxaban (Lixiana; 2016). NOAK är direktverkande (och kallas därför ibland DOAK). Dabigatran hämmar trombin medan de övriga hämmar faktor Xa. De har olika farmakologiska egenskaper som beskrivs i olika riktlinjer [3, 6, 10, 11] och i ett jämförande dokument från oss på janusinfo.se [12].
I korthet skiljer sig de olika NOAK avseende doseringsintervall, halveringstider i plasma, njurfunktionsberoendet i elimineringen, anvisningar för dosreducering vid hög ålder eller sänkt njurfunktion, interaktioner med andra läkemedel och tillgång till antidoter. Europeiska arytmisällskapet har nyligen uppdaterat sina praktiska riktlinjer för NOAK-behandling vid förmaksflimmer med bland annat aktuell information om läkemedelsinteraktioner [11].
De grundläggande NOAK-studierna
De grundläggande förmaksflimmerstudierna, som har något varierande design och ej är direkt jämförbara, visade sammantaget att NOAK var lika bra som eller möjligen bättre än warfarin [13-16]. I RE-LY-studien fick man färre ischemiska stroke men fler GI-blödningar med dabigatran 150 mg × 2, medan 110 mg × 2 var neutralt avseende sådana händelser [13]. I ROCKET-AF-studien var rivaroxaban »non-inferior« avseende ischemisk stroke men orsakade fler GI-blödningar [14]. I ARISTOTLE-studien visades apixaban ge färre ischemiska stroke och allvarliga blödningar samt en lägre mortalitet [15]. I ENGAGE AF-TIMI 48 var edoxaban 60 mg × 1 »non-inferior« avseende ischemisk stroke, men orsakade fler GI-blödningar; 30 mg × 1 gav fler ischemiska stroke men färre GI-blödningar [16]. Samtliga prövningar visade färre hemorragiska stroke med NOAK jämfört med warfarin.
Europeiska kardiologsällskapet rekommenderade NOAK före warfarin redan 2012 [17], men vi hade en del frågor kring NOAK-studiernas generaliserbarhet till svensk sjukvård [4, 12]. För warfarin bör tid inom terapeutiskt intervall (TTR, tiden patienten har PK[INR] 2,0–3,0) vara ≥70 procent [18]. Medel-TTR var under 70 procent i alla studierna och endast 55 procent i ROCKET-AF [14]. Vissa länder hade medel-TTR <50 procent medan svenska centrum hade 75–80 procent. För dabigatran [19] och apixaban [20] visades minst skillnader gentemot warfarin vid höga TTR-värden. NOAK var inte effektivare än warfarin men gav färre allvarliga blödningar i Europa [21]. Patienterna i kliniska prövningar är selekterade och ofta yngre och »friskare« samt bättre informerade och uppföljda än i vanlig rutinsjukvård. I NOAK-studierna var medelåldrarna 70–73 år medan omkring 40 procent av patienterna med förmaksflimmer i SLL är ≥80 år (Tabell 1). Patienter med nedsatt njurfunktion (Cockcroft–Gault <30 ml/min) exkluderades. Så hur väl kunde prövningarnas resultat generaliseras till populationen med förmaksflimmer i vår sjukvård [4, 12]?
Pre-NOAK-eran i SLL
Vi inledde bevakningen av OAK-behandling vid förmaksflimmer med studier av situationen innan NOAK introducerades. I våra studier användes avidentifierade data från SLL:s vårdanalysdatabas som innehåller data avseende ålder, kön, diagnoser (ICD-10), vårdkonsumtion, förskrivarkategori och uthämtning av läkemedel (från Läkemedelsregistret) för alla 2,2 miljoner individer i SLL. Vårdanalysdatabasen täcker både primär och sekundär vård. Patienter med icke-valvulärt förmaksflimmer, utan diagnoskoder för mekanisk hjärtklaff eller mitralisstenos, inkluderades. I den aktuella analysen (Tabell 1) har vi sökt förmaksflimmerdiagnoser under upprepade 5-årsperioder samt redovisat andelen som under ett år hämtat ut respektive läkemedel. In- och utflyttade samt avlidna patienter har exkluderats. För detaljerade beskrivningar av metodik se respektive publikation.
I pre-NOAK-eran återfanns 12 procent av patienterna endast i primärvården, vilket hade betydelse för riskskattningen [22]. Samsjuklighet var vanlig, och medelpoäng på CHA2DS2-VASc var 4,67 för kvinnor och 3,14 för män [22]. Kvinnorna hade således en högre risk än männen även utan poängen för kvinnligt kön. 2011 fanns en markant underbehandling med warfarin (Tabell 1). Endast hälften hade hämtat ut warfarin, medan ASA som monoterapi hämtats ut av 32 procent och ingendera av 17 procent. Bland de äldsta patienterna var ASA ännu vanligare. En studie av könsskillnader i SLL visade att kvinnor behandlades med warfarin i lägre utsträckning än män (och oftare med ASA) 2011 men att skillnaderna hade jämnats ut 2015 i alla åldersgrupper utom hos dem som var äldre än 80 år [23].
En studie av kliniska utfall i SLL innan NOAK-eran [24] visade en incidens av ischemisk stroke på 1,8 procent i warfaringruppen, 4,2 procent i ASA-gruppen och 2,0 procent utan behandling (med både lågrisk- och högriskpatienter) [24]. Hemorragisk stroke inträffade hos 0,6 procent av dem som behandlades med warfarin eller ASA, respektive 0,4 procent utan behandling. Allvarlig blödning återfanns hos 2,4 procent, 3,1 procent respektive 2,0 procent. Grupperna skiljde sig markant med mycket hög 1-årsmortalitet hos patienter med ASA eller ingen behandling. Vi jämförde inte utfall med warfarin eller ASA på grund av gruppernas olikhet men visade en stor strokebörda hos äldre högriskpatienter utan warfarin [24], i överensstämmelse med resultat från Västra Götaland [25].
Introduktionen av NOAK
En ökad användning av OAK på bekostnad av mindre effektiv ASA-behandling var angelägen samtidigt som säkerheten vid införandet av NOAK var viktig. Vi bedrev utbildningsaktiviteter om nytta och risker med OAK-behandling i hela sjukvården, inklusive opererande specialiteter, enligt Kloka listan-konceptet [26], och hade flera utfrågningar med berörda företag. Samtidigt pågick många utbildnings- och marknadsföringsaktiviteter från industrin samt vetenskapliga möten om NOAK. Vi påpekade även att NOAK-behandling inte är så oproblematisk som ofta framfördes vid tidpunkten och att erfarenheter från sjukvården var viktiga att bevaka.
Med ökat fokus på förmaksflimmer har antalet patienter med en icke-valvulär förmaksflimmerdiagnos ökat kraftigt, och deras behandling har förbättrats avsevärt (Tabell 1). Rekommendationerna i Kloka listan vilar på principen att begränsa antalet läkemedel som rekommenderas i rutinsjukvården med syfte att underlätta en säker läkemedelsanvändning. I SLL valde vi att rekommendera apixaban i första hand [12], vilket haft ett stort genomslag (Figur 1).
Nyinsättningarna skiftade gradvis från warfarin till NOAK (Figur 1). OAK-behandlingen totalt sett hade 2017 ökat till drygt 77,3 procent, och endast 7 procent hade ASA i monoterapi (Tabell 1). NOAK dominerar nu totalt sett även bland de äldre (Tabell 1).
Nyinsättningar av antitrombotisk behandling vid förmaksflimmer i SLL specialstuderades under en period från mars 2015 till februari 2016 [27]. Läkemedelsvalen var hos 68,3 procent NOAK, 25,0 procent warfarin och 6,7 procent ASA. Hälften av nyinsättningarna av OAK var övergångar från ASA. Vid hög strokerisk (CHA2DS2-VASc ≥5 poäng) och hög ålder var ASA relativt sett vanligare, medan warfarin var vanligare vid hög blödningsrisk. Bland NOAK föredrogs apixaban i ökande grad vid stigande ålder och ökande strokerisk samt vid hög blödningsrisk, medan förhållandet var det omvända för dabigatran. Val av rivaroxaban påverkades inte av dessa parametrar. Warfarin initierades oftast inom primärvården medan NOAK oftast initierades av kardiologer, med allmänläkare som näst vanligaste förskrivare [27].
Observationella studier
Flera observationsstudier har jämfört utfall med NOAK eller warfarin vid förmaksflimmer. En aktuell metaanalys bekräftar resultaten från prövningarna [28]. Man fann likartad risk för ischemisk stroke men färre intrakraniella blödningar med NOAK jämfört med warfarin. Apixaban associerades med färre GI-blödningar och färre allvarliga blödningar, medan dabigatran och rivaroxaban associerades med fler GI-blödningar. Apixaban och dabigatran associerades även med lägre mortalitet [28]. En metaanalys med fler apixabanstudier (n = 16) visade färre intrakraniella blödningar med apixaban jämfört med både warfarin och rivaroxaban, men inte jämfört med dabigatran [29]. Randomiserade jämförelser av olika NOAK saknas avseende kliniska utfall.
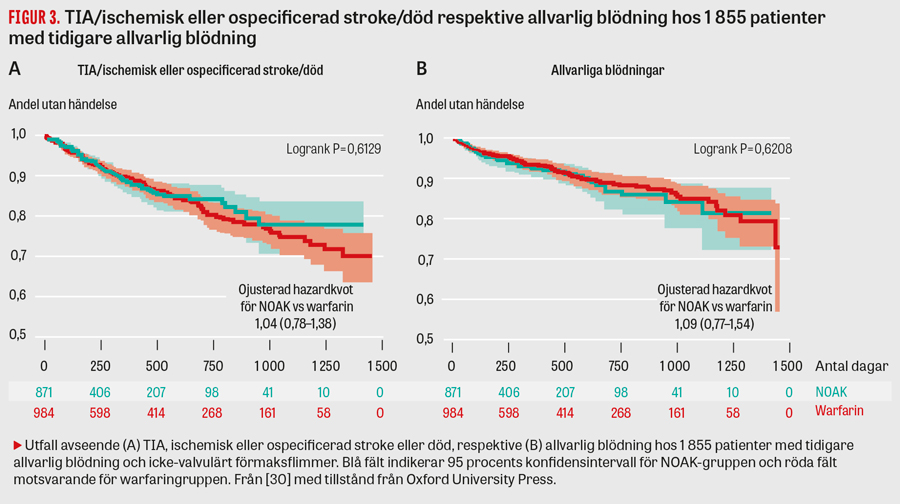
Vi har i SLL jämfört 9 279 NOAK-behandlade med 12 919 warfarin-behandlade patienter med förmaksflimmer (nyinsatta på OAK) avseende kliniska utfall under åren 2012–2015 [30]. NOAK-patienterna var något yngre och hade lägre CHA2DS2-VASc-poäng (3,42 jämfört med 3,68). Ettårsincidensen av ischemisk stroke var 1,2 procent med NOAK och 1,5 procent med warfarin (hazardkvot [HR] 0,81 med 95 procents konfidensintervall [95KI] 0,64–1,02 efter full multivariat justering); allvarliga blödningar inträffade hos 3,0 versus 2,8 procent, varav GI-blödningar var 1,6 versus 1,2 procent (HR 1,28; 95KI 1,03–1,58). Hemorragiska stroke var halverade med NOAK jämfört med warfarin (HR 0,55; 95KI 0,33–0,91) men incidenserna var låga, 0,2 respektive 0,4 procent. Av intresse är att NOAK var lika effektiva och säkra som warfarin även i högriskgrupper med ålder ≥80 år (Figur 2) eller tidigare allvarlig blödning (Figur 3).
Vi studerade även persistens med nyinsatt OAK-behandling i SLL och fann att den var 88 procent efter 1 år och 83 procent efter 2 år [31]. Bäst persistens sågs för apixaban (endast 1-årssiffror) och warfarin [31]. Detta ska jämföras med behandlingsavbrott under cirka 2 år hos 17–24 procent av patienterna i de kliniska prövningarna [13-15].
Diskussion
Införandet av NOAK har inneburit ett paradigmskifte för strokeprofylax vid förmaksflimmer. Lanseringen av NOAK satte förmaksflimmer i fokus, och både diagnostiken (10 000 fler patienter med förmaksflimmer sedan 2011) och OAK-behandlingen har ökat markant i SLL. Vi har nått Socialstyrelsens mål att minst 80 procent av dem som har indikation för OAK ska behandlas [9], men arbetet kring strokeprofylax vid förmaksflimmer är inte avslutat i och med det.
Vi valde att gå försiktigt fram eftersom NOAK bör hanteras med samma respekt för blödningar som warfarin och en ny antikoagulationsbehandling för en stor patientgrupp som innehåller många äldre och sköra patienter ställer krav på kompetens inom många delar av sjukvården. Stockholms läns läkemedelskommitté har bedrivit en omfattande utbildningsverksamhet med besök av informationsläkare och informationsapotekare på vårdcentraler, klinikmöten och symposier samt skriftlig information på www.janusinfo.se. En lathund om OAK-behandling vid förmaksflimmer har uppdaterats vartefter [32] liksom en skrift om orala antitrombotiska läkemedel vid blödning och inför kirurgi [33]. Samtidigt har det förekommit många aktiviteter från andra aktörer med intresse av frågan.
NOAK har i observationella studier visat sig hålla vad de lovar, och vissa skillnader mellan olika NOAK som setts i prövningarna har bekräftats [28, 29]. Vår studie visade att NOAK var minst lika effektiva och säkra som warfarin även hos äldre och högriskpatienter för blödning [30]. Vi har en decentraliserad warfarinbehandling och vet inte hur goda TTR-värden vi har i SLL. En studie från Auricula (Nationellt kvalitetsregister för patienter med atrialt flimmer och antikoagulation) jämförde NOAK-behandlade patienter med matchade warfarinpatienter med en medel-TTR på 71,4 procent [34]. Man fann samma risker för ischemisk stroke och GI-blödningar med NOAK och warfarin, medan NOAK-patienterna hade färre intrakraniella och allvarliga blödningar. Att vi fann en ökad risk för GI-blödningar och ingen minskad risk för allvarliga blödningar med NOAK kan förklaras av vårt oselekterade totalmaterial i SLL [30]. Dessa svenska resultat kan sammantaget tolkas som att vi har en bra standard på warfarinbehandlingen och att NOAK ändå är minst lika bra.
Framtida utmaningar
Antalet patienter med en förmaksflimmerdiagnos ökar, men mörkertalet av odiagnostiserade patienter är sannolikt stort. Generell screening med tum-EKG har avböjts av Socialstyrelsen [35] men detta kan komma att modifieras om STROKE-STOP-studien, där 75–76-åriga individer screenats med tum-EKG [35], får ett bra behandlingsutfall. En enkel åtgärd som rekommenderas av Europeiska kardiologsällskapet [3] och i Kloka listan 2018 är opportunistisk pulspalpation som vid misstanke om förmaksflimmer följs upp med EKG etc [3].
Europeiska kardiologsällskapet:s proaktiva inställning till strokeprofylax med NOAK har fallit väl ut. Med en kraftigt ökad OAK-behandling ser vi goda behandlingsresultat. När vi nu uppnått Socialstyrelsens mål för OAK-behandling vid förmaksflimmer kan man fråga sig om detta arbiträra mål bör höjas. Vi behöver närmare studera om ännu fler gamla och sköra patienter med höga stroke- och blödningsrisker bör behandlas. Omvänt bör vi även studera om vi har en överbehandling av patienter med låg strokerisk. En återkommande bevakning av förmaksflimmerpatienternas behandling och utfall behövs.
Dosreducering av NOAK var mycket vanligare i SLL (32 procent totalt, 72 procent vid ålder ≥80 år) [30] än i prövningarna (till exempel 4,7 procent med apixaban [15]). Hos de äldsta förefaller dosreducering vara adekvat, men hos patienter under 80 år verkar man tappa i effektivitet utan att behandlingen blir säkrare [30]. Flera studier har ifrågasatt om dosreduktion överanvänds [37-39], och problemet behöver belysas ytterligare.
Effekterna av NOAK är koncentrationsberoende, och dosjusteringar för att nå bästa nytta/risk-balans borde vara en fördel även med NOAK. Goda underlag för detta finns för dabigatran [40] och edoxaban [41] och visst underlag även för apixaban [42]. Det finns en stor variation i dalvärden för dabigatran [43] och apixaban [44] hos patienter som erhållit dosering enligt Fass. En ökad individualisering av NOAK-doseringar bör vara till nytta för många patienter. NOAK-mätningar är även av värde i samband med blödningar och inför invasiva ingrepp [11].
Blödningar är ett viktigt problem även med NOAK. Vi behöver få mer erfarenhet av att reversera antikoagulationen i samband med akuta ingrepp och vid allvarliga blödningar. För dabigatran finns en specifik antidot, idarucizumab (Praxbind), medan allvarliga blödningar med FXa-hämmarna får hanteras med protrombinkomplexkoncentrat som medför risk för trombos [11, 45]. Antidoten mot FXa-hämning, andexanet-alfa, är ännu inte godkänd och erfarenheterna av NOAK-reversering är generellt begränsade.
Warfarin behövs fortfarande, exempelvis hos patienter med mekaniska hjärtklaffproteser eller med mycket hög tromboembolirisk såsom ärftliga koagulationsrubbningar eller antifosfolipidsyndrom. I takt med att förskrivningen av warfarin minskar kommer kompetensen i sjukvården att hantera detta mer komplicerade läkemedel att minska. Det är därför viktigt att kompetens säkerställs med särskilda mottagningar för vård av warfarinpatienter och rådgivning. Patienter som behandlas med warfarin bör också erbjudas utbildning i självmätning av PK(INR), vilket i SLL testats i projektform med stor framgång och hög patientnöjdhet.
Nyligen publicerade resultat från SLL [46] visar att strokeincidensen hos patienter med förmaksflimmer gått ner markant mellan 2012 och 2017, från 2,01 till 1,17 per 100 personår (incidenskvot 0,58; 95KI 0,52–0,65). Den ökade OAK-användningen synes ha bidragit med 10 procent av den totala nedgången om 37 procent (efter justering), men vi har även en nedgång av stroke som inte är relaterad till förmaksflimmer [2, 46]. Bättre kardiovaskulär prevention med ökad användning av statiner, bättre blodtryckskontroll och livsstilsinterventioner är sannolikt bidragande faktorer. Hypertoni är en etiologisk faktor för förmaksflimmer, och ett högt blodtryck ökar riskerna för både stroke och allvarlig blödning [47-49]. En viktig uppgift i framtiden är att ytterligare förbättra den allmänna kardiovaskulära preventionen och särskilt omhändertagandet av hypertoni vid förmaksflimmer.
Sammanfattningsvis har stora framsteg skett vad gäller strokeprofylax vid förmaksflimmer, men mycket återstår att »finslipa«. Efter ett gradvis införande är NOAK-behandling nu etablerad som förstahandsval för strokeprofylax vid förmaksflimmer i SLL, och ASA används allt mindre. Detta har bidragit till att uppnå nationella behandlingsmål samt en markant minskning av strokeinsjuknandet i SLL.
Potentiella bindningar eller jävsförhållanden: Inga uppgivna.